АРЕНЫ. БЕНЗОЛ.
Ароматические углеводороды (Арены) – это органические соединения, в молекулах которых имеется одно или несколько бензольных колец. Бензольное кольцо, или ядро, – циклическая группа атомов углерода с особым характером связей.
Общая формула - CnH2n-6
С6H6 – бензол, родоначальник гомологического ряда аренов
Первую структурную формулу бензола предложил в 1865 г. немецкий химик Ф.А.Кекуле:
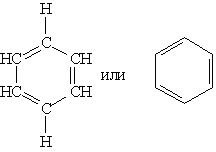 Физические свойства
Физические свойства
Бензол и его ближайшие гомологи – бесцветные жидкости со специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне.
Все арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах.
Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при длительном воздействии), может нарушать структуру хромосом.
Большинство ароматических углеводородов опасны для жизни, токсичны.
Получение.
1) В промышленности: выделяют из нефти и угля методом фракционной перегонки, риформингом; из каменноугольной смолы и коксового газа.
2) Тримеризация ацетилена – реакция Зелинского:
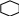
 3С2H2 600°C, акт. уголь → C6H6 (3СН≡СН→ )
3С2H2 600°C, акт. уголь → C6H6 (3СН≡СН→ )
Химические свойства аренов
1. реакции окисления
Горение (коптящее пламя):
2C6H6 + 15O2 t → 12CO2 + 6H2O + Q
Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки.
2. Реакции присоединения (труднее, чем у алкенов)
1. Галогенирование
C6H6 +3Cl2 hν → C6H6Cl6 (гексахлорциклогексан - гексахлоран)
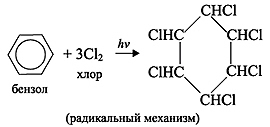
2. Гидрирование
C6H6 + 3H2 t,Pt или Ni → C6H12 (циклогексан)
3.реакции замещения (легче, чем у алканов)
1. Галогенирование
C6H6 + Cl2 AlCl3→ C6H5-Cl + HCl (хлорбензол)

C6H6 + 6Cl2 t ,AlCl3→ C6Cl6 + 6HCl (гексахлорбензол)
2. Нитрование (с азотной кислотой)
C6H6 + HO-NO2 t, H2SO4→ C6H5-NO2 + H2O
нитробензол - запах миндаля!

Применение бензола и его гомологов
Бензол C6H6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C6H5NO2 (растворитель, из него получают анилин), хлорбензола C6H5Cl, фенола C6H5OH, стирола и т.д.
Толуол C6H5–CH3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Хлорпроизводные бензола используют в качестве пестицидов. Гексахлорбензол С6Сl6 – фунгицид(применяют для сухого протравливания семян пшеницы и ржи против твердой головни), гексахлорциклогексан (гексахлоран) С6Н6Сl6 – инсектицид (используют для борьбы с вредными насекомыми).
Стирол C6H5 – CH = CH2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.





 Физические свойства
Физические свойства
 3С2H2 600°C, акт. уголь → C6H6 (3СН≡СН→ )
3С2H2 600°C, акт. уголь → C6H6 (3СН≡СН→ )













