СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока

Была в сети 30.06.2024 07:02

Бектурсунова Клара Бектурсуновна
Химия мугалими
29 лет
Местоположение
Кыргызстан, Жаны Базар
Специализация
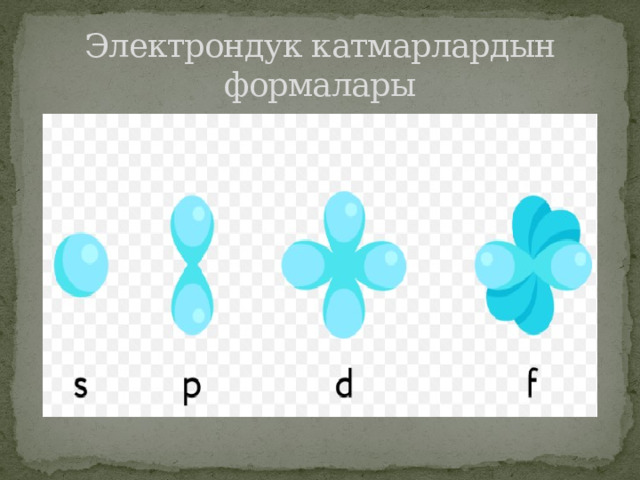
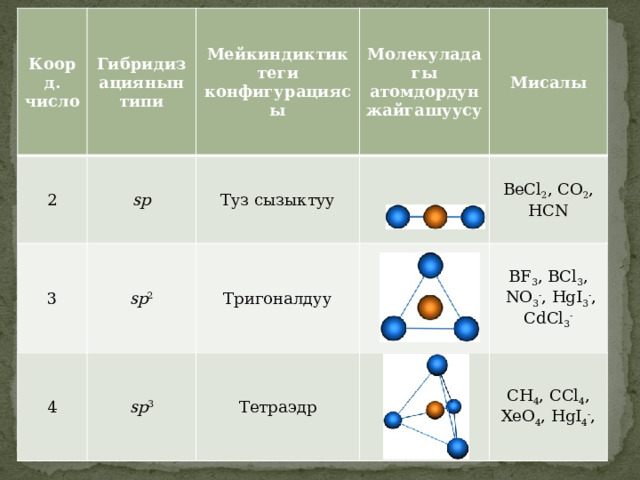
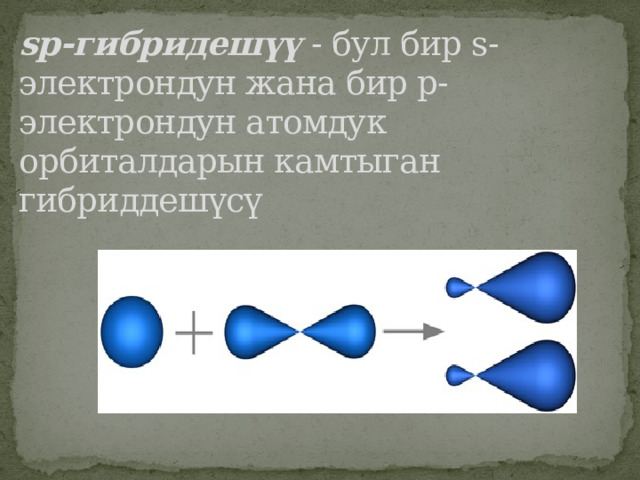
Атом орбиталдарынын гибриддешуусу химия
Категория:
Химия
12.05.2024 18:17