Просмотр содержимого документа
«Атомдун электрондук катмарларынын түзүлүшү»
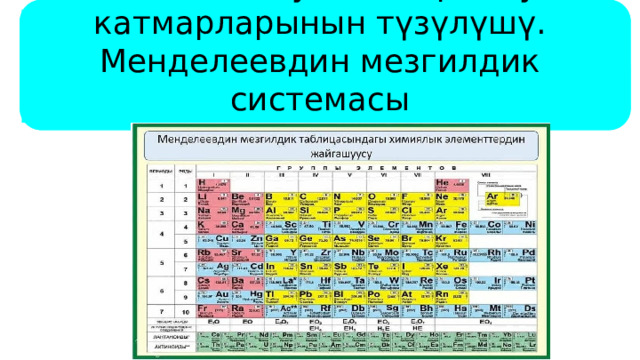
Тема: Атомдун электрондук катмарларынын түзүлүшү. Менделеевдин мезгилдик системасы
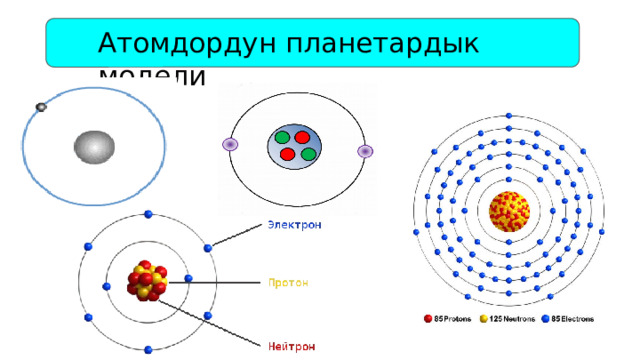
Атомдордун планетардык модели
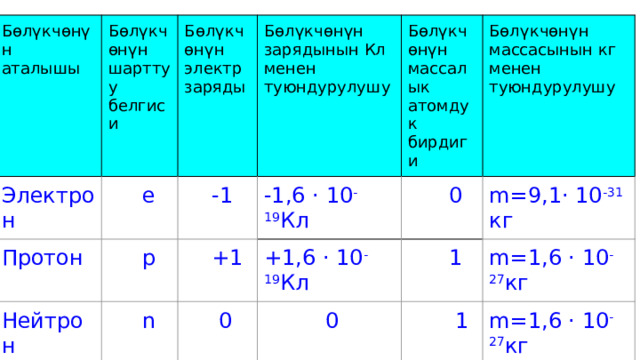
Бөлүкчөнүн аталышы
Бөлүкчөнүн шарттуу белгиси
Электрон
е
Протон
Бөлүкчөнүн электр заряды
Нейтрон
Бөлүкчөнүн зарядынын Кл менен туюндурулушу
р
-1
Бөлүкчөнүн массалык атомдук бирдиги
n
+1
-1,6 ⋅ 10 -19 Кл
Бөлүкчөнүн массасынын кг менен туюндурулушу
+1,6 ⋅ 10 -19 Кл
0
0
1
m=9,1⋅ 10 -31 кг
0
m=1,6 ⋅ 10 -27 кг
1
m=1,6 ⋅ 10 -27 кг

Атомдун кванттык саны
Башкы кванттык саны
Орбиталдык кванттык саны
Магниттик кванттык саны
Спиндик кванттык саны

Башкы кванттык сан -n
Электрондордун энергиясын жана анын ядродон канчалык аралыкта кыймылдап жүргөнүн көрсөтөт.
Башкы кванттык сандын мааниси мезгилдин катар номерине барабар.
n=1,2,3,4,5,6,7
Же энергетикалык деңгээлдер-К,L,M,N,O,P,Q

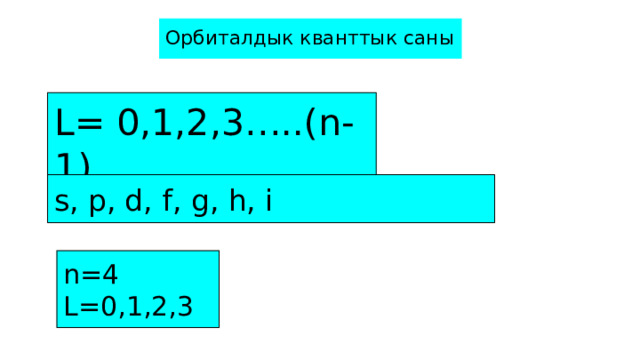
Орбиталдык кванттык саны
L= 0,1,2,3…..(n-1)
s, p, d, f, g, h, i
n=4
L=0,1,2,3
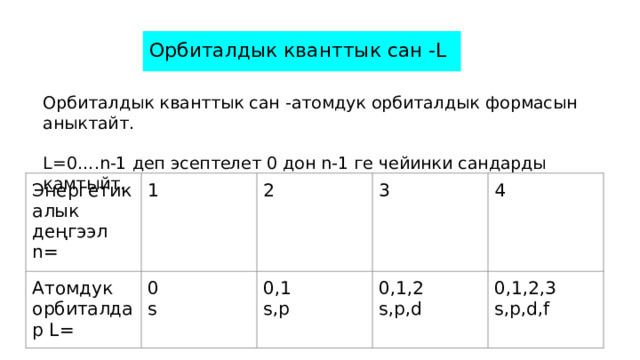
Орбиталдык кванттык сан -L
Орбиталдык кванттык сан -атомдук орбиталдык формасын аныктайт.
L=0….n-1 деп эсептелет 0 дон n-1 ге чейинки сандарды камтыйт.
Энергетикалык деңгээл n=
1
Атомдук орбиталдар L=
2
0
3
s
0,1
4
s,p
0,1,2
s,p,d
0,1,2,3
s,p,d,f
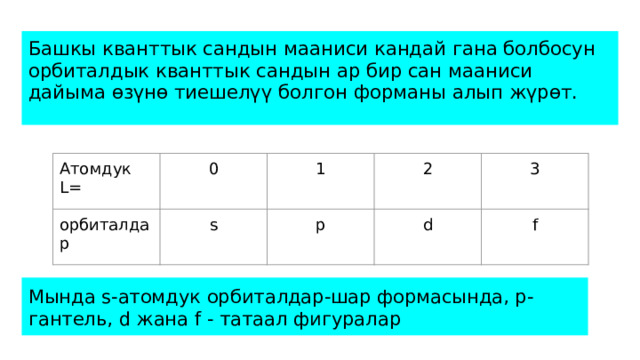
Башкы кванттык сандын мааниси кандай гана болбосун орбиталдык кванттык сандын ар бир сан мааниси дайыма өзүнө тиешелүү болгон форманы алып жүрөт.
Атомдук L=
0
орбиталдар
1
s
2
p
3
d
f
Мында s-атомдук орбиталдар-шар формасында, р-гантель, d жана f - татаал фигуралар


Магниттик кванттык саны
Мейкиндиктеги атомдук орбиталдын сырткы салыштырмалуу магниттик жана электрдик талаасынын багытын мүнөздөйт. Магниттик кванттык санды m-тамгасы менен белгилейбиз
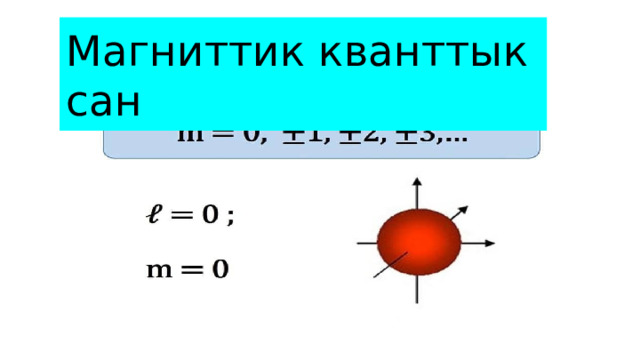
Магниттик кванттык сан
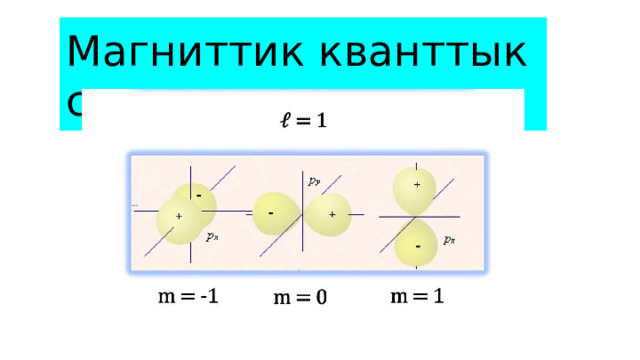
Магниттик кванттык сан
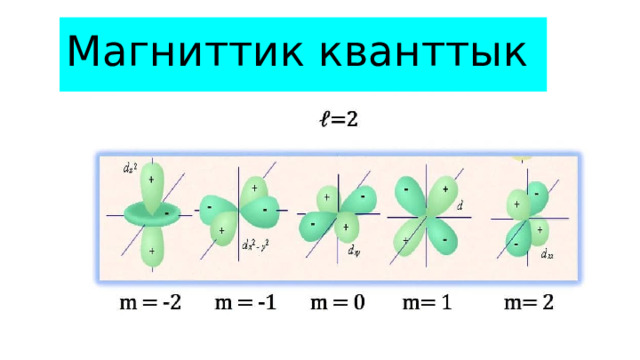
Магниттик кванттык сан
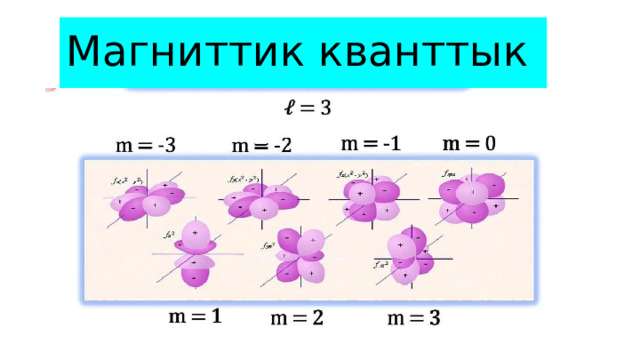
Магниттик кванттык сан

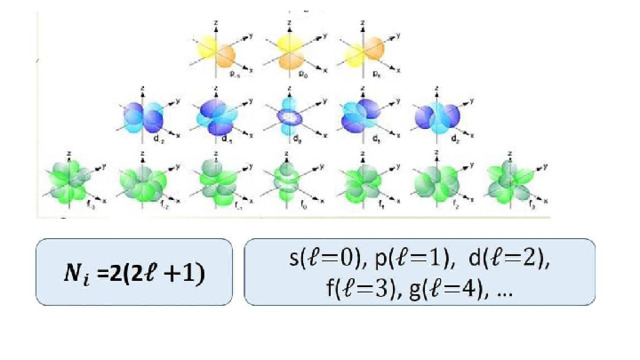


Менделеевдин мезгилдик системасы




































