Цель урока: продолжить формирование у учащихся понятия «кислота» на примере азотной кислоты; создать условия для выявления общих и специфических свойств азотной кислоты посредством решения экспериментальных задач.
Задачи:
Образовательные: изучить химические свойства азотной кислоты; закрепить материал о реакциях ионного обмена и окислительно-восстановительных, закрепить навыки работы с лабораторным оборудованием.
Развивающие: продолжить развитие умений выделять главное, устанавливать причинно-следственные связи, применять знания на практике.
Воспитательные: формирование привычки к самостоятельному труду, аккуратности, навыков работы в группе.
Формируемые УУД:
-Личностные:
- самоопределение – повысить мотивацию учащихся через ученический химический эксперимент;
- смыслообразование – способствовать проявлению интереса к новому; умение использовать имеющиеся знания и личный опыт при изучении физико-химических свойств азотной кислоты;
-Коммуникативные – умение планировать парную и групповую работу на уроке; умение слушать и понимать речь учителя, одноклассников, обмениваться мнениями при работе;
-Познавательные – формулировать цели урока; устанавливать причинно-следственные связи при изучении химических свойств азотной кислоты; выдвигать гипотезу и доказывать ее посредством химического эксперимента;
-Регулятивные – принимать и сохранять учебную задачу; адекватно воспринимать оценочную информацию со стороны одноклассников и учителя по поводу правильности ответов; развивать волевую регуляцию.
Задачи урока:
- Образовательные:
- расширить и привести в систему знания о свойствах азотной кислоты;
- продолжить совершенствование умений составлять уравнения химических реакций, написания полных и сокращенных ионных уравнений реакций.
- Развивающие:
- продолжить формирование навыков самостоятельной работы учащихся;
- развитие умений сравнивать, делать выводы, читать схемы;
- Воспитательные:
- продолжить формирование культуры работы с реактивами;
- воспитывать сотрудничество;
- способствовать развитию грамотной химической речи.
Тип урока: урок усвоения новых знаний.
Методы обучения: частично-поисковый, исследовательский, репродуктивный; словесный (рассказ, эвристическая беседа); наглядные (презентация, видео опыт); работа с книгой.
Формы работы: фронтальная, работа в парах, индивидуальная.
Вещества: растворы белка,азотной кислоты, гидроксида натрия, карбоната натрия, фенолфталеина, метилоранжа, оксид магния
Ход урока.
I. Подведение к теме урока. Совместное целеполагание и проектирование урока.
Девиз урока: "Всё от песчинок до планет из элементов состоит единых"
Создание проблемной ситуации.
Переведите с алхимического языка запись:
“…“Крепкая вода” пожирает “луну”, выпуская “лисий хвост”. Сгущение полученной жидкости порождает “адский камень”, который чернит ткань, бумагу и руки. Чтобы “луна” опять взошла, прокаливай “адский камень” в печи”.
О каких веществах идет речь?
1 Назовите вещества: N2O, NO, NO2, NH3, N2, NH4NO3, HNO3
Что общего во всех этих соединениях?
2 Определите степень окисления азота в них
3 Какие соединения азота изучены? Что еще не рассмотрели?
4 Как звучит тема урока?
Учащиеся, называют тему урока: «Азотная кислота HNO3».
Учитель дополняет – «Особая».
Какова цель урока?
Что мы хотели бы узнать об азотной кислоте?
Учащиеся, формулируют цели урока (На сладе)
Учитель. Вещество, которое мы сегодня изучаем особое, необычное. Давайте, для начала выясним, почему же это вещество, мы относим к классу кислот? (Состоит из элементов – неметаллов, содержит водород, проявляет свойства кислот).
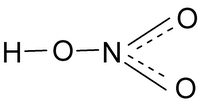
Рассмотрим строение молекулы азотной кислоты: Атом азота максимально может образовывать четыре ковалентные связи – три по механизму спаривания электронов и одну по донорно – акцепторному механизму, что связано с его электронным строением.
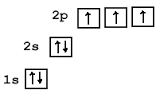
Пять ковалентных связей атом азота, образовывать не может из-за отсутствия свободных атомных орбиталей на втором энергетическом уровне. Опытным путём доказано, что в молекуле азотной кислоты между двумя атомами кислорода и атомом азота две химические связи абсолютно одинаковые. Степень окисления азота +5, а валентность равна IV.
Учитель. Вспомним, а какие общие свойства характерны для кислот?
(изменяют цвет индикатора, взаимодействуют с металлами, оксидами металлов, основаниями и солями)
Учитель. Проверим, некоторые общие свойства азотной кислоты, опытным путем. Но сначала вспомним правила ТБ при работе с кислотами. Ученики, выполняют опыты.
Опыт 1.
В раствор азотной кислоты добавляем 2-3 капли метилоранжа. Раствор окрасился в розовый цвет. Почему изменилась окраска индикатора? (В ней присутствуют ионы водорода). Напишите уравнение диссоциации азотной кислоты. (Ученик на доске пишет уравнение)
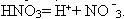
Опыт 2.
Взаимодействие с оксидами металлов. В пробирку с оксидом магния наливаем азотную кислоту. Оксид магния растворяется. Напишите уравнение реакции.
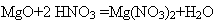 . Напишите молекулярное, полное ионное и сокращенное ионные уравнения. (Ученик на доске пишет уравнение)
. Напишите молекулярное, полное ионное и сокращенное ионные уравнения. (Ученик на доске пишет уравнение)
Опыт 3.
Взаимодействие с основаниями. В пробирку с раствором гидроксида натрия добавляем азотную кислоту (в гидроксиде натрия раствор фенолфталеина).
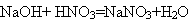 . Напишите молекулярное, полное ионное и сокращенное ионные уравнения. (Ученик на доске пишет уравнение)
. Напишите молекулярное, полное ионное и сокращенное ионные уравнения. (Ученик на доске пишет уравнение)
Демонстрация опыта взаимодействие азотной кислоты с раствором карбоната натрия. Напишите самостоятельно молекулярное, полное ионное и сокращенное ионные уравнения.
Таким образом, мы подтвердили опытным путем, что азотная кислота, обладает общими свойствами всех кислот.
Учитель. А какое из перечисленных свойств кислот, мы не рассмотрели? (Ученик. Взаимодействие кислот с металлами).
Учитель. Верно. И сделали мы это не из-за невнимательности. Как обычно реагируют кислоты с металлами? (Ученик. Образуется соль и выделяется водород).
Учитель. Есть свойства, которые позволяют назвать эту кислоту «особой».
В начале урока мы расставляли степени окисления в соединениях азота. Давайте, вспомним какая степень окисления азота в кислоте (Ученики. +5)
Значит азотная кислота – это… (Ученик. Окислитель, азот в высшей степени окисления).
Причем, сильный окислитель. Именно поэтому азотной кислоте присущи специфические или «особые» свойства. Посмотрите, у вас, на столе таблица, в которой отображена схема взаимодействия азотной кислоты с металлами. Обратите внимание на то, что выделено жирным шрифтом.
(Ученик читает: кислота, в реакциях с металлами, не выделяет водород). Это правило необходимо запомнить. Как видите, продукты реакции зависят от концентрации кислоты и активности металла, образуется соль, вода и соединение азота. Азотная кислота не реагирует с золотом, платиной. Концентрированная азотная кислота, так же не реагирует с алюминием, железом, хромом. Посмотрим, как пример, взаимодействие азотной кислоты с медью. (просмотр видеоопыта). Запишите уравнение реакции. Выделяющийся газ (NO2) называют «бурым газом», в истории сохранилось и другое его название «лисий хвост». Попробуйте теперь расшифровать первое предложение в алхимической загадке. О каких веществах шла речь? Кто попробует составить уравнение этой реакции на доске?
Ag + 2HNO3 = AgNO3 + NO2 + H2O
Также азотную кислоту называют «взрывоопасной». Подтвердите этот эпитет, опираясь на данные таблицы в учебнике на странице 55. Раздел специфические свойства. (Ученик читает: при нагревании и под действием света концентрированная азотная кислота разлагается. Взрывоопасна из – за выделяющегося кислорода)
Учитель. Есть еще специфическое свойство. Если концентрированная азотная кислота попадает на кожу, то остается желтое пятно. Кислота реагирует с белками, вызывая их денатурацию, вследствие этого появляется характерное окрашивание. Такая реакция называется ксантопротеиновой
Демонстрация эксперимента.
Закрепление. Что же мы узнали об азотной кислоте на этом уроке? Выберите из предложенных заданий, то с которым вы справитесь, с учетом полученных знаний. Базовый уровень обязателен для всех. Повышенный уровень для претендентов на более высокую оценку.
Давайте проверим, пришли ли мы к запланированным результатам. Выполните тест.
| I вариант | II вариант |
| 1. Валентность азота в азотной кислоте равна: 1) III 2) IV 3) V 4) II | 1. Степень окисления азота в азотной кислоте равна: 1) +3 2) +4 3) +5 4) -3 |
| 2. Разбавленная азотная кислота не реагирует с: 1) CO2 2) Fe(OH)3 3) Hg 4) CuO | 2. С концентрированной азотной кислотой при комнатной температуре реагирует: 1) Cu, Al 2) Mg, Ag 3) Al, Fe 4) Pb, Al |
| 3. При взаимодействии раствора кислоты с оксидом металла образуются: 1) соль и металл, 2) соль и водород, 3) соль и оксид водорода, 4) соль и вода.
| 3. Газ, образующийся при взаимодействии ртути с концентрированной азотной кислотой: 1) H2 2) N2O 3) NO 4) NO2 |
| 4. Молекула азотной кислоты в водном растворе диссоциирует на ионы: 1) H+ и 3 NO-, 2) H+ и NO3-, 3) H+ и NO2, 4) H- и NO3+. | 4. Взаимодействие кислоты и гидроксида металла является реакцией: 1) соединения, 2) разложения, 3) замещения, 4) обмена (нейтрализации).
|
Ответы
| № задания | 1 | 2 | 3 | 4 |
| I вариант | 2 | 1 | 4 | 2 |
| II вариант | 3 | 2 | 4 | 4 |
Задание
Повышенный уровень сложности.
Как известно, кислоты являются едкими веществами. Азотная кислота – не исключение. Предложите вариант оказания первой медицинской помощи при ожоге раствором азотной кислоты. Каким из веществ (раствором NaOH, раствором NaHCO3, кристаллами лимонной кислоты) вы нейтрализуете кислоту, чтобы не было сильного ожога? Объясните ваши действия и составьте уравнение химической реакции, обеспечивающей нейтрализацию кислоты на кожных покровах.
Примерные ответы:
Смыть поверхность кожи обильной струёй воды. Кислота реагирует с солями, значит, место ожога нужно обработать раствором питьевой соды, гидрокарбоната натрия, NaНСО3, который можно найти в домашней аптечке или кухонном шкафу.
Приведено уравнение реакции между азотной кислотой и гидрокарбонатом натрия.
Нейтрализацию кислоты щёлочью проводить нельзя, т.к. щёлочь может вызвать дополнительный химический ожог. Лимонная кислота не только не смягчит ожог, а усилит его, т.к. кислота с кислотой не реагирует.
Оцените свою работу (самопроверка). Поставьте, пожалуйста, восклицательный знак на тех моментах, где вы допустили ошибку. На эти вопросы при подготовке домашнего задания обратите особое внимание.
Домашнее задание: § 19, задача №2, страница 60.Составить по одному уравнению реакций металла (на выбор) с концентрированной и разбавленной азотной кислотой.
Дополнительное задание
Найти интересные факты об открытии азотной кислоты.
Подготовить сообщение с презентацией «Применение азотной кислоты»
На следующем уроке мы рассмотрим соли азотной кислоты – нитраты. Закончим расшифровку алхимической загадки, узнаем, как из «адского камня» вернуть «луну»
Подведение итога, выставление оценок.


















