Банк заданий
ХИМИЯ 8 класс
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p1:
а) К; б) F; в) Al; г) Be.
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p5:
а)Cl; б) Al; в) Na; г) Be.
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p3:
а) N; б) P; в) Cl; г) Si.
*Чему равен порядковый номер элемента, который находится в четвертом периоде, в главной подгруппе второй группы?
а) 10; б) 30; в)20; г) 40.
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p2:
а) К; б) Si; в) Al; г) F
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p6:
а) Na; б) Ar; в) Cl; г) Be.
*Укажите химический элемент, атомы которого имеют электронную формулу 1s22s22p63s23p6:
а) Na; б) Ar; в) Cl; г) Be.
*Среди химических элементов Мg, Si, S, Cl более ярко свойства металла выражены у:
а) магния; б) азота; в) серы; г) хлора.
*В порядке возрастания электроотрицательности атомов химические элементы расположены в следующем ряду:
а) F, Cl, Br, I;
б) I, Br, Cl, F;
в) Cl, S, P, Si;
г) F, O, N, C.
*В ряду химических элементов Li — Be —В — С металлические свойства
а) ослабевают; в) не изменяются;
б) усиливаются; г) изменяются периодически
*В каком ряду простые вещества расположены в порядке усиления металлических свойств?
а) Mg, Ca, Ва;
б) К, Са, Fe;
в) Na, Mg, Al;
г) Sc, Ca, Mg.
*Среди химических элементов Na, Si, S, Ar более ярко свойства металла выражены у:
а) натрия; б) азота; в) серы; г) аргона
*Ковалентная полярная химическая связь образуется между элементами в соединении:
а) Cl2; б) HCl; в) LiCl; г) NaCl.
*Какой вид химической связи характерен для меди?
а) ковалентная неполярная;
б) металлическая;
в) ионная;
г) ковалентная полярная.
*В молекуле фтора химическая связь
а) ионная;
б) ковалентная полярная;
в) ковалентная неполярная;
г) металлическая.
*Какой вид химической связи в оксиде кальция?
а) ковалентная неполярная;
б) металлическая;
в) ковалентная полярная;
г) ионная.
*Какой вид химической связи в оксиде магния?
а) ковалентная неполярная;
б) металлическая;
в) ковалентная полярная;
г) ионная.
*В молекуле хлора химическая связь
а) ионная;
б) ковалентная полярная;
в) ковалентная неполярная;
г) металлическая
*В каком соединении степень окисления хрома равна+6?
а) Сг2S3;
б) СгО3;
в) СгСl2;
г) Сг.
*Степень окисления азота (-3) в соединении:
а) Na3N;
б) N2O3;
в) N2O5;
г) N2O.
*Степень окисления -3 азот имеет в веществе:
а) N2O3;
б) NH3;
в)N2;
г)NF3.
*Низшие степени окисления азота и серы соответственно равны
а) −З и −2;
б) +1 и +2;
в) +3 и + 2;
г) −1 и −2.
*В каком соединении степень окисления хрома равна+2?
а) Сг2S3;
б) СгО3;
в) СгСl2;
г) Сг.
*Степень окисления +3 азот имеет в веществе:
а) N2O5;
б) NH3;
в) N2;
г) NF3
*К основаниям относится каждое из 2-х веществ:
а) H2O, Na2O;
б) KOH, NaOH;
в) HPO3, HNO3;
г) SO2, Na2O.
*Вещества, расположенные в последовательности оксид – гидроксид – соль, находятся в ряду:
а) CaF2 – NaOH – PbI2;
б) P2O5 – ZnSO4 – Ba(OH)2;
в) CaО – H2CO3 – NaOH;
г) H2O – KOH– K2CO3.
*Вещества, формулы которых —SО3 и Н2S, являются
соответственно
а) основным оксидом и кислотой;
б) кислотным оксидом и солью;
в) кислотным оксидом и кислотой;
г) амфотерным оксидом и кислотой.
*Основным оксидом и щелочью соответственно являются
а) СаО иNаОН;
б) SiO2 и Ва(ОН)2;
в) СuО и Н2SiO3;
г) ВаО и NН4ОН.
*Вещества, формулы которых —CaО и Н2SO4, являются
соответственно
а) основным оксидом и кислотой;
б) кислотным оксидом и солью;
в) кислотным оксидом и кислотой;
г) амфотерным оксидом и кислотой
*К веществам, взаимодействующим с гидроксидом бария, относятся:
а) оксид хлора (V); г) оксид натрия;
б) оксид азота (I); д) оксид марганца (VII);
в) оксид фосфора (III); е) оксид свинца (II).
Ответ:
*С азотной кислотой взаимодействуют:
а) оксид азота (I); г) оксид свинца (II);
б) оксид кальция; д) оксид лития;
в) оксид хрома (VI); е) оксид серы (IV).
Ответ:
*С серной кислотой взаимодействуют:
а) оксид магния; г) оксид азота (II);
б) оксид марганца (VII); д) оксид железа (III);
в) оксид калия; е) оксид углерода (IV).
Ответ:
*С серной кислотой взаимодействуют:
а) оксид азота (V); г) оксид фосфора (III);
б) оксид меди (II); д) оксид алюминия;
в) оксид железа (III); е) оксид азота (I).
Ответ:
*На какой диаграмме распределение массовых долей элементов соответствует количественному составу карбоната калия?
*На какой диаграмме распределение массовых долей элементов соответствует количественному составу нитрат калия?
*На какой диаграмме распределение массовых долей элементов соответствует количественному составу сульфата железа(II)?
*На какой диаграмме распределение массовых долей элементов соответствует количественному составу нитрата железа(II)?
*Установите соответствие между формулами исходных веществ и продуктов реакции
| Исходные вещества | Продукты реакции |
| 1) Mg(OH)2 + HNO3 2) MgCO3 + HNO3 3) CuSO4 + KOH 4) K2O + H2SO4 | а) Mg(NO3)2 + CO2 + H2O б) Cu(OH)2 + K2SO4 в) Mg(NO3)2 +H2O г) K2SO4 +H2O |
*Установите соответствие между формулами исходных веществ и продуктов реакции
| Исходные вещества | Продукты реакции |
| 1) NaOH+ CO2 2) NaOH +CO2 3)Na + H2O 4)NaOH + HCl | а)NaOH + H2 б) Na2CO3 + H2O в)NaCl + H2O г)NaHCO3 |
*Установите соответствие между формулой вещества и реагентами, с которыми это вещество может взаимодействовать.
| Исходные вещества | Продукты реакции |
| 1) CuSO4 +LiOH 2) NH4Cl + KOH 3)CaCO3 +HNO3 | а)Ca(NO3)2 + H2O+CO2 б) Cu(OH)2 + Li2SO4 в)KCl + NH3 +H2O г)NH3+H2O |
*Установите соответствие между формулами исходных веществ и продуктов реакции
| Исходные вещества | Продукты реакции |
| 1)Mg(OH)2 +HCl 2) Mg(OH)2 +CO2 3) Мg + НСl | а) МgСO3 + H2O б) МgСl2+H2 в) МgСl2 г) МgСl2+ H2O |
Часть 2
*Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения.
Ва ВаО Ва(OH)2 ВаСl2 ВаSO4
Р → Р2O5 → H3РO4 → Na3РO4 → Ca3(РO4)2
S → SO2 → SO3 → H2SO4 → Na2SO4
Ca → CaO → Ca(OH)2 →CaСO3 → CaO
C→CO2→Na2CO3→CO2 → CaCO3
Zn → ZnO → ZnCl2 →Zn(OH)2 → ZnO → Zn
Ca → Ca(OH)2 → CaSO4 → BaSO4
C → CO2 → CaCO3 → CO2 → CaCO3
* К раствору силиката натрия массой 20,53 г и массовой долей 15% прилили избыток раствора нитрата бария. Вычислите массу образовавшегося осадка.
Ответ:___________________(Запишите ответ с точностью до десятых)
*60 г сульфида алюминия обработали избытком водного раствора хлороводородной кислоты. Рассчитайте объём (н.у.) газа, выделившегося в результате этой реакции.
Ответ: ___________________ л (Запишите число с точностью до целых.)
*При сгорании серы было получено 8,0 оксида серы (IV). Определите объем (н.у.) израсходованного кислорода.
Ответ: ___________________ л (Запишите число с точностью до десятых)
*К раствору сульфата железа (II) массой 68,4 г и массовой долей 8% прилили избыток раствора хлорида бария. Вычислите массу образовавшегося осадка.
Ответ:_________________(Запишите число с точностью до десятых)
*К раствору силиката натрия массой 10,53 г и массовой долей 10% прилили избыток раствора нитрата бария. Вычислите массу образовавшегося осадка.
Ответ:___________________(Запишите ответ с точностью до десятых)
*К раствору сульфата железа (II) массой 70 г и массовой долей 7% прилили избыток раствора хлорида бария. Вычислите массу образовавшегося осадка.
Ответ:_________________(Запишите число с точностью до десятых)






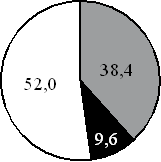
 б
б г
г а
а б
б в
в
 а
а б
б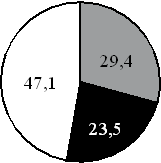 в
в г
г а
а б
б в
в г
г









