Бензол
[править | править код]
Материал из Википедии — свободной энциклопедии
Перейти к навигацииПерейти к поиску
| Бензол |
| 
 |
| Общие |
| Систематическое
наименование | бензол |
| Сокращения | PhH |
| Традиционные названия | фен (Лоран, 1837),
фениловый водород, бензен |
| Хим. формула | C6H6 |
| Рац. формула | C6H6 |
| Физические свойства |
| Состояние | жидкость |
| Молярная масса | 78,11 г/моль |
| Плотность | 0,8786 г/см³ |
| Динамическая вязкость | 0,0652 Па·с |
| Энергия ионизации | 9,24 ± 0,01 эВ[2] |
| Термические свойства |
|
|
| Температура |
| • плавления | 5,5 °C |
| • кипения | 80,1 °C |
| • вспышки | −11 °C |
| • самовоспламенения | 562 °C |
| Пределы взрываемости | 1,2 ± 0,1 об.%[2] |
|
|
| Энтальпия |
| • образования | 82 930 Дж/моль[1] и 49 080 Дж/моль[1] |
| Давление пара | 75 ± 1 мм рт.ст.[2] |
| Химические свойства |
|
|
| Растворимость |
| • в воде | 0,073 г/100 мл |
| Классификация |
| Рег. номер CAS | 71-43-2 |
| PubChem | 241 |
| Рег. номер EINECS | 200-753-7 |
| SMILES | [показать] |
| InChI | [показать] |
| RTECS | CY1400000 |
| ChEBI | 16716 |
| ChemSpider | 236 |
| Безопасность |
| Токсичность | токсичен, обладает канцерогенными и наркотическими свойствами |
| Краткие характер. опасности (H) | H225, H304, H315, H319, H340, H350, H372, H412 |
| Меры предостор. (P) | P201, P210, P280, P308+P313, P370+P378, P403+P235 |
| Сигнальное слово | ОПАСНО! |
| Пиктограммы СГС |      
|
| NFPA 704 |  4 3 0 |
| Приведены данные для стандартных условий(25 °C, 100 кПа), если не указано иное. |
|  Медиафайлы на Викискладе Медиафайлы на Викискладе |
Бензо́л (C6H6, PhH) — органическое химическое соединение, бесцветная жидкость со специфическим сладковатым запахом. Простейший ароматический углеводород. Бензол входит в состав бензина, широко применяется в промышленности, является исходным сырьём для производства лекарств, различных пластмасс, синтетической резины, красителей. Хотя бензол входит в состав сырой нефти, в промышленных масштабах он синтезируется из других её компонентов. Токсичен, канцерогенен. Контаминант.

Содержание
История[править | править код]
Впервые бензолсодержащие смеси, образующиеся в результате перегонки каменноугольной смолы, описал немецкий химик Иоганн Глаубер в книге Furni novi philosophici, опубликованной в 1651 году[3]. Бензол как индивидуальное вещество был описан Майклом Фарадеем, выделившим это вещество в 1825 году из конденсата светильного газа, получаемого коксованием угля. Вскоре, в 1833 году, получил бензол — при сухой перегонке кальциевой соли бензойной кислоты — и немецкий физико-химик Эйльгард Мичерлих. Именно после этого получения вещество стали называть бензолом.
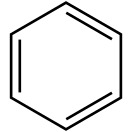
К 1860-м годам было известно, что соотношение количества атомов углерода и атомов водорода в молекуле бензола аналогично таковому у ацетилена, и эмпирическая формула их — CnHn. Изучением бензола серьёзно занялся немецкий химик Фридрих Август Кекуле, которому в 1865 году и удалось предложить правильную — циклическую формулу этого соединения. Известна история о том, что Ф. Кекуле представлял в своём воображении бензол в виде змеи из шести атомов углерода[4]. Идея же о цикличности соединения пришла ему во сне, когда воображаемая змея укусила себя за хвост. Фридриху Кекуле удалось в то время наиболее полно описать свойства бензола.
Физические свойства[править | править код]
Бензол (жидкий)
Бесцветная жидкость со своеобразным резким запахом. Температура плавления = 5,5 °C, температура кипения = 80,1 °C, плотность = 0,879 г/см³, молярная масса = 78,11 г/моль. Подобно ненасыщенным углеводородам бензол горит сильно коптящим пламенем. С воздухом образует взрывоопасные смеси, хорошо смешивается с эфиром, бензином и другими органическими растворителями, с водой образует азеотропную смесь с температурой кипения 69,25 °C (91 % бензола). Растворимость в воде 1,79 г/л (при 25 °C).
Химические свойства[править | править код]
Для бензола характерны реакции замещения — бензол реагирует с алкенами, хлоралканами, галогенами, азотной и серной кислотами. Реакции разрыва бензольного кольца проходят в жёстких условиях (температура, давление).
Взаимодействие с алкенами (алкилирование), в результате реакции образуются гомологи бензола, например, этилбензол и кумол:
{\displaystyle {\mathsf {C_{6}H_{6}+H_{2}C=CH_{2}{\xrightarrow[{}]{AlCl_{3}*HCl}}C_{6}H_{5}CH_{2}CH_{3}}}}
{\displaystyle {\mathsf {C_{6}H_{6}+CH_{2}=CH-CH_{3}{\xrightarrow[{}]{AlCl_{3}*HCl}}C_{6}H_{5}CH(CH_{3})_{2}}}}
Взаимодействие с хлором и бромом в присутствии катализатора с образованием хлорбензола (реакция электрофильного замещения):
{\displaystyle {\mathsf {C_{6}H_{6}+Cl_{2}{\xrightarrow[{}]{FeCl_{3}}}C_{6}H_{5}Cl+HCl}}}
В отсутствие катализатора при нагревании или освещении идёт радикальная реакция присоединения с образованием смеси изомеров гексахлорциклогексана
{\displaystyle {\mathsf {C_{6}H_{6}+3Cl_{2}{\xrightarrow[{}]{T,h\nu }}C_{6}H_{6}Cl_{6}}}}
{\displaystyle {\mathsf {C_{6}H_{6}+6Br_{2}{\xrightarrow[{}]{H_{2}SO_{4}*SO_{3}}}C_{6}Br_{6}+6HBr}}}
Взаимодействие с галогенопроизводными алканов (алкилирование бензола, реакция Фриделя — Крафтса) с образованием алкилбензолов:
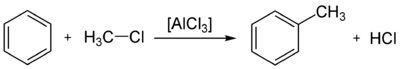
Реакция ацилирования по Фриделю—Крафтсу, бензола ангидридами, галогенангидридами карбоновых кислот приводит к образованию ароматических и жирноароматических кетонов:
{\displaystyle {\mathsf {C_{6}H_{6}+(CH_{3}CO)_{2}O{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COCH_{3}+CH_{3}COOH}}}
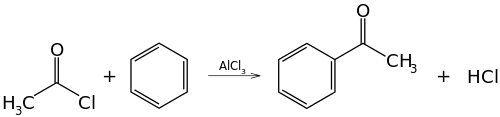
{\displaystyle {\mathsf {C_{6}H_{6}+C_{6}H_{5}COCl{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COC_{6}H_{5}+HCl}}}
В первой и второй реакциях образуется ацетофенон (метилфенилкетон), замена хлорида алюминия на хлорид сурьмы V позволяет снизить температуру протекании реакции до 25° С. В третьей реакции образуется бензофенон (дифенилкетон).
Реакция формилирования — взаимодействие бензола со смесью СО и НСl, протекает при высоком давлении и под действием катализатора, продуктом реакции является бензальдегид:
{\displaystyle {\mathsf {C_{6}H_{6}+CO+HCl{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COH+HCl}}}
{\displaystyle {\mathsf {C_{6}H_{6}+HNO_{3}{\xrightarrow[{}]{H_{2}SO_{4}}}C_{6}H_{5}NO_{2}+H_{2}O}}}
{\displaystyle {\mathsf {C_{6}H_{6}+H_{2}SO_{4}\rightarrow C_{6}H_{5}SO_{3}H+H_{2}O}}}
{\displaystyle {\mathsf {C_{6}H_{6}+3H_{2}{\xrightarrow[{}]{Ni/Pd,Pt;t}}C_{6}H_{12}}}}
Реакции окисления[править | править код]
Бензол, вследствие своего строения, очень устойчив к окислению, на него не действует, например, раствор перманганата калия. Однако окисление до малеинового ангидрида можно провести при помощи катализатора оксида ванадия V:
Реакция озонолиза. Также бензол подвергается озонолизу, но процесс протекает медленнее, чем с непредельными углеводородами:
Результатом реакции является образование диальдегида — глиоксаля (1,2-этандиаля).
Реакция горения. Горение бензола является предельным случаем окисления. Бензол легко воспламеняется и горит на воздухе сильно коптящим пламенем (содержит до 92% углерода в молекуле):
{\displaystyle {\mathsf {2C_{6}H_{6}+15O_{2}\rightarrow 12CO_{2}+6H_{2}O}}}
Структура[править | править код]
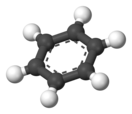
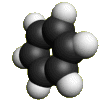
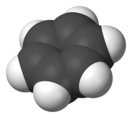
Бензол по составу относится к ненасыщенным углеводородам (гомологический ряд CnH2n−6), но в отличие от углеводородов ряда этилена, C2H4, проявляет свойства, присущие ненасыщенным углеводородам (для них характерны реакции присоединения), только при жёстких условиях, а вот к реакциям замещения бензол более склонен. Такое «поведение» бензола объясняется его особым строением: нахождением атомов в одной плоскости и наличием в структуре сопряжённого 6π-электронного облака. Современное представление об электронной природе связей в бензоле основывается на гипотезе Лайнуса Полинга, который предложил изображать молекулу бензола в виде шестиугольника с вписанной окружностью, подчёркивая тем самым отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла.
В специальной и популярной литературе распространён термин бензольное кольцо, относящийся, как правило, к углеродной структуре бензола без учёта иных атомов и групп, связанных с атомами углерода. Бензольное кольцо входит в состав множества различных соединений.