
Бейметалдардың периодтық жүйедегі орны,
оларлың қасиеттері мен табиғатта таралуы

Сабақтың мақсаты :
1.Бейметалдар периодтық жүйедегі орны
және электрондық құрылысы, физикалық қасиеттері,
бейметалдар және олардың
қосылыстарының Қазақстанның аймақтарында таралуы
туралы білімдерін бекіту .
2. Бейметалдарды алу әдістері туралы білімдерін тереңдету.Элемент,жай және күрделі заттар туралы білімдерін кеңейту.
3. Оқушылардың ғылыми дүниетанымын қалыптастыру .

Сабақтың барысы :
І. Ұйымдастыру кезеңі
а)Сыныпты топқа бөлу
В) Үй тапсырмасын сұрау
Қораптағы сұрақтар .

Ой толғау
Ережесі:
-бірінші қатарға бір сөзбен тақырып жазылады(зат есім)
-екінші қатарға тақырыпты екі сөзбен келтіруі (екі сын есім)
-үшінші қатарға үш сөзбен осы тақырып бойынша іс-әрекет жазылады (етістік)
-төртінші қатарға төрт сөзден тұратын осы тақырыпқа қатысты сөйлем немесе сөз тіркесі жазылады
Мысалы: Күкірт
Сары,ұнтақ
Ерімейді,жанады,әрекеттеседі
Тұздары,қышқылдары, оксидттері болады.

Топтық тергеу әдісі бойынша мәтінді қорғайды
Баяндамашы - мәтінді мазмұндап айтады
Сұрақ қоюшы- мәтінге байланысты сұрақ қояды
Сілтеме табушы- мәтіннің ішіндегі термин және түйін сөздерді табады
Дәнекерлеуші – оқып отырған мәтінді өмірмен байланыстырады
Бейнелеуші, суреттеуші- осы тақырып аясында реакция теңдеулерін жазады.
І топ:
Бейметалдардың
периодтық жүйедегі орны,
оларлың қасиеттері
ІІ топ:
Табиғатта таралуы
және қолданылуы

Бейметалдарды ң валенттілігі мен тотығу дәрежесі
Толықтырған
энергетикалық
деңгейдің
нөмірі
I
IV-VII топтағы
бейметалдардың валенттіліктері мен
тотығу дәрежелері
II
C
III
Si
IV
II
Ge
+4
-4
+2
IV
II
N
+4
-4
IV
II
V
III
+4
-4
P
As
V
III
+5
-3
O
V
III
+5
-3
S
II
+5
-3
VI
IV
II
+2
-2
Se
+6
+4
-2
VI
II
+6
-2
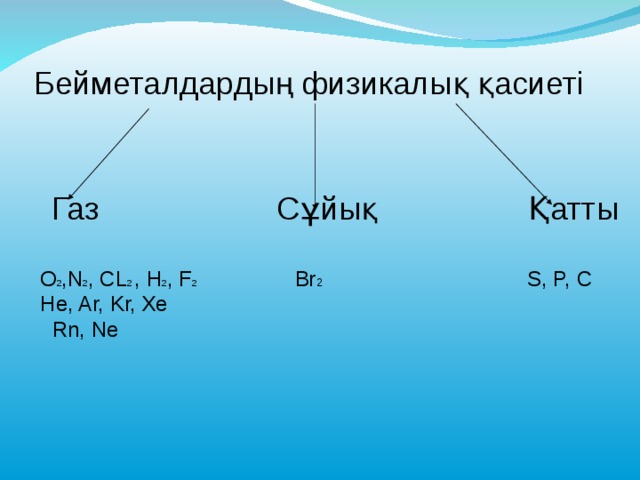
Бейметалдардың физикалық қасиеті
Газ С ұ йық Қатты
O 2 ,N 2 , CL 2 , H 2 , F 2 Br 2 S, P, C
He, Ar, Kr, Xe
Rn, Ne

Бейметалдардың алынуы
2Ca(PO4)2+10C+6SiO2=6CaSiO3+P4+10CO
2HgO=2Hg+O2
2KMnO4=K2MnO2+MnO2+O2
2NaI+Cl2=I2+2NaCl
MnO2+4HCl=MnCl2+Cl2+2H2O
2NaCl+2H2O=H2+Cl+2NaOH
SiO2+C=Si+CO2
SiO2+2Mg=Si+2MgO
NH4+NO2=N2+2H2O
NaNO3+NH4Cl=N2+NaCl+2H2O
3SiO2+4Al=3Si+2Al2O3
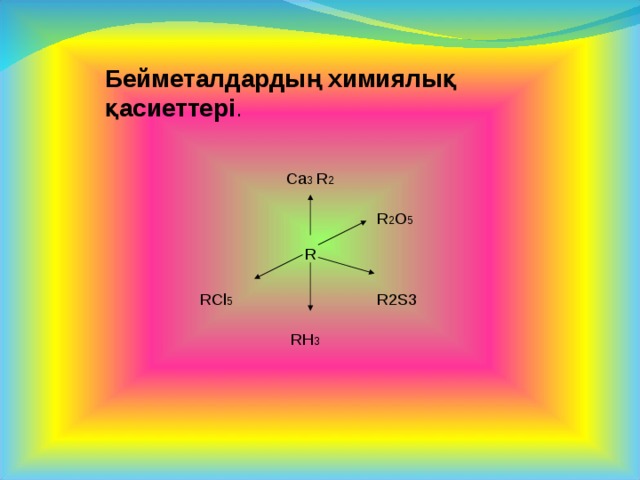
Бейметалдардың химиялық қасиеттері .
Ca 3 R 2
R 2 O 5
R
RCl 5
R2S3
RH 3
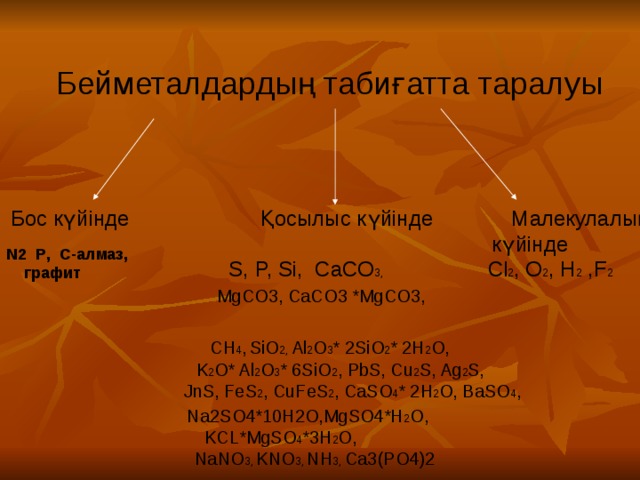
Бейметалдардың табиғатта таралуы
Бос күйінде Қосылыс күйінде Малекулалық
күйінде
S, P, Si, CaCO 3, Cl 2 , O 2 , H 2 ,F 2
MgCO3, CaCO3 *MgCO3,
CH 4 , SiO 2, Al 2 O 3 * 2SiO 2 * 2H 2 O,
K 2 O* Al 2 O 3 * 6SiO 2 , PbS, Cu 2 S, Ag 2 S,
JnS, FeS 2 , CuFeS 2 , CaSO 4 * 2H 2 O, BaSO 4 ,
Na2SO4*10H2O,MgSO4*H 2 O ,
KCL*MgSO 4 *3H 2 O ,
NaNO 3 , KNO 3 , NH 3 , Ca3 ( PO4 ) 2
N2 P , C- алмаз,
графит
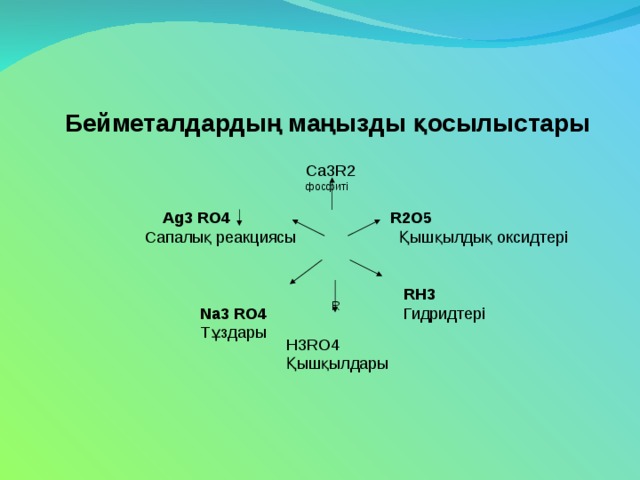
Бейметалдардың маңызды қосылыстары
Ca3R2 фосфиті
R
Ag3 RO4 R2O5
Сапалық реакциясы Қышқылдық оксидтері
RH3
Гидридтері
Na3 RO4
Тұздары
H3RO4
Қышқылдары
Қолданылуы
N P S Si Cl
J
O
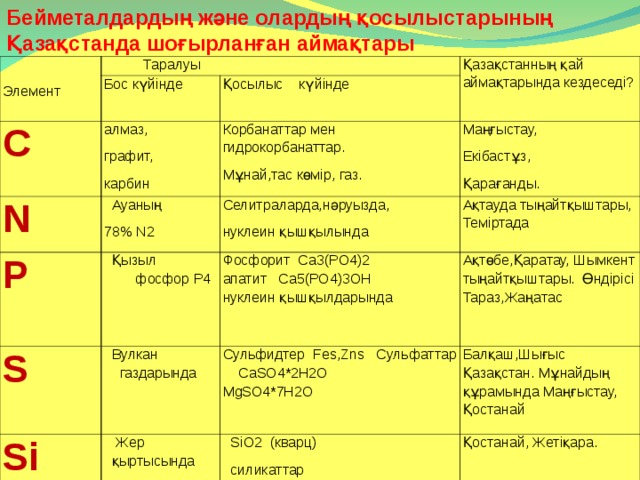
Бейметалдардың және олардың қосылыстарының Қазақстанда шоғырланған аймақтары
Элемент
Таралуы
C
Бос күйінде
Қазақстанның қай аймақтарында кездеседі ?
N
Қосылыс күйінде
алмаз,
графит,
карбин
P
Ауаның
78 % N2
Корбанаттар мен гидрокорбанаттар.
Мұнай,тас көмір, газ.
Селитраларда,нәруызда,
нуклеин қышқылында
Маңғыстау,
Екібастұз,
Қарағанды.
S
Қызыл фосфор Р4
Ақтауда тыңайтқыштары, Теміртада
Фосфорит Ca3(PO4)2 апатит Ca5(PO4)3OH нуклеин қышқылдарында
Вулкан газдарында
Si
Ақтөбе,Қаратау, Шымкент тыңайтқыштары. Өндірісі Тараз,Жаңатас
Сульфидтер Fes,Zns Сульфаттар CaSO4*2H2O MgSO4*7H2O
Жер қыртысында
Балқаш,Шығыс Қазақстан. Мұнайдың құрамында Маңғыстау, Қостанай
SiO2 ( кварц )
силикаттар
Қостанай, Жетіқара.

Бейметалдардың биохимиялық ролі
С - көміртек тірі организмдер үшін ең басты органоген. Бірақ күйе түріндегі
көміртек және оның монооксиді СО адам үшін зиянды. Ұзақ уақыт күйемен
Немесе көмір шаңымен жұмыс істегенде қатерлі тері ісігін тудырады.
Көміртек монооксиді СО өте улы. СО-ның уландырғыш әсері, ол қанның
Гемоглобиніне жеңілқосылып, оны оттекті өкпеден ұлпаларға тасымалдауға
Қабілетсіз етеді. СО – мен уланғанда антидот ретінде карбоген деп аталатын 3-5 %
- ті СО2 мен О2 –нің қоспасы қолданылады. Бұл қоспадағы О2 –нің жоғары қысымы
Ұлпадан СО-ны ығыстырады, ал СО2 -нің қанды қышқылдандыру, сондай –ақ
СО2 СО-ның ығыстырады. Карбонаттары СаСО3, NaHCO3 медициналық
Препараттардың антиацидтік /қышқылға қарсы/ әсері бар және асқазан сөлінің
Қышқылдығын төмендету үшін қолданылады.
Si - кремний қоспа элемент деп аталады. Оның адам организміндегі мөлшері өте аз
Және 10-3 –тін құрайды. Кремнийдің бауырда, бүйректе, шашта және көздің
Қарашығында болатыны анықталған.

Бекіту
« Айқыштар мен нөлдер» ойыны
1.Металдарды –айқышпен бейнелеңіз
Бейметалдарды -нөлдермен бейнелеңіз
1- топ 2-топ
Be
N
Al
Cl
Na
Si
Mg
C
Ge
In
Ce
Be
Si
Al
Mg
S
Ca
Na
2.

Есептер шығару.
І топ
Массасы 3,42 грамм сілтілік металл сумен әрекеттескенде (қ.ж.) 0,448л сутегі бөлінді.Бұл қандай металл ?
ІІ топ
3.Массасы 13,7 грамм металл заряды +2-ге тең катион түзіп сумен реакцияласқанда қалыпты жағдайда 2,24л газ бөлінеді.Бұл қандай металл?

Үйге тапсырма . 4.5 оқу
Мына өзгерістерді жүзеге асыруға болатын реакция теңдеулерін жазыңдар:


































