Просмотр содержимого документа
«Белки и аминокислоты.»

АМИНОКИСЛОТЫ. БЕЛКИ.

Аминокислоты -
это органические соединения, в состав которых входят две функциональные группы: карбоксильная –COOH и аминогруппа – NH 2 .
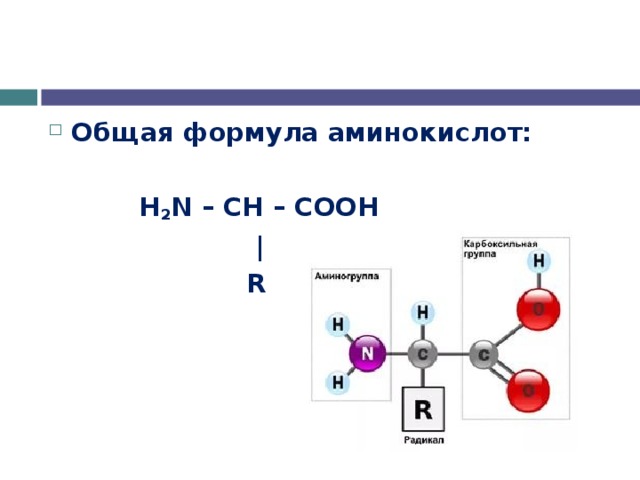
- Общая формула аминокислот:
H 2 N – CH – COOH
|
R
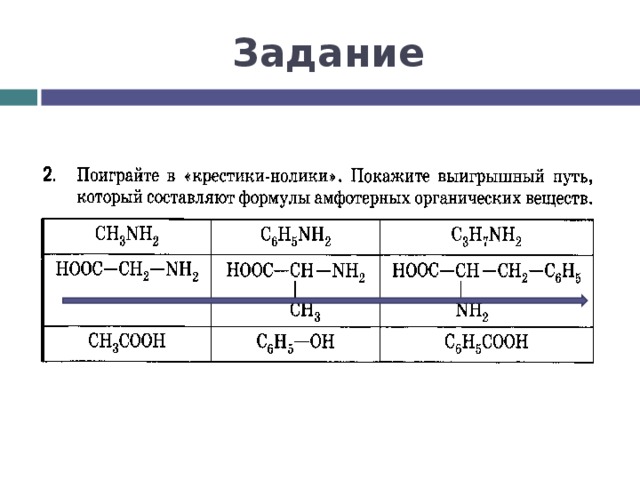
Задание
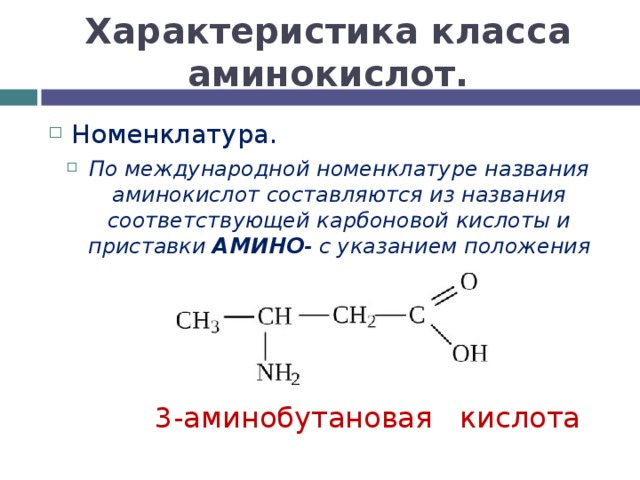
Характеристика класса аминокислот.
- Номенклатура.
- По международной номенклатуре названия аминокислот составляются из названия соответствующей карбоновой кислоты и приставки АМИНО - с указанием положения аминогруппы:
3-аминобутановая кислота
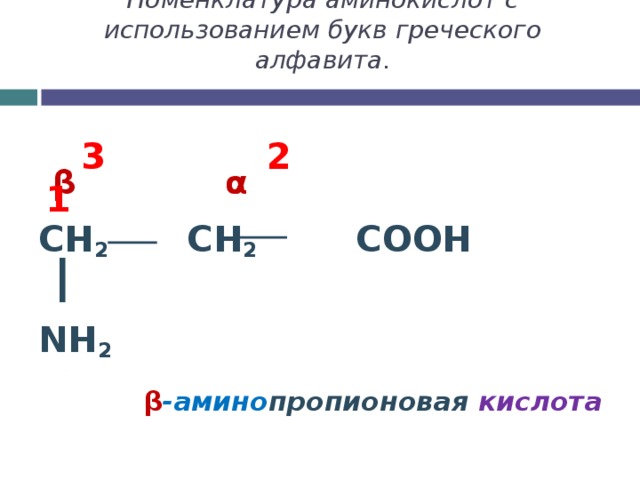
Номенклатура аминокислот с использованием букв греческого алфавита.
CH 2 CH 2 COOH
NH 2
β α
β -амино пропионовая кислота
3 2 1
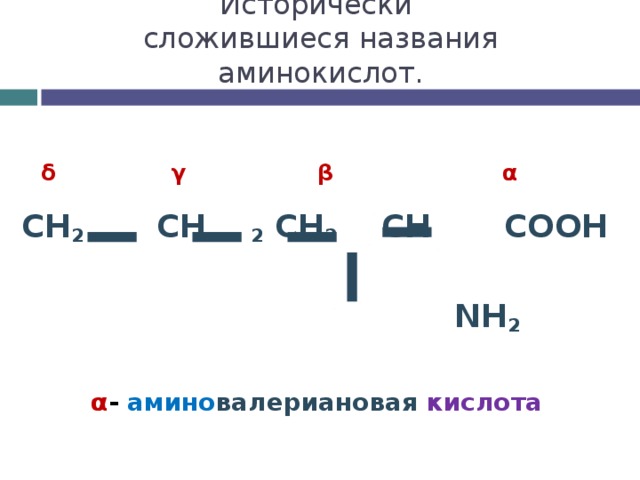
Исторически сложившиеся названия аминокислот.
CH 2 CH 2 CH 2 CH COOH
NH 2
δ γ β α
α - амино валериановая кислота
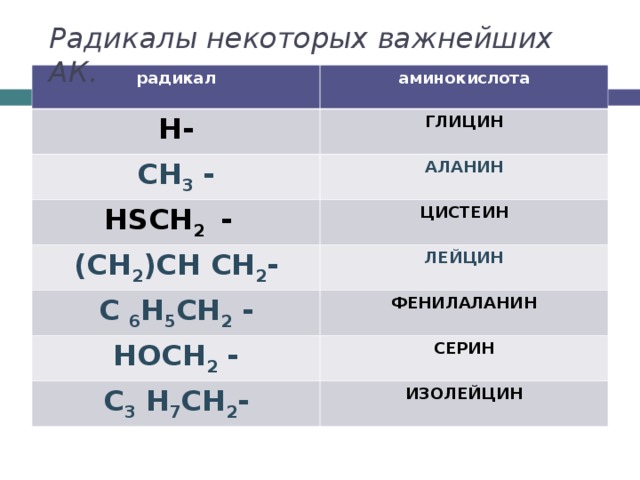
Радикалы некоторых важнейших АК.
радикал
аминокислота
Н-
ГЛИЦИН
СН 3 -
АЛАНИН
Н SCH 2 -
ЦИСТЕИН
(СН 2 )СН СН 2 -
ЛЕЙЦИН
С 6 Н 5 СН 2 -
ФЕНИЛАЛАНИН
НОСН 2 -
СЕРИН
С 3 Н 7 СН 2 -
ИЗОЛЕЙЦИН

Характеристика класса аминокислот.
- Физические свойства.
- Твёрдые кристаллические вещества;
- Хорошо растворяются в воде;
- Имеют достаточно высокие температуры плавления;
- В зависимости от радикала могут иметь сладкий, горький или соленый вкус
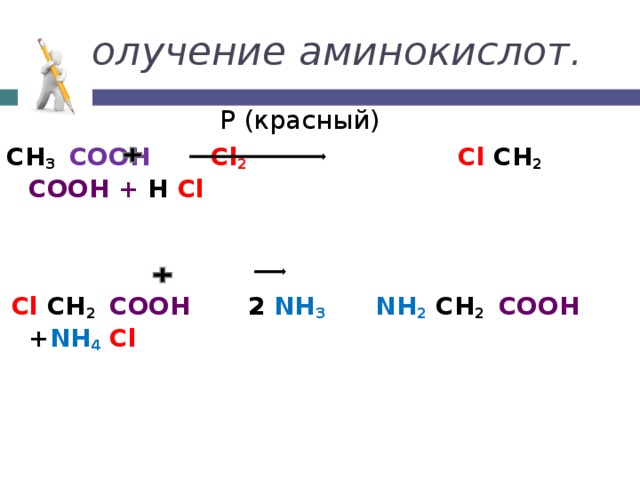
Получение аминокислот.
P (красный)
СН 3 СООН С l 2 С l СН 2 СООН + Н С l
С l СН 2 СООН 2 N Н 3 N Н 2 СН 2 СООН + N Н 4 С l

Реакции АК, как оснований
Взаимодействуют с кислотами.
глицин(аминоуксусная кислота)
хлорид глициния
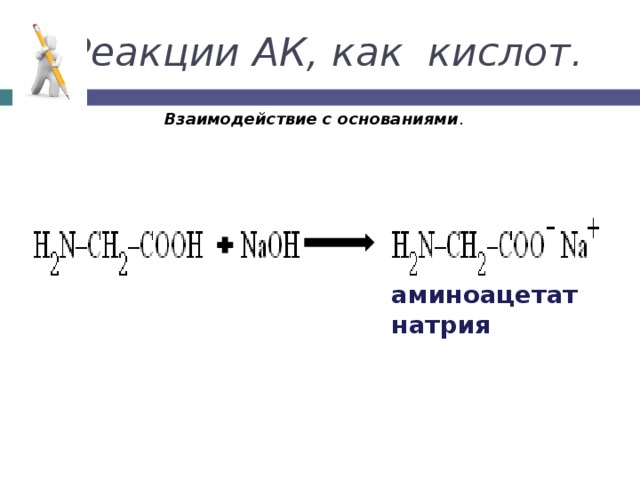
Реакции АК, как кислот.
Взаимодействие с основаниями .
аминоацетат натрия
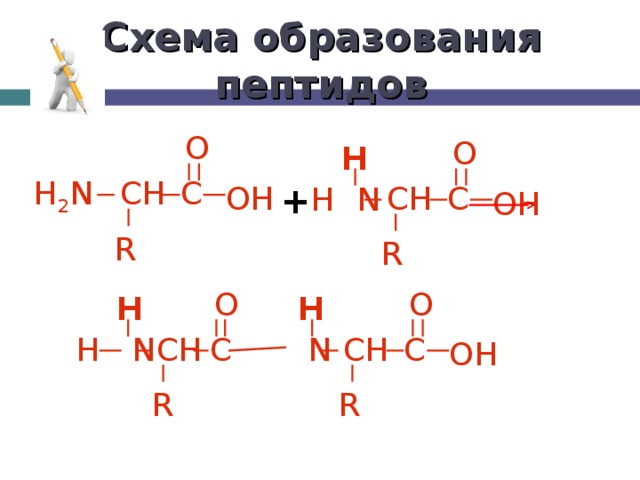
Схема образования пептидов
O
O
H
C
H 2 N
CH
CH
C
+
OH
H
N
OH
R
R
O
O
H
H
C
H
N
CH
C
N
CH
OH
R
R
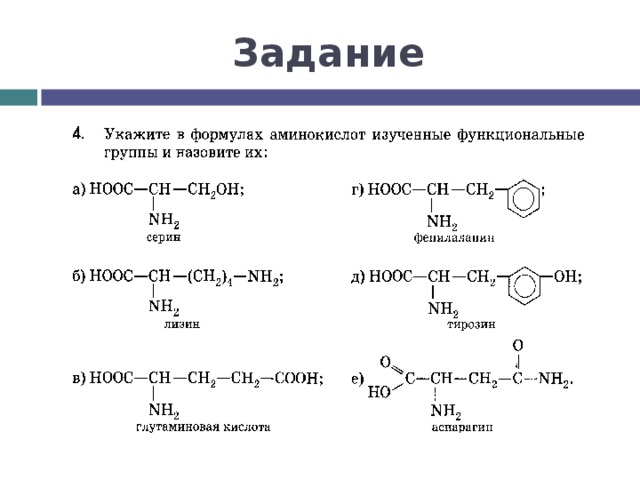
Задание

Горение аминокислот.
4NH 2 CH 2 COOH + 13O 2 8CO 2 + 10H 2 O + 2N 2

Этерификация
NH 2 CH 2 COOH + C 2 H 5 OH NH 2 CH 2 COOC 2 H 5 + H 2 O
H 2 SO 4 ( к)

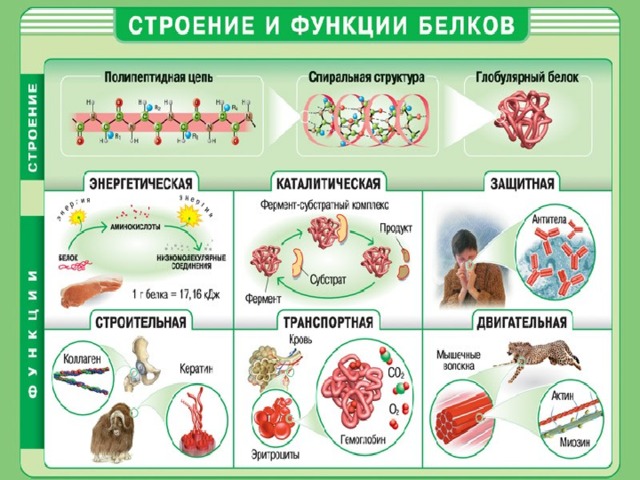
Белки.

- Белки (полипептиды) биополимеры, построенные из остатков -аминокислот , соединенных пептидными связями.
Макромолекулы белков имеют строго упорядоченное химическое и
пространственное строение, исключительно важное для проявления ими определенных биологических свойств
Выделяют 4 уровня структурной организации белков:
- первичная
- вторичная
- третичная
- четвертичная
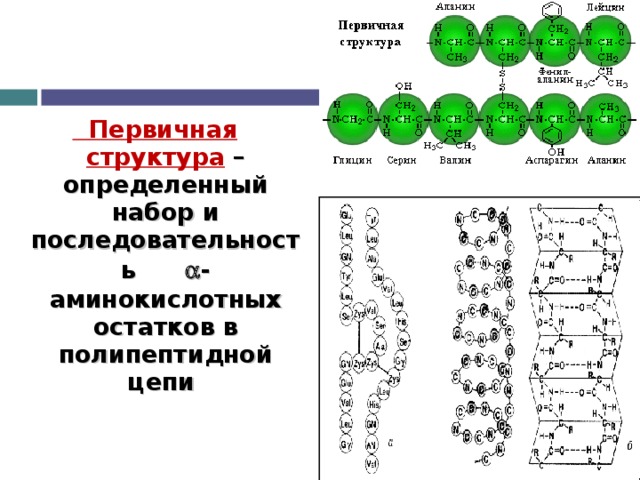
Первичная структура – определенный набор и последовательность -аминокислотных остатков в полипептидной цепи
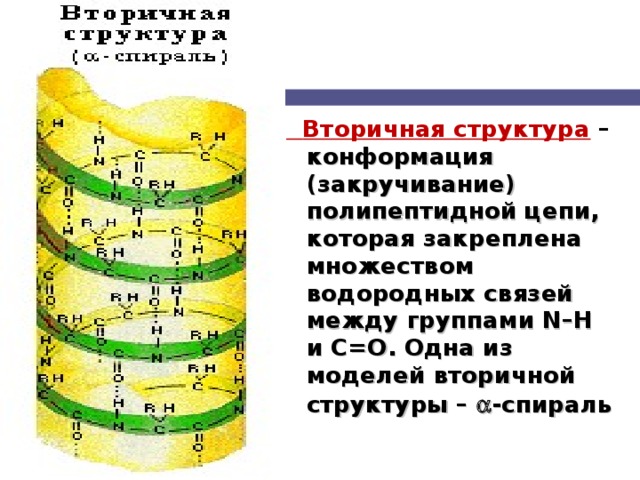
Вторичная структура – конформация (закручивание) полипептидной цепи, которая закреплена множеством водородных связей между группами N–H и С=О. Одна из моделей вторичной структуры – -спираль

Третичная структура
форма закрученной спирали в пространстве, образованная главным образом за счет дисульфидных мостиков -S-S-, водородных связей, гидрофобных и ионных взаимодействий

Четвертичная структура
агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей
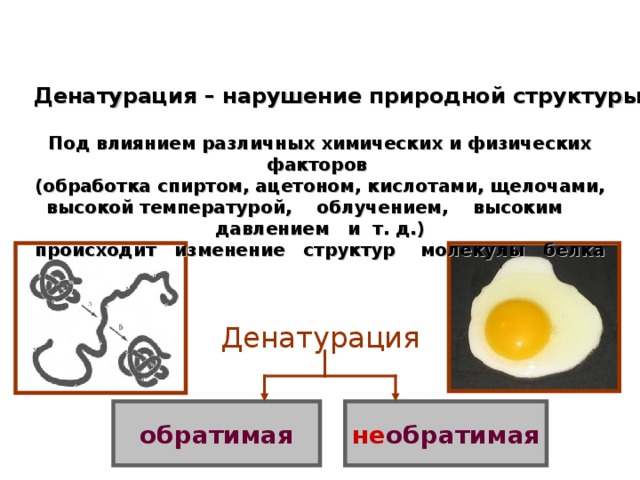
Денатурация – нарушение природной структуры белка.
Под влиянием различных химических и физических факторов
(обработка спиртом, ацетоном, кислотами, щелочами, высокой температурой, облучением, высоким давлением и т. д.)
происходит изменение структур молекулы белка
Денатурация
не обратимая
обратимая

Гидролиз белков
Белки аминокислоты
поликонденсация

Качественные реакции на белки
- Ксантопротеиновая реакция – действие на белки концентрированной азотной кислотой (белый осадок, при нагревании желтеет, при добавлении NH 4 OH становится оранжевым )
- Биуретовая реакция – действие на белки свежеприготовленного раствора гидроксида меди (II) в щелочной среде (фиолетовое окрашивание)
- Качественное определение серы в белках (при нагревании – характерный запах «жженого рога»)






















































