
Презентация по химии
на тему:
«Белки –
природные
полимеры»

БЕЛКИ — это азотсодержащие высокомолекулярные органические вещества со сложным составом и строением молекул.
Белок можно рассматривать как сложный полимер аминокислот.
Белки входят в состав всех живых организмов, но особо важную роль они играют в животных организмах, которые состоят из тех или иных форм белков (мышцы, покровные ткани, внутренние органы, хрящи, кровь).
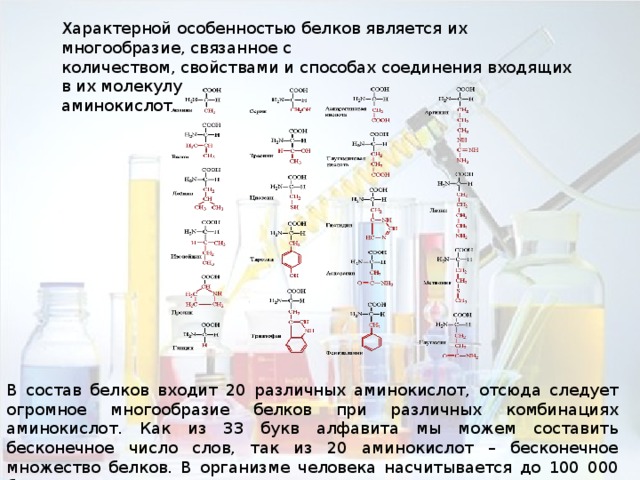
Характерной особенностью белков является их многообразие, связанное с
количеством, свойствами и способах соединения входящих в их молекулу
аминокислот.
В состав белков входит 20 различных аминокислот, отсюда следует огромное многообразие белков при различных комбинациях аминокислот. Как из 33 букв алфавита мы можем составить бесконечное число слов, так из 20 аминокислот – бесконечное множество белков. В организме человека насчитывается до 100 000 белков.

Растения синтезируют белки из углекислого газа СО2 и воды Н2О за счет фотосинтеза, усваивая остальные элементы белков (азот N, фосфор Р, серу S, железо Fe, магний Mg) из растворимых солей, находящихся в почве.
Животные организмы в основном получают готовые аминокислоты с пищей и на их
базе строят белки своей организма. Ряд аминокислот (заменимые аминокислоты)
могут синтезироваться непосредственно животными организмами.

Строение белков
Белки представляют собой нерегулярные полимеры, построенные из остатков аминокислот.
Остатки аминокислот в белках соединены амидной связью между амино- и карбоксильными группами. Связь между двумя аминокислотными остатками обычно называется пептидной связью, а полимеры, построенные из остатков аминокислот, соединенных пептидными связями, называют полипептидами.
Таким образом, белок представляет собой полипептид, содержащий сотни или
тысячи аминокислотных звеньев.
Белок как биологически значимая структура может представлять собой как один полипептид, так и несколько полипептидов, образующих в результате
нековалентных взаимодействий единый комплекс.

Немного из истории..
Историческая справка.
Первая гипотеза о строении молекулы белка была предложена в 70-х годах XIX в. Это была уреидная теория строения белка. В 1903 г. немецкий ученый Э.Г.Фишер предложил пептидную теорию, которая стала ключом к тайне строения белка. Фишер предположил, что белки представляют собой полимеры из остатков аминокислот, соединенных пептидной связью NH–CO.
Идея о том, что белки – это полимерные образования, высказывалась еще в 1888 г. русским ученым А.Я.Данилевским. Согласно полипептидной теории белки имеют определенную структуру. В клетке находятся свободные аминокислоты, составляющие аминокислотный фонд, за счет которого происходит синтез новых белков. Этот фонд пополняется аминокислотами, постоянно поступающими в клетку вследствие расщепления белков пищи пищеварительными ферментами или собственных запасных белков.
Э.Г.Фишер
А. Я. Данилевский

Классификация
Белки подразделяют на протеины (простые белки) и протеиды (сложные белки)

Функции белков
Функции белков.
Белки:
• защищают организм от микробов и вирусов, участвуя в выработке антител;
• регулируют энергобаланс, особенно при больших нагрузках или при дефиците в пище жиров и углеводов.
• обеспечивают рост, размножение и полноценное развитие организма, особенно нервной системы, регулируя раздражимость и реакции на внешние раздражители;
• входят в состав гормонов, мышц и других тканей;
• в связи с витаминами и микроэлементами являются биологическими катализаторами — ферментами;
• формируют способность высшей формы движения материи — мышление;

Элементный состав
белков
Элементный состав белков
Белки содержат в среднем около 1 6% азота, 50-55% углерода , 21-
23% кислорода , 6-7% водорода , 0,3-2,5% серы .
В составе отдельных белков обнаружены также фосфор, йод, железо, медь и некоторые другие макро- и микроэлементы, в различных, часто очень малых количествах.
Содержание основных химических элементов в белках может различаться,
за исключением азота, концентрация которого характеризуется наибольшим
постоянством.

Структура белков
Особый характер белка каждого вида связан не только с длиной, составом и строением входящих в его молекулу полипептидных цепей, но и с тем, как эти цепи ориентируются.
В структуре любого белка существует несколько степеней организации:
Первичная структура белков
1 . Первичная структура белка — специфическая последовательность аминокислот в полипептидной цепи.
Даже одинаковые по длине и аминокислотному составу пептиды могут быть разными веществами потому, что последовательность аминокислот в цепи у них разная.
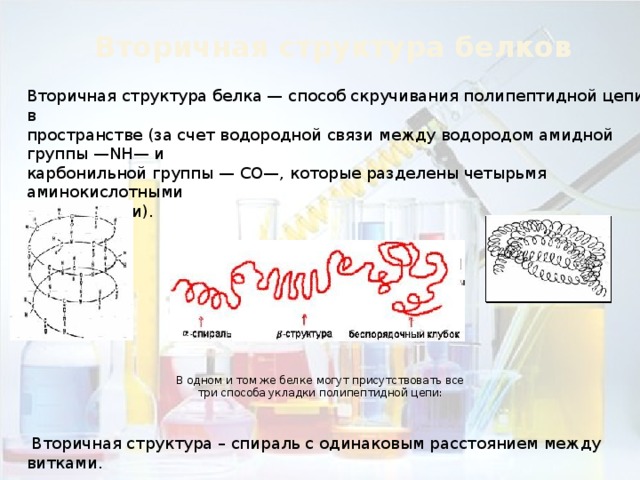
Вторичная структура белков
Вторичная структура белка — способ скручивания полипептидной цепи в
пространстве (за счет водородной связи между водородом амидной группы —NH— и
карбонильной группы — СО—, которые разделены четырьмя аминокислотными
фрагментами).
В одном и том же белке могут присутствовать все три способа укладки полипептидной цепи:
Вторичная структура – спираль с одинаковым расстоянием между витками.

Третичная структура белков
Третичная структура белка — реальная трехмерная конфигурация закрученной спирали полипептидной цепи в пространстве (спираль, скрученная в спираль).
Третичная структура белка обуславливает специфическую биологическую активность белковой молекулы. Третичная структура белка поддерживается за счет взаимодействия различных функциональных групп полипептидной цепи:
· дисульфидный мостик (-S-S-) между атомами серы,
· сложноэфирный мостик – между карбоксильной группой (-СО-) и
гидроксильной (-ОН),
· солевой мостик - между карбоксильной (-СО-) и аминогруппами (NH2).
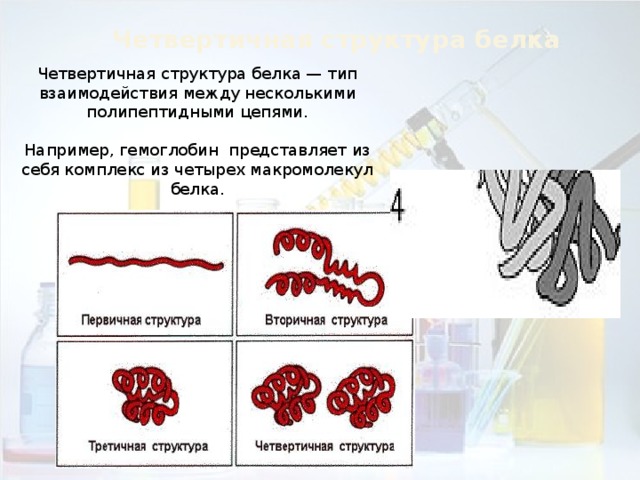
Четвертичная структура белка
Четвертичная структура белка — тип взаимодействия между несколькими
полипептидными цепями.
Например, гемоглобин представляет из себя комплекс из четырех макромолекул
белка.

Физические свойства
Белки имеют большую молекулярную массу ( 104—107),
многие белки растворимы в воде, но образуют, как правило, коллоидные растворы, из которых выпадают при увеличении концентрации неорганических солей, добавлении солей тяжелых металлов, органических растворителей или при нагревании
Белки способны к набуханию, характеризуются оптической активностью и подвижностью в электрическом поле, некоторые растворимы в воде. Белки имеют изоэлектрическую точку.

Химические свойства
Важнейшим свойством белков является их способность проявлять как
кислотные, так и основные свойства, то есть выступать в роли амфотерных
электролитов.

Свойство а мфотерности лежит в основе буферных свойств белков и их
участии в регуляции рН крови.

Химические свойства
2. Качественные реакции на белок:
биуретовая реакция: фиолетовое окрашивание при обработке солями меди в щелочной среде (дают все белки),
ксантопротеиновая реакция: желтое окрашивание при действии
концентрированной азотной кислоты, переходящее в оранжевое под действием
аммиака,
выпадение черного осадка (содержащего серу) при добавлении ацетата свинца
(II), гидроксида натрия и нагревании.
- Денатурация — разрушение вторичной и третичной структуры белка.
Необратимая денатурация
белка куриного яйца под воздействием высокой температуры
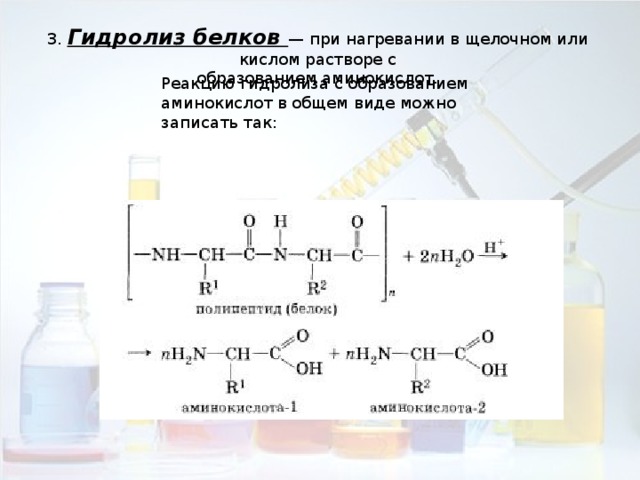
3. Гидролиз белков — при нагревании в щелочном или кислом растворе с
образованием аминокислот.
Реакцию гидролиза с образованием аминокислот в общем виде можно записать так:

Горение
Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев.

Синтез белков
Изыскивая пути исусственного получения белка, ученые интенсивноиизучают механизм его синтеза в организмах. Ведь здесь он совершается в «мягких» условиях, удивительно четко и с большой скоростью. (Молекула белка в клетке образуется всего за 2—3 с.)
Выяснено, что синтез белков в организме осуществляется с участием других высокомолекулярных
веществ—нуклеиновых кислот.
В настоящее время человек уже глубоко познал механизм биосинтеза белка и приступил к искусственному получению важнейших
белков на основе тех же принципов, которые столь совершенно отработаны в
процессе развития органического мира.

Вывод
В данной работе были рассмотрены химические и физические свойства белков, классификация белков, состав и строение белков, были рассмотрены разнообразные функции белков, а также их значение.
Доказано, что белки - обязательная составная часть всех живых клеток, играют исключительно важную роль в живой природе, являются главным, наиболее ценным и незаменимым компонентом питания. Это связанно с той огромной ролью, которую они играют в процессах развития и жизни человека. Белки являются основой структурных элементов и тканей, поддерживают обмен веществ и энергии, участвуют в процессах роста и размножения, обеспечивают механизмы движений, развитие иммунных реакций, необходимы для функционирования всех органов и систем организма.
"Жизнь - это форма существования белка"

Источники информации





































