№ 12- сабак
I.Сабактын темасы. Карбон кислоталары жана анын туундулары
Карбон кислоталарынын түзүлүшү жана класстары
Курамында функционалдык карбоксил тобу менен байланышкан углеводороддук радикалдардан турган органикалык заттар карбон кислоталары деп аталат.
Карбон кислоталары углеводороддук радикалдын жаратылышына жараша чектүү, чексиз жана ароматикалык карбон кислоталары болуп бөлүнүшөт. Мындан тышкары функционалдык карбоксил тобунун санына жараша бир негиздүү, эки негиздүү жана үч негиздүү деп бөлүнүшөт.
Карбон кислоталарынын функционалдык тобу карбоксилдин түзүлүшү - СООН
Чектүү бир негиздүү карбон кислоталары. Татаал эфирлер
Органикалык кислоталардын айрымдарынын даамдары силерге белгилүү. Мисалы алма кислотасы, лимон кислотасы, сүт кислотасы, уксус кислотасы ж.б.
Ал эми бул теманын чегинде бир негиздүү карбон кислоталарынын айрымдарын гана карайбыз.
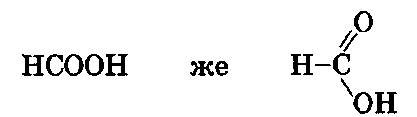
Бул кислота метандык кислота деп да аталат (аны метандан өндүрүлгөн катары да кароого болот).
Альдегиддерди кычкылдандыруунун натыйжасында органикалык кислоталар алынат. Алардын курамында карбоксил тобу бар:
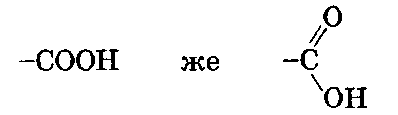
Демек, углеводороддук радикал менен байланышкан карбоксил тобу бар органикалык бирикмелер карбон кислоталары деп аталат, алардын жалпы формуласы:
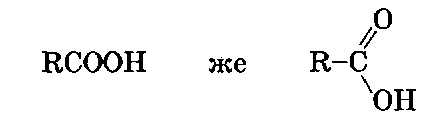
Бул жерде R - углеводороддук радикал. Эгерде кислотанын курамындагы углеводороддук радикал CnH2n+1 болсо, анда ага туура келген кислотанын жалпы формуласын CпH2n+1COOH деп жазууга болот. Мындай жалпы формулага туура келген кислоталар чектүү бир негиздүү кислоталар деп аталышат. Бир негиздүү болгондугунун себеби, алардын курамында бирден карбоксил тобу бар (молекуласында эки же андан көп карбоксил тобун кармап жүргөн органикалык кислоталар да бар).
Чектүү бир негиздүү карбон кислоталарынын гомологиялык катарын кумурска кислотасы баштайт. Анын молекуласында карбоксил тобу радикал менен байланышпастан, суутектин атому менен байланышкан:
Карбон кислоталарынын гомологдору, изомерлери жана номенклатурасы
Карбон кислоталарын углеводороддордун туундулары катарында эл аралык систематикалык номенклатура боюнча атоо углеводороддун санына карата номерленүүчү карбоксил тобундагы көмүртектен баштап номерлеп, биринчи радикал жайгашкан көмүртектин сандары жазылып аягында -ан мүчөсүн улап кислотасы деген сөз кошулуп айтылат.
4 3 2 1
Н 3С – СН – СН2 – СООН 3- метилбутан кислотасы
|
СН3
Карбон кислоталарынын ичинде изомерлер байкалат. Мисалы, СН3 –СООН уксус кислотасы жана НООС – СН3 кумурска кислотасынын метил эфири деп кароого болот.
Карбон кислоталарындагы электрондордун тыгыздыгы терс электрлүүлүгү күчтүү болгон кычкылтектин атомуна жылышкандыктан көмүртектин атому бир аз оӊ зариядка ээ болот. Натыйжада көмүртектин атому –ОН тобундагы электрондун тыгыздыгын өзүнө тартат, ошондуктан – ОН тобундагы суутектин атомдору кыймылдуу болуп, кислоталык касиетке ээ болуп суудагы эритмеси иондорго диссоциацияланат.
 R – COOH R-COO - + H+
R – COOH R-COO - + H+
Функционалдык карбоксил тобунун өзгөчө жагы кислоталык касиети бар экенин көрсөтөт.
Карбон кислоталарынын табигый булактары.
Карбон кислоталарынын айырм өкүлдөрү, мисалы- кумурска кислотасы кумурскаларда, чалканда, ийне жалбырактуу өсүмдүктөрдүн ийне жалбырактарында;
НООС-СООН козукулак кислотасы- козукулак өсүмдүктөрүнүн жалбырактарында;
СН3 – (СН2 )3 – СООН валериан кислотасы- валериан өсүмдүктөрүнүн тамырында
СН3 – (СН 2 )4 – СООН капрон кисотасы – эчкинин майында;
СН3 – (СН 2 )14 – СООН пальмитин кислотасы пальма өсүмдүктөрдүн майында.
Бир негиздүү жана эки негиздүү карбон кислоталарынын гомологиялык катарлары жана маанилүү өкүлдөрү.
Таблица 7.
| Чектүү, каныккан кислоталар | Чексиз,каныкпаган Карбон кислоталары | Ароматикалык кислоталар | Эки негиздүү кислоталар |
| 1.Н- СООН кумурска (метан) кислотасы | СН2 = СН-СООН пропен же акрил кислотасы | С 6Н5 – СООН Бензой кислотасы | НООС-СООН козукулак кислотасы |
| 2.СН3 –СООН уксус же этан кислотасы | СН2 = С – СООН | СН3 метакрил кислотасы | Н3С– С 6Н5 – СООН П-толуил кислотасы | НООС-СН2 –СООН Мпропандион же малон кислотасы |
| 3.( СН3)2 –СН-СООН Изобутан кислотасы | СН3–СН=СН-СООН Бутен-2 же кротон кислотасы | НО-С6Н5–( СООН) Салицил кислотасы
| НООС-С6Н5 – СООН Фтал кислотасы |
3.Карбон кислоталарынын алыныштары
1. Алкандарды каталиттик жол менен кычкылдандыруу.
 2СН4 + 3О2 2НСООН + 2 Н 2О
2СН4 + 3О2 2НСООН + 2 Н 2О
2.Ферменттер же башка катализаторлордун таасири менен спирттерди кычкылдандыруудан алат.
 СН3 - СН 2 ОН + 3О2 СН3 – СООН + 2 Н 2О
СН3 - СН 2 ОН + 3О2 СН3 – СООН + 2 Н 2О
3.Кычкылдангычтардын жардамы менен алдегиддерди кычкылдандыруудан алат.
 СН3 – СНО + О СН3 –СООН уксус кислотасы
СН3 – СНО + О СН3 –СООН уксус кислотасы
4.Кумурска кислотасын көмүртектин (11) оксидинен синтездеп алуу.

 CO + NaOH HCOONa + H2SO4 HCOOH + Na2SO4
CO + NaOH HCOONa + H2SO4 HCOOH + Na2SO4
көмүртектин (11) натрий формияты кумурска кислотасы
оксиди
4.Карбон кислоталарынын касиеттери
Физикалык касиеттери. Массасы женил карбон кислоталары же биринчи мүчөлөрү - сууда жакшы эриген, ачуу жыттуу суюктуктар. Май кислотасынан баштап жогорку түзүлүштөгү карбон кислоталары сууда эрибейт. Массасы оор жогорку карбон кислоталар, пеларгон (нонан) С8Н17 – СООН кислотасынан тартып сууда эрибей турган, жытсыз, катуу заттар болот. Молекулалык массалары өскөн сайын кайноо температурасы жогорулайт. Уксус кислотасы - түссүз мүнөздүү кескин жыттуу суюктук. 160 Сдан төмөнкү температурада музга окшогон кристаллдык массаны пайда кылгандыктан, «муз» кислотасы деп аташат.Сууда эӊ жакшы эрийт. 70 – 80 % эритмеси уксус эссенциясы деген ат менен белгилүү.
Карбон кислоталары химиялык касиеттери
Карбон кислоталарынын химиялык касиеттери, молекуласындагы карбоксил тобунун касиеттери менен аныкталынат. Карбон кислоталары минералдык кислоталар сыяктуу суудагы эритмелериинде диссоциацияланат, суутек иону бөлүнүп чыгат. Ошондуктан алар кычкыл чөйрөнү көрсөтүп, кислоталык касиетке ээ болушат.
Кумурска кислотасы күчтүү кислота, бирок начар электролит, кескин жыттуу, түссүз суюктук, 1010 С да кайнайт.Терини күйгүзөт.
Кумурска кислотасы түзүлүшү боюнча алып караганда альдегидке жана карбон кислотасына дагы окшош болот. Ошондуктан эки түрдүү касиет мүнөздүү.
Альдегид катарында НСООН калыбына келтиргич касиетке ээ.

НСООН + Ag2O 2Ag ! + CO2 + Н 2О
2.Кумурска кислотасы сууну сиӊирип алуучу заттардын таасири астында
(РС15, H2SO4, катализаторлор) СО –пайда кылып сууну бөлүп чыгарат.
H2SO4, кат.
 НСООН СО + Н 2О
НСООН СО + Н 2О
Кумурска ксслотасы көмүртектин (11) оксиди
3.Уксус кислотасы минералдык кислоталар сыяктуу электр тогун начар өткөрүшөт, кычкыл дамы бар, эритмеси иондорго диссоциацияланат, начар кислота.

 СН3 – СООН СН3 – СОО- + Н +
СН3 – СООН СН3 – СОО- + Н +
4.Минералдык кислоталар сыяктуу уксус кислотасы активдүү металлдардын, оксиддери, гидроксиддери менен реакцияга кирип туздарды пайда кылат. Уксус кислотасынын туздарын ацетаттар, кумурска кислотасынын туздарын формиаттар деп аталат.
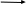 СН3 – СООН + NaOH СН3 – СООNa + Н 2О
СН3 – СООН + NaOH СН3 – СООNa + Н 2О
уксус кислотасынын натрий ацетаты
 2СН3 – СООН + СаО (СН3 –СОО)2 Са + Н2 О Калций ацетаты.
2СН3 – СООН + СаО (СН3 –СОО)2 Са + Н2 О Калций ацетаты.
 СН3 – СООН + NH3 СН3–СООNН4 аммоний ацетаты
СН3 – СООН + NH3 СН3–СООNН4 аммоний ацетаты
t 0 C
 СН3 – СООNН4 СН3 – СООNН2 + Н2О уксус кислотасынын амиди же ацетамид
СН3 – СООNН4 СН3 – СООNН2 + Н2О уксус кислотасынын амиди же ацетамид
5. Карбон кислоталарынын колдонулушу
Жогорку молекулалуу карбон кислоталары көп атомдуу спирттер, глицерин менен аракеттенишкенде майлар алынат. Майлар суюк жана тоң болуп экиге бөлүнөт.
Суюк майлар: күнкарама, зайтун (олива), пахта, кендир, зыгыр майлары. Өсүмдүктөрдөн катуу майлар да алынышы мүмкүн, мисалы, какао майы, кокос майы.
Суюк майларды гидрлөө менен катуу майларды алууга болот. Анткени катуу майлардын техникалык жана тамак-аш продуктусу катары мааниси чоӊ. Катуу майлардан баалуу самындар өндүрүлөт.
Самын - бул майлуу кислоталардын туздары болуп саналат. Натрий самындары көбүрөөк колдонулат. Аларды майларды жегич натрий же соода менен ысытуу аркылуу гидролиздөөдөн алышат. Бул процесс майларды самындантуу деп аталат, натыйжада органикалык кислоталардын туздары пайда болот, майдын курамындагы глицерин бөлүнүп чыгат. Самынды глицеринден бөлүп алуу үчүн аралашмага хлордуу натрийдин эритмеси кошулат. Анткени хлордуу натрий эритмесинде самын өтө начар эрийт, ошондуктан эритменин ылдыйкы бөлүгөндө глицерин жана кайнатма туздун эритмеси, үстүнкү бөлүгүндө алынган самын калат.
Натрий самынынын формуласы RСООNа. Калий самындары RСООК формуласына туура келет. Алар - суюк самындар. Майлар самын өндүрүүдө, тамак-аш катары гана колдонулбастан, май боекторун, глицеринди, косметикалык каражаттарды, курулуш сырларын суюлтууга колдонулуучу олифтерди алууда да пайдаланылат. Азыркы учурда май боекторун өндүрүүдө өсүмдүк майлары эмес, углеводороддук сырье (мунай, газ) колдонулат. Бул сырье кир кетирүүчү каражаттарды өндүрүүдө да кенири керектелип, синтетикалык кир кетирүүчү каражаттар да көп чыгарылууда.
V. Бышыктоо.
1.Органикалык кислоталардын органикалык эмес кислоталардан айырмасы эмнеде? Окшоштугу кайсы?
2.Эмне үчүн айрым органикалык кислоталар карбон кислоталары деп аталышат?
3.Формиаттар жана ацетаттар кантип пайда болот?
4.Татаал эфирлердин пайда болуу реакциясы кандай жүрөт?
5. Эмне үчүн майлар татаал эфирлерге кирет?
6. Карбон кислоталарынын металлдар, негиздик оксиддер, негиздер жана туздар менен болгон реакцияларынын тендемелерин түзүүгө аракет жасагыла.
7. Төмөнкү айланыштар ишке аша турган реакциялардын тендемелерин түзгүлө: этан → этилен → этил спирти → уксус альдегиди→ уксус кислотасы → уксус этил эфири.
8. Суюк майларды кандай жол менен катуу майларга айландырышат? Самын кантип өндүрүлөт?







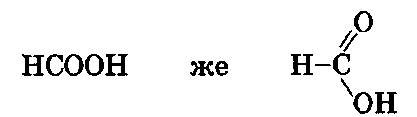
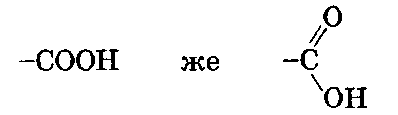
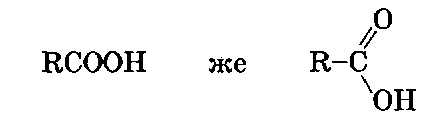
 R – COOH R-COO - + H+
R – COOH R-COO - + H+  2СН4 + 3О2 2НСООН + 2 Н 2О
2СН4 + 3О2 2НСООН + 2 Н 2О СН3 - СН 2 ОН + 3О2 СН3 – СООН + 2 Н 2О
СН3 - СН 2 ОН + 3О2 СН3 – СООН + 2 Н 2О СН3 – СНО + О СН3 –СООН уксус кислотасы
СН3 – СНО + О СН3 –СООН уксус кислотасы
 CO + NaOH HCOONa + H2SO4 HCOOH + Na2SO4
CO + NaOH HCOONa + H2SO4 HCOOH + Na2SO4
 НСООН СО + Н 2О
НСООН СО + Н 2О
 СН3 – СООН + NaOH СН3 – СООNa + Н 2О
СН3 – СООН + NaOH СН3 – СООNa + Н 2О 2СН3 – СООН + СаО (СН3 –СОО)2 Са + Н2 О Калций ацетаты.
2СН3 – СООН + СаО (СН3 –СОО)2 Са + Н2 О Калций ацетаты.









