Просмотр содержимого документа
«Коррозия металлов. Способы защиты»

Коррозия металлов
МБОУ СОШ №60
Трубникова Е.В.

Металлы в наше время:

Металлы в нашей жизни.

Кружевная решетка Летнего сада Санкт-Петербурга

- Уже полтора тысячелетия стоит на одной из площадей Дели железная колонна высотой около 8 метров, диаметром 65 сантиметров, массой 6,5 тонн. И, несмотря на жаркий и влажный климат Индии, не ней нет ни единого ржавого пятнышка.

- Это объясняется тем, что колонна сделана из чистого железа. А чистое железо не ржавеет.
- Сейчас лишь немногие крупнейшие металлургические лаборатории мира могут получить граммы железа такой чистоты.
- Как это удалось древним индийским металлургам?!

- Эйфелева башня изготовлена из обычной стали и необратимо ржавеет и разрушается, и только постоянная химиотерапия помогает бороться с этим недугом: Эйфелеву башню красили 18 раз, отчего ее масса (9000 т) каждый раз увеличивалась на 70т

«Ржа – ест железо».
- Мы видим мрачную картину, Вот ржавый гвоздь и ржавая труба, И даже новую машину За год буквально съела ржа. Ползет она как змей ужасный И вглубь, и вширь, и поперек. Корабль, краскою блиставший, С дырой в боку ко дну идет. Ржавеет все – тросы, лебедка, Опоры зданий и мостов, И даже руль подводной лодки Всегда к ржавлению готов. И где же выход из проблемы, И в чем причина бедствий тех? Найдем ответ мы непременно Пусть нам сопутствует успех.
Трубникова Е.В.

Жертвы коррозии:

Коррозия в автомобилях.
- Коррозия металла – это проблема, которой подвержен кузов каждого автомобиля. Факторы влияющие на металл автомобиля – это влага, разные химические элементы (частая мойка авто под давлением с пеной, соль на дорогах зимой и т.п.), отсутствие защиты на подкрылках и другие неприятности, приводят к появлению ржавчины в разных местах кузова автомобиля.
Трубникова Е.В.

Экономический ущерб от коррозии.
- Экономические потери от коррозии металлов огромны. В США по последним данным NACE ущерб от коррозии и затраты на борьбу с ней составили 3,1 % от ВВП (276 млрд долларов). В Германии этот ущерб составил 2,8 % от ВВП. По оценкам специалистов различных стран эти потери в промышленно развитых странах составляют от 2 до 4 % валового национального продукта. При этом потери металла, включающие массу вышедших из строя металлических конструкций, изделий, оборудования, составляют от 10 до 20 % годового производства стали.

Обрушение Серебряного моста.
- Ржавчина является одной из наиболее распространенных причин аварий мостов. Так как ржавчина имеет гораздо больший объём, чем исходная масса железа, её наращивание может привести к неравномерному прилеганию друг к друга конструкционных деталей. 15 декабря 1967 года Серебряный мост, соединяющий Поинт-Плезант, штат Западная Виржиния, и Канауга, штат Огайо, неожиданно рухнул в реку Огайо. В момент обрушения 37 автомобилей двигались по мосту, и 31 из них упали вместе с мостом. Сорок шесть человек погибли, и девять серьезно пострадали. Помимо человеческих жертв и травм, был разрушен основной транспортный путь между Западной Виржинией и Огайо. Причиной обрушения стала коррозия.

- В начале ХХ века из нью-йоркского порта вышла в открытый океан красавица яхта. Её владелец, американский миллионер, не пожалел денег, чтобы удивить свет: корпус яхты был сделан из очень дорогого в то время алюминия, листы которого скреплялись медными заклёпками. Это было так красиво: сверкающий серебристым блеском корабль, усеянный золотистыми головками заклёпок!

- Однако недолго наслаждался владелец новой яхты. Через несколько дней, когда в океане поднялось лёгкое волнение, обшивка корпуса вдруг начала расходиться, и яхта быстро пошла ко дну. Команда едва успела спустить на воду шлюпки, которые… тоже были из алюминия с медью. К счастью, незадачливых мореплавателей подобрало проходившее мимо судно.

Коррозия металлов.
- Коррозия-это самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды
- Виды коррозии (по процессам) :
- Химическая коррозия;
- Электрохимическая коррозия.

Задачи урока.
- Изучить химическую и электрохимическую коррозию как окислительно-восстановительный процесс;
- Рассмотреть бытовые и экономические проблемы, вызываемые коррозией;
- Способы защиты от коррозии.

Химическая коррозия.
- Химическая коррозия протекает в сухих газах(газовая коррозия) при повышенных температурах и не сопровождается возникновением электрического тока. Она происходит по механизму гетерогенной реакции
- 3Fe + 2O₂ = Fe₃O₄
- 2Fe + 3Cl₂ = 2FeCl₃
- 2Fe + 3SO₂ + 3O₂ =Fe₂(SO₄)₃
- 4Fe + 3O 2 → 2Fe 2 O 3

Электрохимическая коррозия
- Электрохимическая коррозия протекает в растворах электролитов(кислоты, основания, соли, морская и речная вода, влажная почва, атмосфера любого влажного газа) и сопровождается возникновением электрического тока. Она протекает по механизму гальванического элемента.
Электрохимическая коррозия происходит в токопроводящей среде (в электролите).

Гальванический элемент

МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ

МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ

МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ

Презентация 1 группы

Презентация 2 группы

N\N пробирки
Условия опыта
№ 1
Железный гвоздь + H 2 О (кипяченая) Гвоздь в воде находится полностью, чтобы не было доступа О 2
№ 2
Наблюдения и вывод
№ 3
Гвоздь наполовину в воде
Процесс коррозии идет очень медленно.
Железный гвоздь обмотанный Zn проволокой в щелочной среде.
Наблюдается коррозия железа(образование осадка бурого цвета) процесс идет быстрее в пробирке №1 т.к. есть доступ кислорода.
№ 4
Наблюдается разрушение Zn как более активного металла, образуется осадок белого цвета.
Железный гвоздь в растворе электролита NaCl
№ 5
№ 6
Железный гвоздь в 10%-м растворе щелочи
Наблюдается более интенсивное разрушение Fe (больше осадка, чем в чистой воде)
Железный гвоздь обмотанный медной проволокой в растворе электролита NaCl
В щелочной среде коррозия не наблюдается
Идет очень сильное разрушение Fe. Здесь на процесс коррозии влияют 2 фактора:
- контакт Fe с менее активным металлом
- 2) среда электролита
Презентация 3 группы
Изучение коррозии железа в
различных электролитах

Презентация 4 группы

Презентация 5 группы

Методы защиты от коррозии
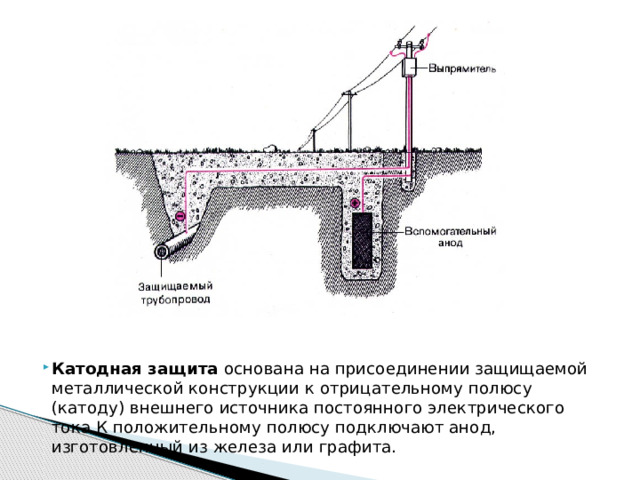
- Катодная защита основана на присоединении защищаемой металлической конструкции к отрицательному полюсу (катоду) внешнего источника постоянного электрического тока К положительному полюсу подключают анод, изготовленный из железа или графита.

- Протекторная защита основана на присоединении к защищаемой металлической конструкции листов (протекторов) из более активного металла. Протектор разрушается, предохраняя защищаемый металл.

Способы защиты от коррозии:
- Покрытия (неметаллические, металлические, химические);
- Анодная защита;
- Катодная защита;
- Протекторная защита;
- Ингибирование.

Как я усвоил материал по теме «Отчего ржавеют металлы»
1 вариант:
2 вариант:
2. а
3. б
2. б
3. а
4. б,в
5. а
4. а,в
5. б
6. б
7. а
6. а
7. в

Урок закончен. Всем спасибо.


















































