

«Отыщи всему начало и ты многое поймешь»
(Козьма Прутков)


Строение атома. Изотопы.

В основе философии Демокрита лежит учение:
Атом есть мельчайшее «неделимое» тело, не подверженное никаким изменениям. Неделимость атома аналогична неделимости «бытия» .
ИСТОРИЧЕСКАЯ СПРАВКА
Демокрит
(460 г – 370 г до н.э.)
Как устроен атом?

Джозеф Джон Томсон (18 декабря 1856- 30 августа 1940) английский физик, лауреат Нобелевской премии по физике 1906 года

Модель атома Томсона
«Пудинг с изюмом»
Джозеф Джон Томсон

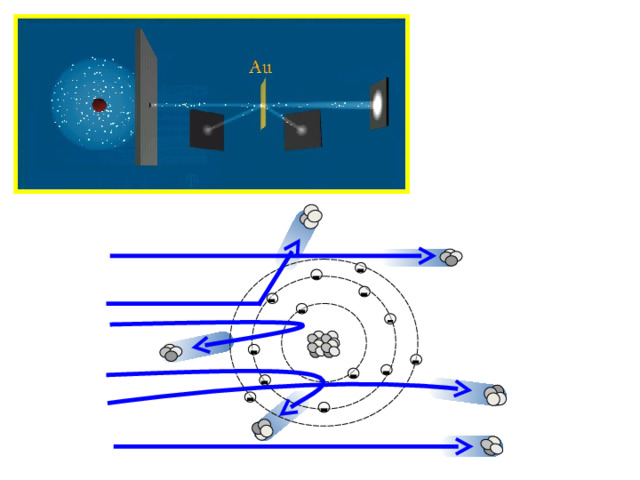
Эрнест Резерфорд (30 августа 1871 г. – 19 октября 1937 г.) Нобелевская премия по химии, 1908 год
-
-
-
-
-
-
-
-
-
-
-
-
-

Планетарная модель атома

В. Брюсов об атоме (1922 г.)
Быть может эти электроны –
Миры, где пять материков,
Искусства, знанья, войны, троны
И память сорока веков!
Еще, быть может, каждый атом – Вселенная, где сто планет;
Там – все, что здесь, в объеме сжатом,
Но также то, чего здесь нет.
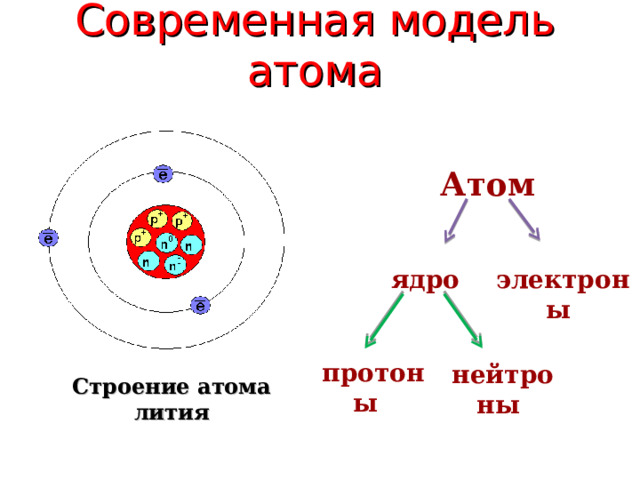
Современная модель атома
Атом
ядро
электроны
протоны
нейтроны
Строение атома лития
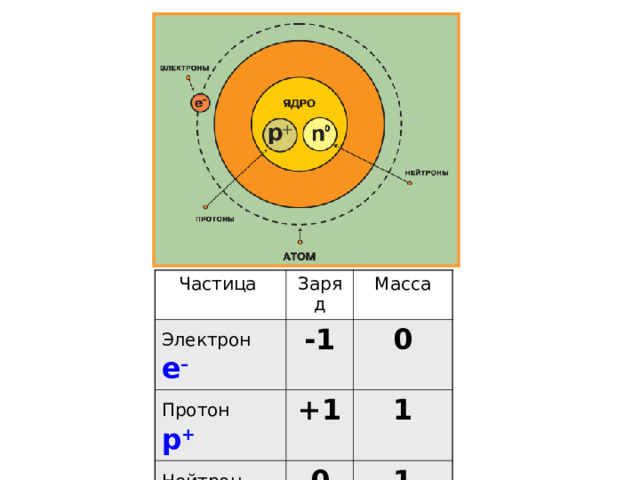
Частица
Электрон е –
Заряд
Масса
-1
Протон р +
0
Нейтрон n 0
+1
1
0
1

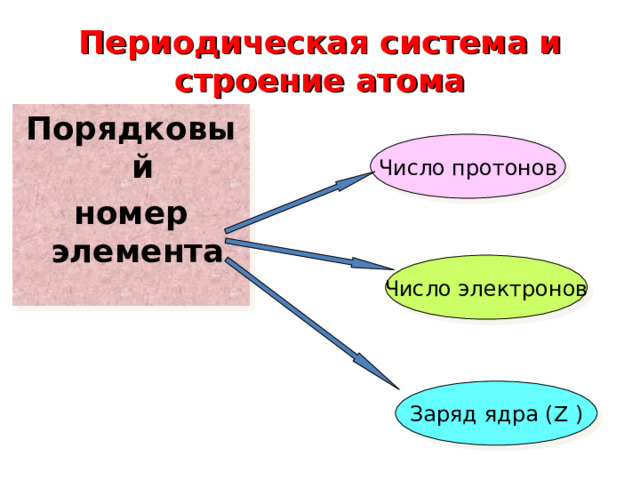
Периодическая система и строение атома
Порядковый
номер элемента
Число протонов
Число электронов
Заряд ядра ( Z )
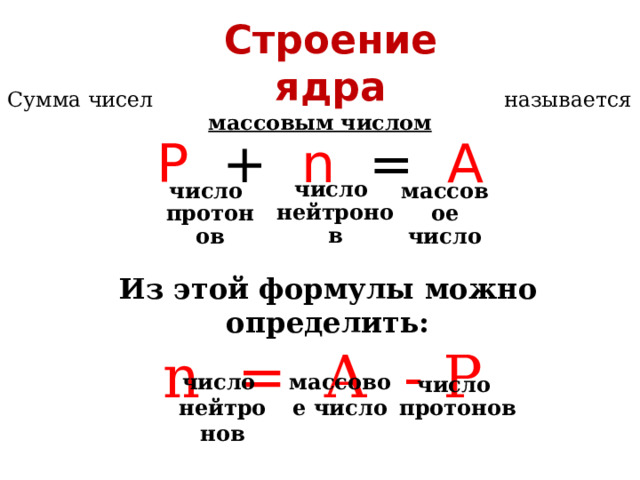
Строение ядра
Сумма чисел протонов и нейтронов в атоме называется
массовым числом
Р + n = A
число нейтронов
число протонов
массовое число
Из этой формулы можно определить:
n = A - Р
число нейтронов
массовое число
число протонов

Заряд ядра ( Z)
Число протонов в ядре ( Р )
Число электронов
(e)
Порядковый номер элемента в ПС
=
=
=
Атом – электронейтральная частица

Алгоритм определения состава атома:
- По ПСХЭ определить порядковый номер химического элемента.
Порядковый номер элемента в ПСХЭ = заряду ядра атома ( Z )
2 . Заряд ядра атома ( Z ) = числу протонов ( P )
3 . Число протонов (Р) = числу электронов (е)
4. Число нейтронов ( n ) = массовое число (А) – заряд ядра ( Z )
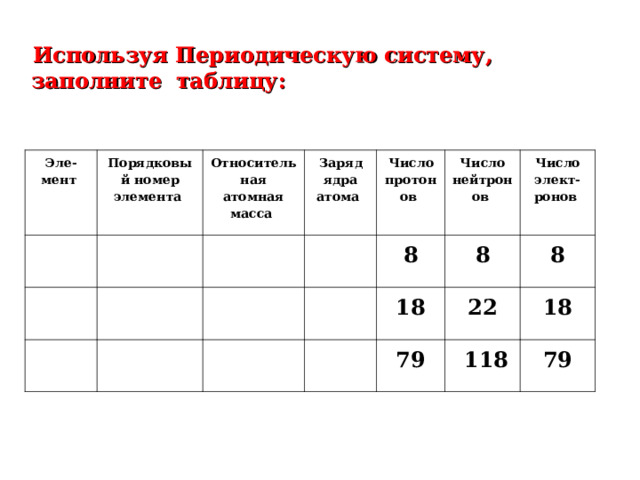
Используя Периодическую систему, заполните таблицу:
Эле-
мент
Порядковый номер элемента
Относительная атомная масса
Заряд ядра атома
Число протонов
Число нейтронов
8
Число элект-ронов
18
8
22
8
79
18
118
79
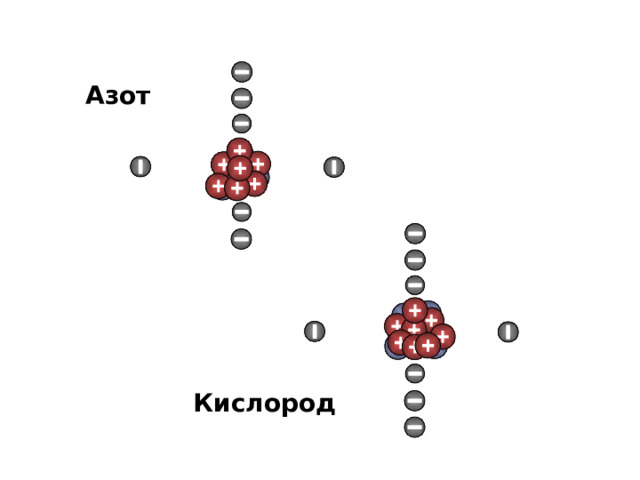
Азот
Кислород
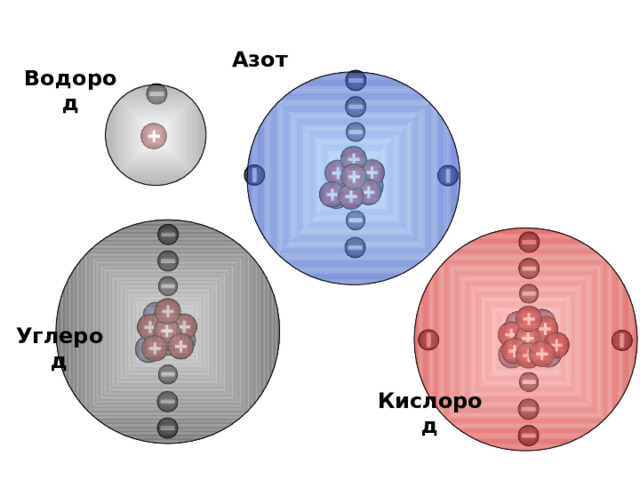
Азот
Водород
Углерод
Кислород
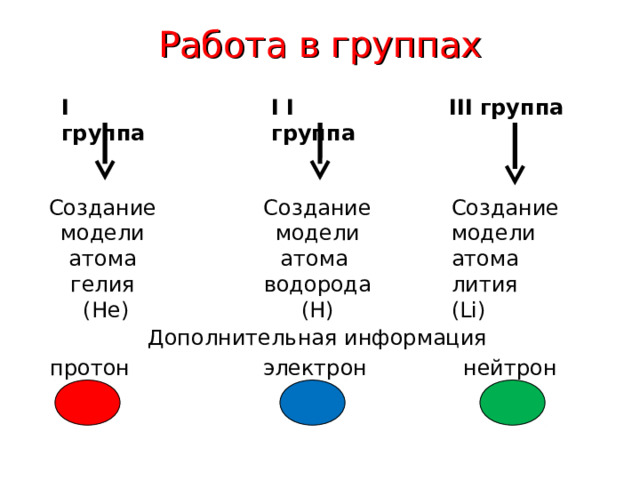
Работа в группах
III группа
I группа
I I группа
Создание модели атома гелия
( He )
Создание модели атома водорода ( H )
Создание модели атома лития ( Li )
Дополнительная информация
протон
электрон
нейтрон
е –
е –
е –
-
-
-
n
р
n
+
+
+
р
р
n
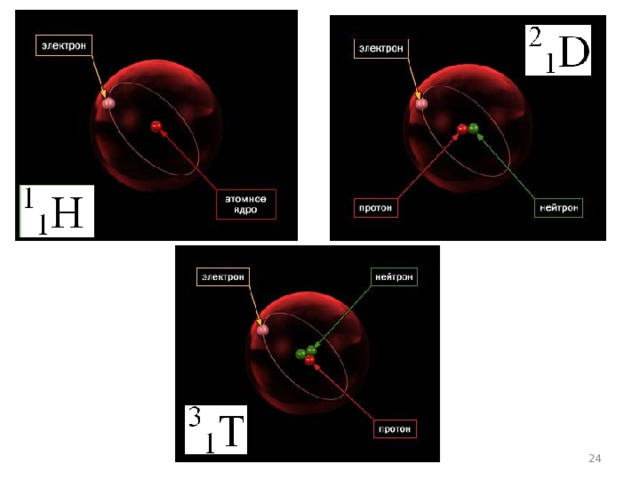
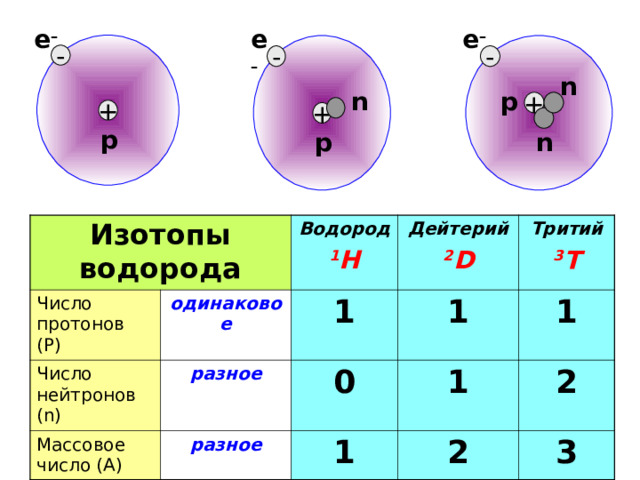
Изотопы водорода
Число протонов ( Р )
Число нейтронов (n)
Водород
одинаковое
Массовое число ( А )
1
Дейтерий
разное
1 H
Тритий
1
0
разное
2 D
1
1
1
3 T
2
2
3

- Химический элемент – это совокупность атомов с одинаковым зарядом ядра .

Тестовые задания
1) Заряд ядра атома азота равен :
а) 7 б) 13 в) 4 г) 29 д) 11
2) Число протонов в ядре атома криптона :
а ) 36 б) 17 в) 4 г) 31 д) 6
3) Число нейтронов в ядре атома цинка :
а) 8 б) 35 в) 11 г) 30 д) 4
4) Число электронов в атоме железа :
а) 11 б) 8 в) 56 г) 26 д) 30
5) Изотопы водорода отличаются друг от друга :
а)числом электронов; б)числом нейтронов;
в) химическим знаком; г) числом протонов; д)массовым числом
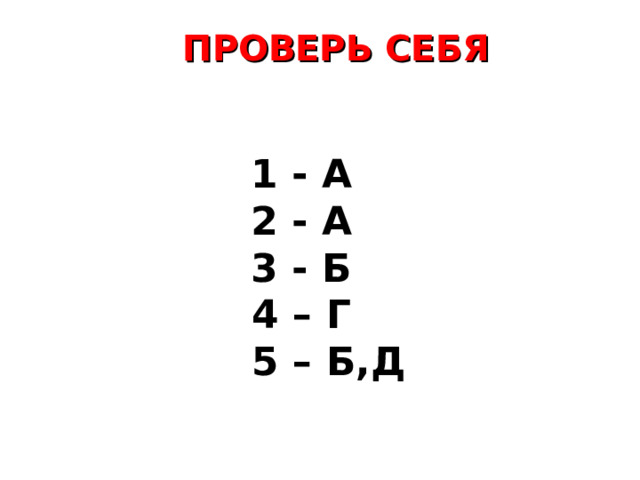
ПРОВЕРЬ СЕБЯ
1 - А
2 - А
3 - Б
4 – Г
5 – Б,Д

Критерии оценки:
5, 6 верных ответов – «5»
4 верных ответа – «4»
3 верных ответа – «3»

Рефлексия
- «Сегодня я узнал…»
- «Я понял, что…»
- «Теперь я могу…»
- «Я приобрел…»
- «Я научился…»
Рефлексия
Электроны
Протоны
Нейтроны
Я тему понял хорошо, могу объяснить другому
Недостаточно понял эту тему, сам ошибаюсь
По данной теме у меня остались вопросы

Домашнее задание:
- § 39, № 2, 8 стр. 169
- Творческое задание: представьте себя каким –либо физическим объектом – атомом, электроном – и напишите небольшой рассказ о своем состоянии, окружении и о том, что происходит с вами, что вы наблюдаете.
3. Используя изученные на уроке термины: атом, ядро, оболочка, протон, нейтрон, электрон, фамилии ученых: Томсон, Резерфорд, составить кроссворд.

























































