ДИСПЕРСНАЯ СИСТЕМА
Дисперсная система – структура, где мельчайшие частицы одного вещества равномерно распределены в другом веществе.
Компонент, который занимает больший объем, имеет название «среда».
Компонент, имеющий меньший объем обозначается термином «дисперсная фаза».

Окружающий нас мир состоит из множества дисперсных систем.
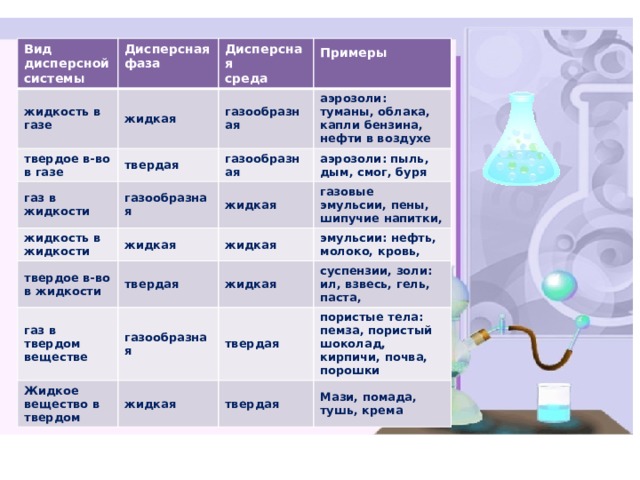
Вид дисперсной
системы
Дисперсная
жидкость в газе
фаза
Дисперсная
твердое в-во в газе
жидкая
среда
Примеры
газ в жидкости
газообразная
твердая
газообразная
аэрозоли: туманы, облака, капли бензина, нефти в воздухе
газообразная
жидкость в жидкости
твердое в-во в жидкости
жидкая
жидкая
аэрозоли: пыль, дым, смог, буря
газовые эмульсии, пены, шипучие напитки,
жидкая
твердая
газ в твердом веществе
эмульсии: нефть, молоко, кровь,
жидкая
газообразная
Жидкое вещество в твердом
суспензии, золи: ил, взвесь, гель, паста,
твердая
жидкая
пористые тела: пемза, пористый шоколад, кирпичи, почва, порошки
твердая
Мази, помада, тушь, крема
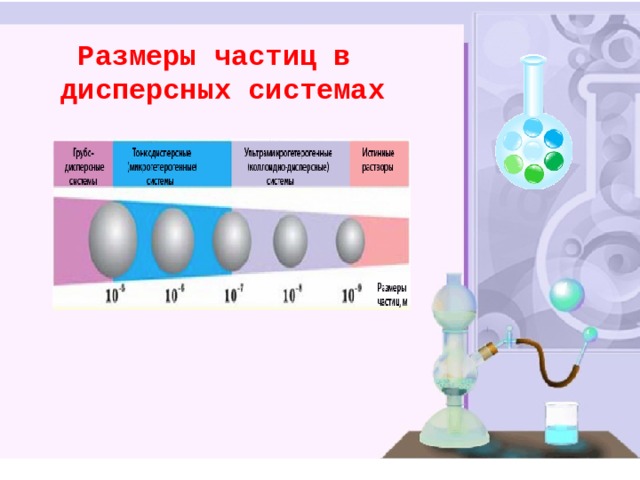
Размеры частиц в
дисперсных системах

Размеры частиц в дисперсных системах
Грубодисперсные системы
Тонкодисперсные коллоидные системы
- Эмульсии
- Суспензии
- Аэрозоли
гели, кровь, чай
соки, кофе, яичный белок
Это явление называют эффектом Тиндаля .
«светящаяся дорожка» — конус - при пропускании через них луча света.

- В нашей обыденной жизни термин раствор ассоциируется исключительно с жидкой системой.
- Раствором называется гомогенная система, образованная двумя или более веществами, которые, как правило, подразделяют на растворитель и растворенные вещества.
- Растворителем называют то вещество, которое в чистом виде находится в такой же фазе, что и раствор. В случае твердых растворов — это твердые вещества, в случае жидких растворов - жидкости.
- Если одна жидкость растворяется в другой, то растворителем обычно считается та, которой в растворе больше.
- Если вода является одним из веществ раствора, то, как правило, ее считают растворителем.
Истинные растворы
При достижении предела растворимости между растворяемым веществом и образовавшимся раствором наступает равновесие.
Раствор, находящийся при данных условиях в равновесии с растворяемым веществом, называется насыщенным раствором.
Раствор, в котором при данных условиях предел растворимости не достигнут, называется ненасыщенным.
В некоторых случаях удается получить раствор, в котором растворенное вещества содержится больше, чем в насыщенном растворе. Такой раствор называется пересыщенным.
Пересыщенные растворы неустойчивы, и иногда под действием случайных причин, например от сотрясения, избыток растворенное вещества может самопроизвольно выделиться из такое раствора.
При достижении предела растворимости между растворяемым веществом и образовавшимся раствором наступает равновесие.
Раствор, находящийся при данных условиях в равновесии с растворяемым веществом, называется насыщенным раствором.
Раствор, в котором при данных условиях предел растворимости не достигнут, называется ненасыщенным.
В некоторых случаях удается получить раствор, в котором растворенное вещества содержится больше, чем в насыщенном растворе. Такой раствор называется пересыщенным.
Пересыщенные растворы неустойчивы, и иногда под действием случайных причин, например от сотрясения, избыток растворенное вещества может самопроизвольно выделиться из такое раствора.

Растворы подразделяют на: • молекулярные — это водные растворы неэлектролитов — органических веществ (спирта, глюкозы, сахарозы и т. д.); молекулярно-ионные — это растворы слабых электролитов H 2 CO 3 , H 2 S, HNO 2 , CH 3 COOH, NH 4 OH
ионные — это растворы сильных электролитов (щелочей, солей, кислот — NaOH, K 2 S0 4 , HN0 3 , НС1О 4 ).
Растворы подразделяют на:
- молекулярные — это водные растворы неэлектролитов — органических веществ (спирта, глюкозы, сахарозы и т. д.)
- молекулярно-ионные — это растворы слабых электролитов (H 2 CO 3 , H 2 S, HNO 2 , CH 3 COOH, NH 4 OH)
- ионные — это растворы сильных электролитов (щелочей, солей, кислот — NaOH, K 2 S0 4 , HN0 3 , НС1О 4 )