
Теория электролитической диссоциации
(обобщающий урок)

Терминология Фарадея
1833-1834 гг.
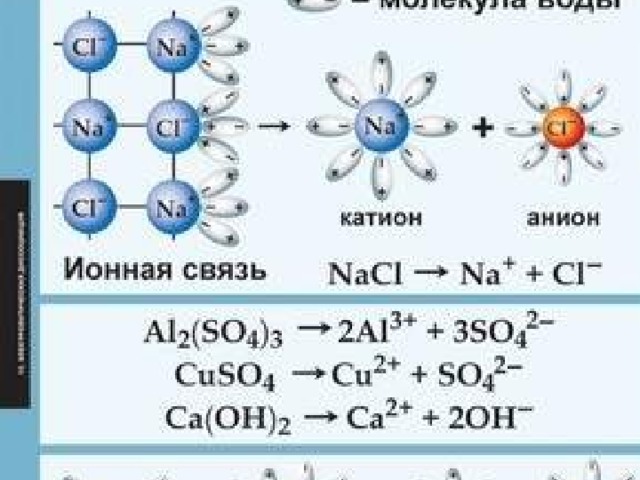
Ион
Катион
Анион
Электролит
Катод
Анод
Электролиз
Диэлектрическая проницаемость
Майкл Фарадей
(1791 -1867)

Предыстория открытия ТЭД
1857 г. Р. Клаузиус создал теорию электропроводности.
Ионы образуются в растворе без воздействия тока.
Рудольф Клаузиус

Теория растворов Менделеева
18 65-1887 г. цикл работ по изучению растворов
Гидратная теория растворов
1865 г. докторская диссертация
«О соединении спирта с водою»
1887 г. «Исследование водных растворов
по удельному весу»
Д.И. Менделеев
(1834-1907)
Изучил зависимость плотности от состава
для 233 веществ
H 2 SO 4
H 2 SO 4 H 2 O
H 2 SO 4 6 H 2 O
H 2 SO 4 150 H 2 O
1889 г. выступил на заседании РФХО
«О диссоциации растворенных веществ в воде»,
опровергая идеи Аррениуса.

Теория электролитической диссоциации
1883 г. – защита диссертации
« Химическая теория электролитов »
Электролиты в растворе распадаются на ионы
под действием молекул полярного растворителя –
электролитическая диссоциация
Сванте Аррениус
(1859-1927)
Ионы существенно отличаются от атомов.
В растворе ионы движутся хаотично.
При пропускании через раствор электролита постоянного
электрического тока ионы перемещаются направленно:
катионы к катоду, анионы к аноду.
 30% Соли Зависит: от природы электролита от t ° от с Органические кислоты, H 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Щелочи HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3 " width="640"
30% Соли Зависит: от природы электролита от t ° от с Органические кислоты, H 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Щелочи HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3 " width="640"
Сильные и слабые электролиты
Слабые,
Средней силы,
3%
Сильные,
30%
Соли
Зависит:
электролита
Органические
кислоты,
H 2 S
H 2 SiO 3
H 2 CO 3
HCN
H 3 PO 4
HF
HNO 2
H 2 SO 3
Щелочи
HCl, HBr, HI
H 2 SO 4
HNO 3
HClO 4 , HClO 3
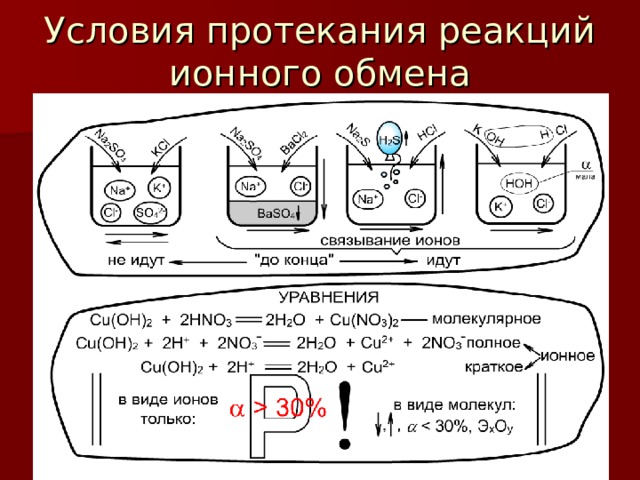
Условия протекания реакций ионного обмена

Проверь свои знания
2. Положительно заряженные ионы
2. Катионы
3. Отрицательно заряженные ионы
3. Анионы
4. Вещества, растворы и расплавы которых проводят электрический ток
4. Электролиты
5. Вещества растворы и расплавы которых не проводят электрический ток
5. Неэлектролиты
6. Электролиты, в растворах которых все молекулы распались на ионы
6. Сильные электролиты
7. Вещества частично диссоциирующие на ионы
7. Слабые электролиты
8. Процесс распада электролитов на ионы при растворении в воде или расплавлении
8. Электролитическая диссоциация

Генетическая связь между классами неорганических соединений с точки зрения ТЭД
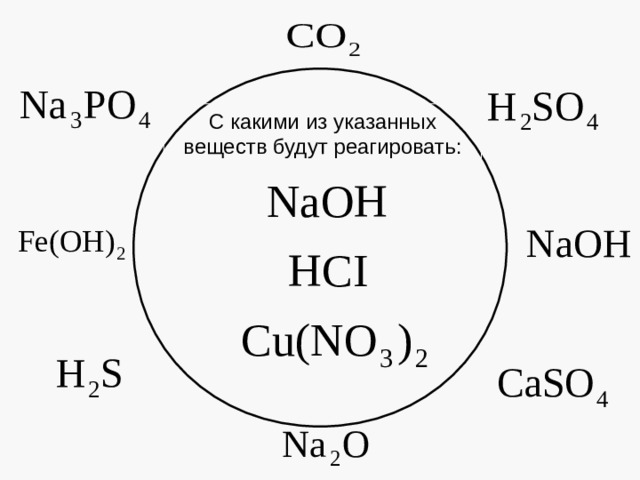
С какими из указанных веществ будут реагировать :

Практическое задание : условия протекания реакций ионного обмена

Правила техники безопасности
(а) тушить спиртовку только колпачком;
(б) запрещается зажигать одну спиртовку от другой, передавать спиртовку в зажженном виде;
(в) запрещается пробовать вещества на вкус;
(г) запрещается брать вещества руками;
(д) запрещается выливать или высыпать
остатки реактивов в склянки и банки,
из которых они были взяты;
(е) запрещается менять пробки и пипетки
от различных банок или склянок;
(ж) работать только над столом;
(з) смыть водой, затем нейтрализующим веществом реактив,
если он попал на кожу или одежду;
(и) собирайте остатки веществ в
специально предназначенную посуду
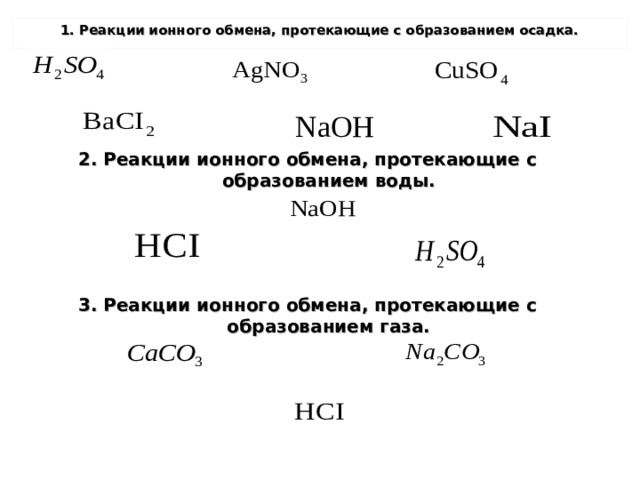
1. Реакции ионного обмена, протекающие с образованием осадка.
2. Реакции ионного обмена, протекающие с образованием воды.
3 . Реакции ионного обмена, протекающие с образованием газа.

2006 г. 9Б класс
Презентация фрагмента урока

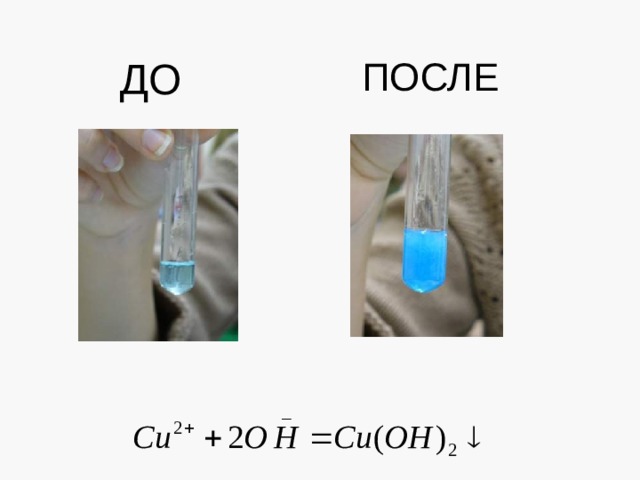
ДО
ПОСЛЕ


ДО
ПОСЛЕ

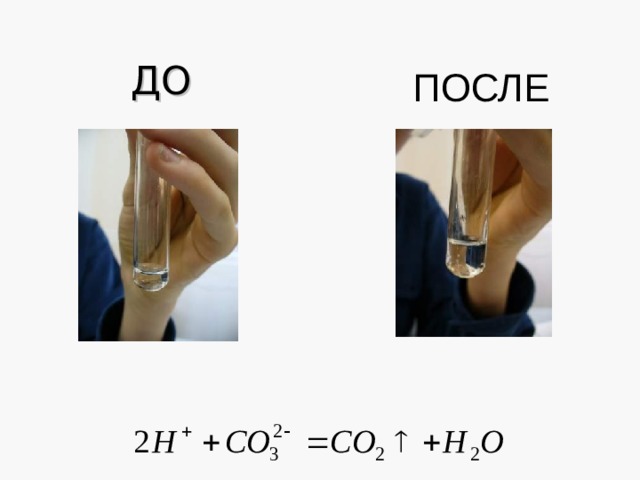
ДО
ПОСЛЕ













 30% Соли Зависит: от природы электролита от t ° от с Органические кислоты, H 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Щелочи HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3 " width="640"
30% Соли Зависит: от природы электролита от t ° от с Органические кислоты, H 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Щелочи HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3 " width="640"


























