
ЭЛЕКТРОЛИЗ
Подготовка к ЕГЭ
Розенман
Елена Александровна
МОУСОШ №2 г. Буй
Костромская область

ЦЕЛЬ ЗАНЯТИЯ:
Изучить сущность процесса электролиза, научиться писать уравнения электролиза. Решить задания №№ 20, 31, 32, 34

ЭЛЕКТРОЛИЗ
окислительно – восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или водный раствор электролита.
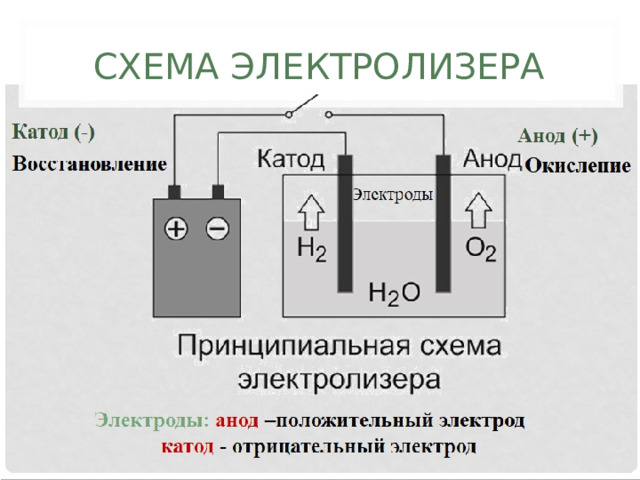
СХЕМА ЭЛЕКТРОЛИЗЕРА

МНЕМОНИЧЕСКОЕ ПРАВИЛО
Для запоминания катодных и анодных процессов в электрохимии существует следующее мнемоническое правило:
У анода анионы окисляются.
На катоде катионы восстанавливаются.
В первой строке все слова начинаются с гласной буквы, во второй — с согласной.

ЭЛЕКТРОЛИЗ РАСПЛАВОВ ОКСИДОВ
На катоде идет восстановление:
Me n+ + ne — → Me 0 , т.е. на катоде выделяется металл.
На аноде окисляется кислород:
2O -2 -4e — → O 2
Возьмем для примера электролиз расплава
оксида калия: 2K 2 O → 4K + O 2

ЭЛЕКТРОЛИЗ AL 2 O 3
Расплав Al 2 O 3 в Na 3 AlF 6 (криолит)
В расплаве криолита оксид алюминия диссоциирует на ионы:
Al 2 O 3 → Al 3+ + AlO3 3-
(–) Катод: Al 3+ + 3ē = Al 0
(+) Анод: 4 AlO 3 3- – 12ē = 2Al 2 O 3 + 3O 2 ↑
2Al 2 O 3 = 4Al +3O 2

ЭЛЕКТРОЛИЗ РАСПЛАВОВ ОСНОВАНИЙ
На катоде традиционно восстанавливается
металл:
Me n+ +ne — = Me 0
На аноде будет окисляться кислород в
составе гидроксид-группы:
4OH − −4e =2H 2 O + O 2

ЭЛЕКТРОЛИЗ РАСПЛАВА NAOH

ЭЛЕКТРОЛИЗ РАСПЛАВОВ СОЛЕЙ
1. Электролиз расплава бескислородной
соли:
На катоде всегда восстанавливается
металл: Me n+ +ne — = Me 0
На аноде окисляется бескислородный
анион: A n- — ne — = A 0
Электролиз расплава NaCl: 2NaCl = 2Na + Cl 2

ЭЛЕКТРОЛИЗ РАСПЛАВА KI

ЭЛЕКТРОЛИЗ РАСПЛАВОВ СОЛЕЙ
2. Электролиз расплава кислородсодержащей соли
(элемент аниона не в высшей степени окисления):
На катоде всегда восстанавливается
металл: Me n+ +ne — = Me 0
На аноде будет окисляться элемент
+4 +6
аниона: SO 3 2- — 2e — = SO 3
Например, электролиз расплава сульфита
натрия:
Na 2 SO 3 = 2Na + SO 3
S в сульфите имеет степень окисления +4, при
электролизе она окисляется до +6 — SO 3

ЭЛЕКТРОЛИЗ РАСПЛАВОВ СОЛЕЙ
3. Электролиз расплава кислородсодержащей соли
(элемент аниона в высшей степени
окисления):
На катоде все без изменений
На аноде — т.к. элемент уже в высшей
степени окисления, то окисляться будет
кислород:
+4 +4
2CO 2 3- — 4e — = 2CO 2 + O 2
Например, электролиз расплава карбоната
натрия:
2Na 2 CO 3 = 4Na + 2CO 2 + O 2

ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ
При электролизе водных растворов, кроме ионов электролита, присутствуют молекулы воды и ионы Н + и ОН - - продукты диссоциации воды.
Катодные процессы. Последовательность разрядки катионов на катоде зависит от положения металла в электрохимическом ряду напряжений.

Катодные процессы
Катионы металлов от лития до алюминия (включительно), не восстанавливаются на катоде, вместо них восстанавливаются молекулы воды, катионы металлов остаются в растворе.
2Н 2 О +2е - = Н 2 + 2ОН -

Катодные процессы
Катионы металлов от алюминия до водорода восстанавливаются на катоде одновременно с молекулами воды.
Ме n+ +ne - = Me 0
2Н 2 О +2е - = Н 2 + 2ОН -
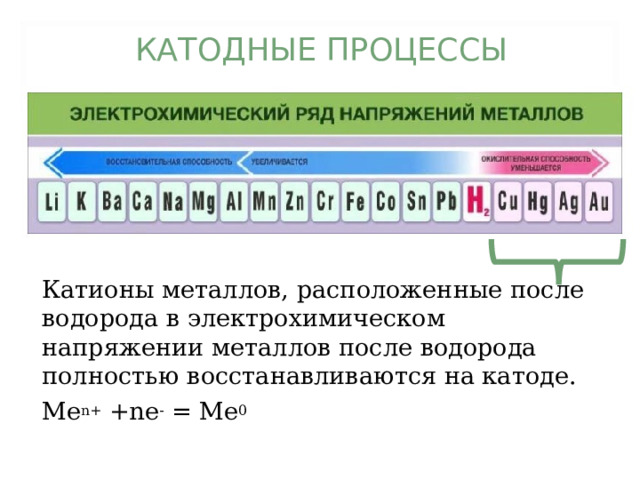
КАТОДНЫЕ ПРОЦЕССЫ
Катионы металлов, расположенные после водорода в электрохимическом напряжении металлов после водорода полностью восстанавливаются на катоде.
Ме n+ +ne - = Me 0

Катодные процессы
Если водный раствор содержит катионы различных металлов, то при электролизе восстановление их на катоде происходит в порядке уменьшения их химической активности.
При электролизе растворов кислот на катоде восстанавливаются катионы водорода.
2Н + + 2е - = Н 2 0
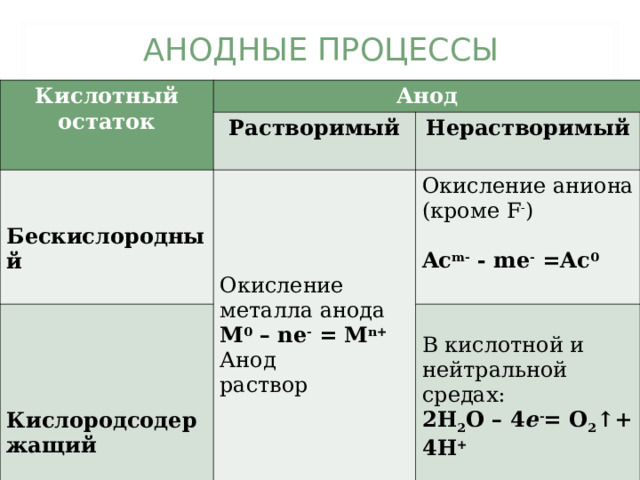
АНОДНЫЕ ПРОЦЕССЫ
Кислотный остаток
Анод
Растворимый
Бескислородный
Нерастворимый
Окисление металла анода
M 0 – ne - = M n+
Анод раствор
Кислородсодержащий
Окисление аниона (кроме F - )
Ac m- - me - =Ac 0
В кислотной и нейтральной средах:
2 H 2 O – 4 e - = O 2 ↑+ 4 H +
В щелочной среде
4 OH - – 4 e - = 2 O 2 ↑+ 4 H +

ЭЛЕКТРОЛИЗ РАСТВОРОВ СОЛЕЙ КАРБОНОВЫХ КИСЛОТ

КАКИЕ ПРОЦЕССЫ ПРОИСХОДЯТ С ИОНАМИ НА КАТОДЕ И АНОДЕ?
Катод (−) Н 2 О + 2е → Н 2 + 2ОН − *1
Анод (+) 2 I − -2 e → I 2 0 *1
электролиз
2Н 2 О + 2 I − → Н 2 + 2ОН − + I 2
электролиз
2Н 2 О + 2К I → Н 2 + 2КОН + I 2

СХЕМА ЭЛЕКТРОЛИЗА РАСТВОРА СУЛЬФАТА МЕДИ (II)

ПРИМЕНЕНИЕ ЭЛЕКТРОЛИЗА
- Электрометаллургия
- Получение газов, металлов, щелочей, кислот
- Рафинирование металлов
- Гальваностегия
- Гальванопластика

ЭЛЕКТРОМЕТАЛЛУРГИЯ:
- получение активных металлов ( K , Na , Ca , Mg , Al и др.) электролизом расплавов природных соединений;
- получение металлов средней активности ( Zn , Cd , Co ) электролизом растворов их солей
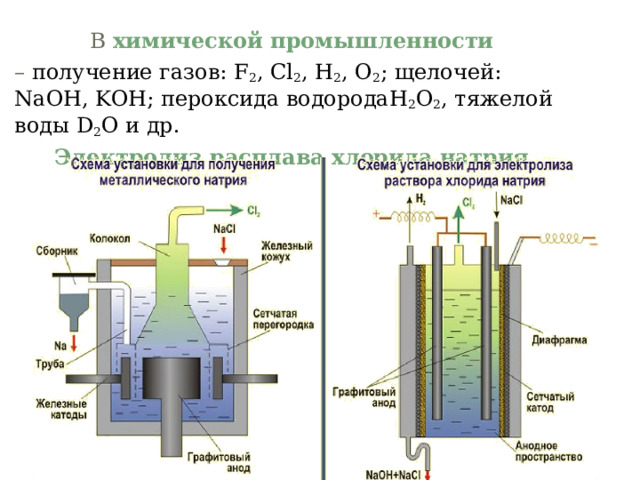
В химической промышленности
– получение газов: F 2 , Cl 2 , H 2 , O 2 ; щелочей: NaOH , KOH ; пероксида водорода H 2 O 2 , тяжелой воды D 2 O и др.
Электролиз расплава хлорида натрия
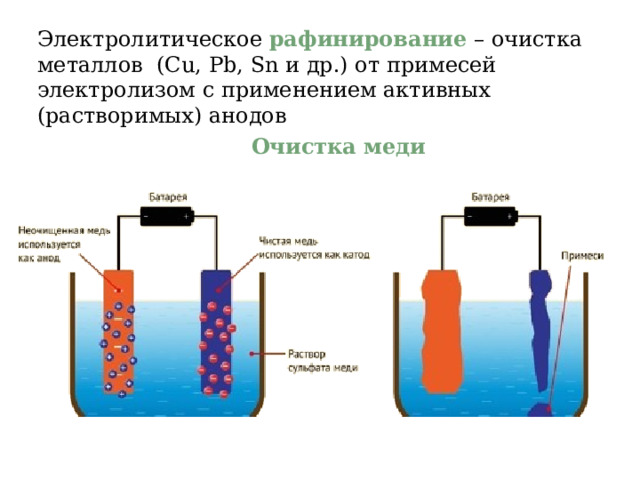
Электролитическое рафинирование – очистка металлов ( Cu , Pb , Sn и др.) от примесей электролизом с применением активных (растворимых) анодов
Очистка меди

ГАЛЬВАНОСТЕГИЯ
нанесение металлических покрытий на поверхность металлического изделия для защиты от коррозии или придания декоративного вида. Например, оцинковка, хромирование, никелирование и пр.

ГАЛЬВАНОПЛАСТИКА
- получение металлических копий с различных матриц, а также покрытие неметаллических предметов слоем металлов.
- Последний процесс (золочение деревянных статуй и ваз) был известен еще в Древнем Египте

ЗАДАНИЕ № 20
Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора
ФОРМУЛА СОЛИ
ПРОДУКТ НА АНОДЕ
А) NaI
1) H 2
Б) BaCl 2
2) I 2
В) AgNO 3
3) NO
Г) K 2 SO 4
4) Cl 2
5) SO 2
6) O 2

ЗАДАНИЕ №31
- Пример задания : провели электролиз раствора хлорида натрия, к полученному раствору добавили хлорид железа( III), выпавший осадок отфильтровали и прокалили, твёрдый остаток растворили в иодоводородной кислоте.
- Вариант ответа :
- 2 NaCl + 2H 2 O = Н 2 + 2 Na ОН + Cl 2 ( электролиз).
- FeCl 3 + 3NaOH = Fe(OH) 3 ↓ + 3NaCl.
- 2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O.
- Fe 2 O 3 + 6HI = 2FeI 2 + I 2 + 3H 2 O.

ЗАДАНИЕ ЕГЭ №31
Ещё один пример : при электролизе водного раствора нитрата меди(II) получили металл, который обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества, это вещество нагрели с концентрированным раствором гидроксида калия.
Вариант ответа :
2Cu(NO 3 ) 2 + 2H 2 O = 2Cu + 4HNO 3 + O 2 (электролиз).
Cu + 2H 2 SO 4 (конц.) = CuSO 4 + SO 2 ↑ + 2H 2 O.
SO 2 + 2H 2 S = 3S + 2H 2 O.
3S + 6KOH = 2K 2 S + K 2 SO 3 + 3H 2 O
(возможно образование K 2 S 2 O 3 ).

ЗАДАНИЕ 32

ЗАДАНИЕ ЕГЭ №34
Электролиз 80 г 22,35%–го раствора хлорида калия продолжали до тех пор, пока на катоде не выделилось 8,96 л (при н.у.) газа. К оставшемуся раствору добавили при небольшом нагревании 8,52 г оксида фосфора (V), полученный раствор охладили. Вычислите массу безводной соли калия, выпавшей в осадок, если ее растворимость в холодном растворе равна 25 г/100 г воды.
Полный разбор задачи можно посмотреть по ссылке:
https://stepenin.ru/tasks/task33/test1944/5?ysclid=mhkqk6a9f1440531910

ИСПОЛЬЗУЕМЫЕ САЙТЫ
- https://chemer.ru/services/electrolysis/melts/Na3PO4
- https://ya.ru/images/search?lr=10700&source=serp&text=%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D0%B7%20%D1%80%D0%B0%D1%81%D0%BF%D0%BB%D0%B0%D0%B2%D0%B0%20%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%BA%D1%81%D0%B8%D0%B4%D0%B0%20%D0%BD%D0%B0%D1%82%D1%80%D0%B8%D1%8F
- https://ya.ru/images/search?lr=10700&text=%D0%B3%D0%B0%D0%BB%D1%8C%D0%B2%D0%B0%D0%BD%D0%BE%D1%81%D1%82%D0%B5%D0%B3%D0%B8%D1%8F
- https://studarium.ru/article/157?ysclid=mhkhpwy8d175088889
- https://ya.ru/images/search?lr=10700&text=%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D0%B7%20%D1%85%D0%BB%D0%BE%D1%80%D0%B8%D0%B4%D0%B0%20%D0%BD%D0%B0%D1%82%D1%80%D0%B8%D1%8F
- rosuchebnik.ru
- https://ya.ru/images/search?img_url=https%3A%2F%2Fstankotk.ru%2Fwp-content%2Fuploads%2Fb%2F8%2Fb%2Fb8bb1fbcaec515118b15ce2ee8a319c5.jpeg&lr=10700&pos=6&rpt=simage&source=serp&text=%D0%B3%D0%B0%D0%BB%D1%8C%D0%B2%D0%B0%D0%BD%D0%BE%D0%BF%D0%BB%D0%B0%D1%81%D1%82%D0%B8%D0%BA%D0%B0%20%D0%BA%D0%B0%D1%80%D1%82%D0%B8%D0%BD%D0%BA%D0%B8
- https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D0%B7


















































