СПИРТЫ

Предельные одноатомные спирты

R–OH, или С n Н 2n +1 O Н
Предельными одноатомными спиртами или алканолами называют органические соединения, в молекулах которых алкильный радикал (R) связан
с гидроксильной группой.
—
—
—
—
Н
Н
H — C — C — O — H
Н
Н
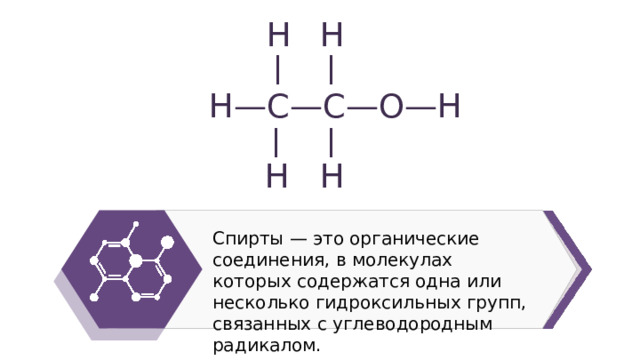
Спирты — это органические соединения, в молекулах которых содержатся одна или несколько гидроксильных групп, связанных с углеводородным радикалом.
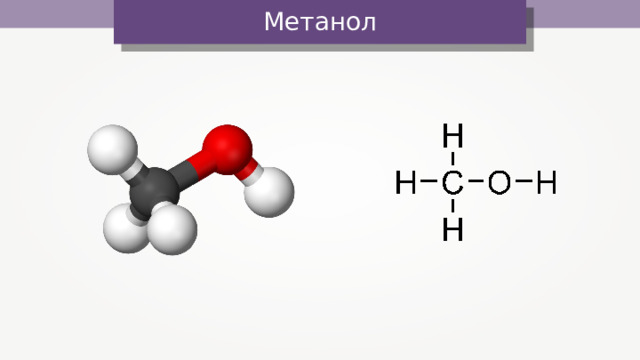
Метанол
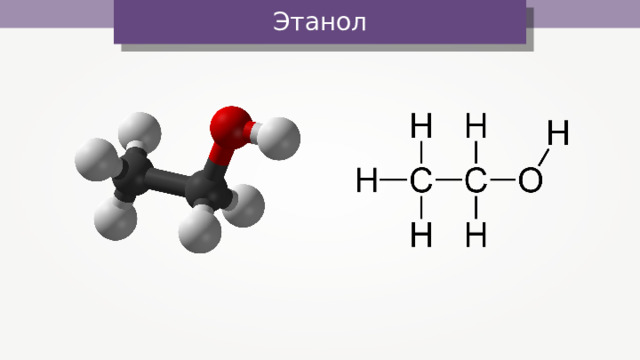
Этанол
Одноатомные спирты
С H 3 OH
С H 3 OH
Метиловый спирт
Метанол
С 3 H 7 OH
С 3 H 7 OH
Пропиловый спирт
Пропанол
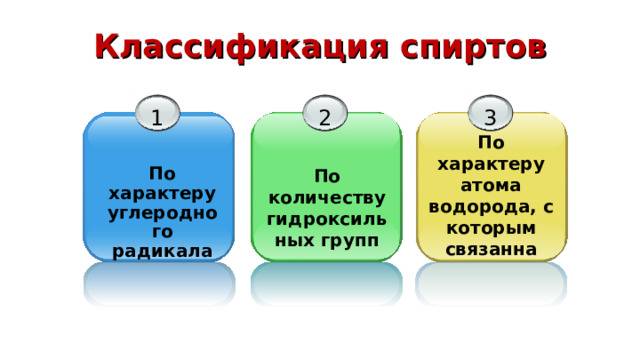
Классификация спиртов
2
1
3
По характеру атома водорода, с которым связанна гидроксильная группа
По характеру углеродного радикала
По количеству гидроксильных групп
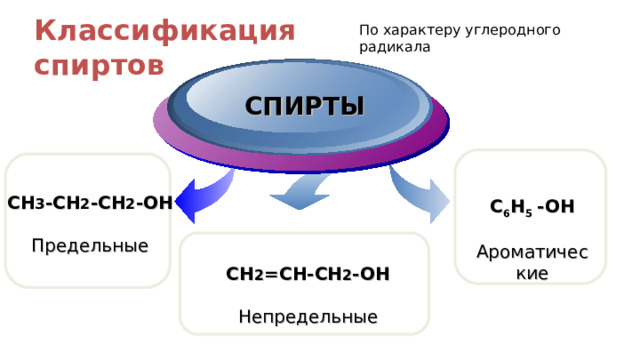
Классификация спиртов
По характеру углеродного радикала
Title
Add your text
СПИРТЫ
CH 3 -CH 2 -CH 2 -OH
Предельные
C 6 H 5 -OH
Ароматические
CH 2 = CH-CH 2 -OH
Непредельные
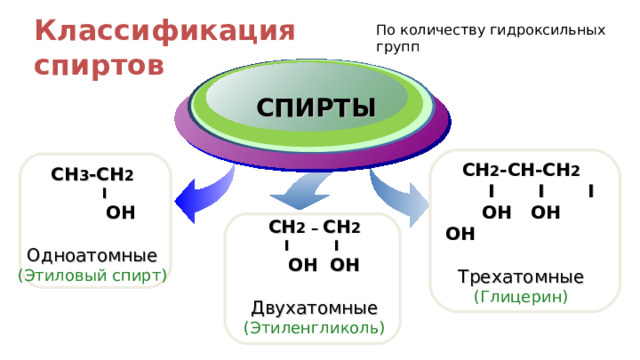
Классификация спиртов
По количеству гидроксильных групп
Title
Add your text
СПИРТЫ
CH 2 - CH-CH 2
I I I
OH OH OH
Трехатомные
(Глицерин)
CH 3 -CH 2
I
OH
Одноатомные
(Этиловый спирт)
CH 2 – CH 2
I I
OH OH
Двухатомные
(Этиленгликоль)

Классификация спиртов
По характеру атома, с которым связана гидроксильная группа
Title
Add your text
СПИРТЫ
CH 3
I
CH 3 -C- С H 3
I
OH
Третичные
(2-метилпропанол-2)
CH 3 -CH 2 -CH 2
I
OH
Первичные
(пропанол - 1)
CH 3 - CH 2 -CH- С H 3
I
OH
Вторичные
(бутанол - 2)

Гомологический ряд предельных
одноатомных спиртов
Формула
СН 3 OH
Название
С 2 Н 5 OH
Метанол
Число изомеров
Этанол
С 3 Н 7 OH
С 4 Н 9 OH
Пропанол
Бутанол

ИЗОМЕРИЯ СПИРТОВ
Для алканолов характерны три вида изомерии :
изомерия положения гидроксильной
группы в углеродной цепи
изомерия углеродного скелета
межклассовая изомерия
(с простыми эфирами)

Изомерия положения гидроксильной группы в углеродной цепи
CH 3 -CH 2 -CH 2 -OH
пропанол-1
н. -пропиловый спирт
CH 3 -CH-CH 3
l
OH
пропанол-2
(изопропиловый спирт)

Изомерия углеродного скелета
CH 3 -CH 2 -CH 2 – СН 2 -OH
бутанол-1
н. -бутиловый спирт
CH 3 -CH-CH 2 -ОН
l
СН 3
2-метилпропанол-1
(изобутиловый спирт)

—
—
—
—
—
—
—
—
Межклассовая изомерия
Н
Н
Н
Н
H — C — O—C — H
H — C — C — O — H
Н
Н
Н
Н
Простые эфиры – органические вещества, молекулы которых состоят из двух углеводородных радикалов, соединённых посредством атома кислорода.
Общая формула R – O – R

Физические свойства спиртов:
Алканолы являются бесцветными жидкостями или кристаллическими веществами с характерным запахом. Первые члены гомологического ряда имеют приятный запах, для бутанолов и пентанолов запах становится неприятным и раздражающим.

Водородная связь
Высокая температура кипения спиртов объясняется значительным межмолекулярным взаимодействием – ассоциацией молекул, возможность которой объясняется полярностью связи О–Н и неподелёнными электронными парами атомов кислорода. Такое взаимодействие называют водородной связью.

Метанол, этанол и пропанол смешиваются с водой в любых отношениях.
Все спирты легче воды.

Средние спирты имеют неприятный запах, а высшие — запаха не имеют.

Метиловый спирт — сильный яд!
В малых количествах вызывает слепоту,
а в больших — смерть.

Химические свойства спиртов:
Реакции окисления
Реакция замещения атомов водорода группы -ОН
Реакция дегидратации (отщепления молекулы воды)
Реакция замещения -ОН группы

Взаимодействие с активными металлами (щелочными и щёлочноземельными)
При взаимодействии
с активными металлами спирты проявляют свойства слабых кислот и образуют соли, называемые алкоголятами.
2CH 3 OH + 2Na = 2CH 3 ONa + H 2 ↑
алкоголят

Алкоголяты химически не стабильны и при действии воды гидролизуются с образованием спирта и гидроксида металла.
C 2 H 5 O К + H 2 O = C 2 H 5 OH + К OH

Одноатомные спирты
не взаимодействуют с растворами щелочей!!!

Взаимодействие с галогеноводородами
CH 3 -OH + H-Cl = CH 3 -Cl + H 2 O
метанол
хлорметан
 140 o C Н ОН Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства) " width="640"
140 o C Н ОН Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства) " width="640"
—
—
—
—
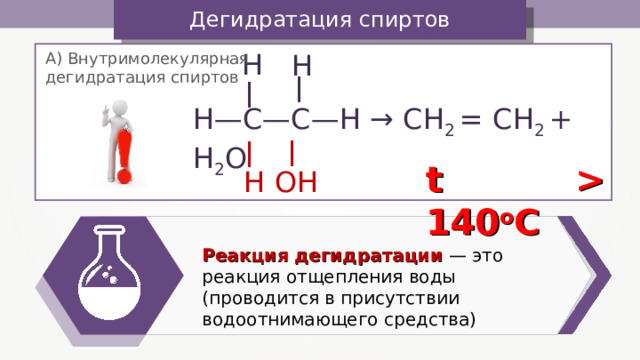
Дегидратация спиртов
Н
Н
А) Внутримолекулярная дегидратация спиртов
Н—С—С—Н → CH 2 = CH 2 + H 2 O
t 140 o C
Н
ОН
Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства)

Дегидратация спиртов
Б) Межмолекулярная дегидратация спиртов
→ C 2 H 5 —O—C 2 H 5 + H 2 O
C 2 H 5 OH
C 2 H 5 O H
диэтиловый эфир
t o C
Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства).

—
—
—
—
—
—
Окисление спиртов
О
окислитель
С 2 Н 5 О H → H 3 C—C
H
ацетальдегид
этанол
(первичный спирт)
Дихромат калия ( K 2 Cr 2 O 7 )
СН 3
СН 3
окислитель
—
H 3 C — C — OH → H 3 C—C—O
Н
Перманганат калия
(КМ n О 4 )
диметилкетон
изопропанол
(вторичный спирт)
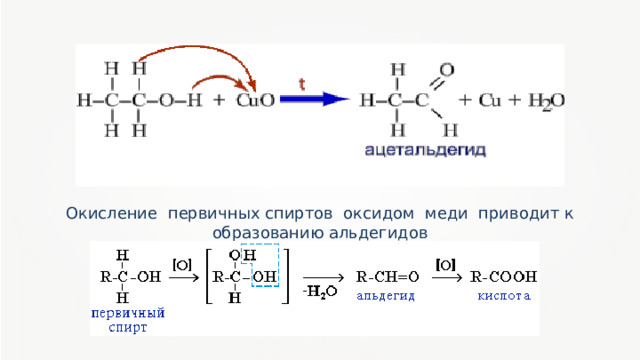
Окисление первичных спиртов оксидом меди приводит к образованию альдегидов
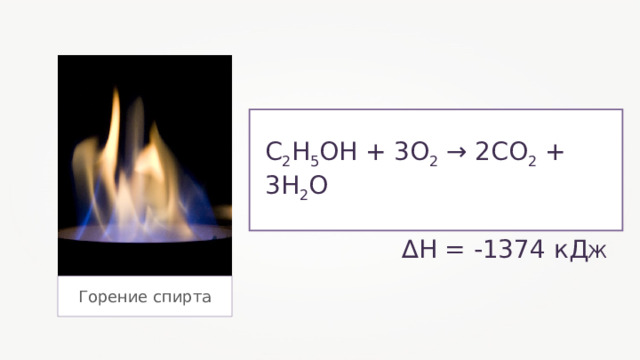
С 2 Н 5 ОН + 3О 2 → 2СО 2 + 3Н 2 О
∆ Н = -1374 кД Ж
Горение спирта

Получение спиртов
C О + 2 H 2 → C Н 3 О H
«Синтез-газ» — смесь, которую получают в результате взаимодействия метана с водяным паром при высокой температуре.
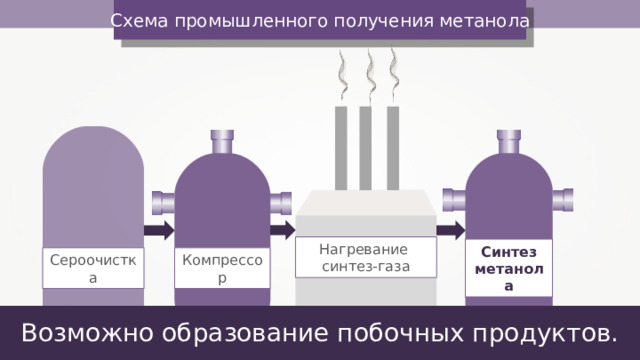
Схема промышленного получения метанола
Нагревание
синтез-газа
Синтез метанола
Компрессор
Сероочистка
Возможно образование побочных продуктов.

—
—
—
O
Pt
СН 3 —С + H 2 → С 2 H 5 OH
Восстановление альдегидов
H
этанол
этаналь
С H 3 — CH 2 —Cl + NaOH ( водн) → C Н 2 —CH 2 —OH + NaCl
хлорэтан
Щелочной гидролиз галогенпроизводных алканов
катализатор
—
Н 2 С—С H 2 + H 2 O → C 2 H 5 OH
Гидратация алкенов
этанол
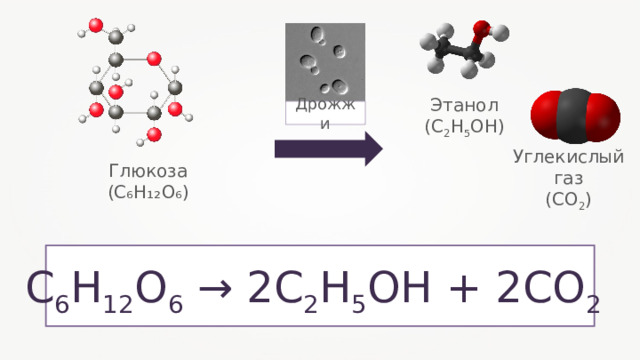
Этанол
(С 2 Н 5 ОН)
Дрожжи
Углекислый газ
(СО 2 )
Глюкоза
( C₆H₁₂O₆ )
С 6 Н 12 О 6 → 2С 2 Н 5 ОН + 2СО 2
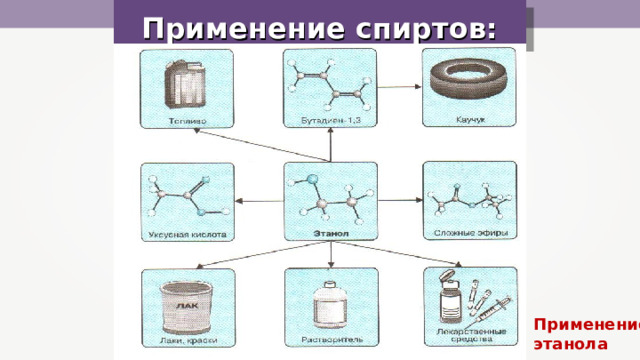
Применение спиртов:
Применение
этанола

Спирты можно использовать для получения всевозможных органических соединений, применяемых в качестве органических растворителей при производстве полимеров, красителей и лекарственных препаратов.

Большие объёмы метанола используют при добыче и транспорте природного газа.

Метанол — наиболее токсичное соединение среди всех спиртов!
100 мл
смертельная доза при приёме внутрь

Бутанол используют как растворитель жиров и смол, кроме того, он служит сырьём для получения душистых веществ.
Бутанол
(С 4 H 9 OH )
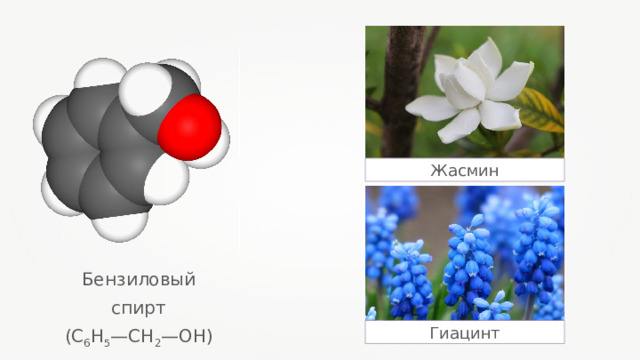
Жасмин
Бензиловый спирт
(С 6 Н 5 —CH 2 —OH )
Гиацинт


Домашнее задание:
§9,
с. 74 зад. 1,7,8 (устно)
11 (письм.)































 140 o C Н ОН Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства) " width="640"
140 o C Н ОН Реакция дегидратации — это реакция отщепления воды (проводится в присутствии водоотнимающего средства) " width="640"


























