
«Химия» пәні ЕРІТІНДІЛЕР . ЕРІТІНДІЛЕР КОНЦЕНТРАЦИЯСЫ. ТҰЗДАР ГИДРОЛИЗІ.

Жоспар:
- Ерітінділердің анықтамасы және олардың концентрациясын бейнелеу әдістері
- Заттардың ерігіштігі және оған әсер ететін факторлар
- Тұздар. Тұздар гидролизі.

Дәрістің мақсаты :
а ) білімділік: Студенттерге тұздар гидролиз туралы мағлұмат беру, тұз ерітіндісіндегі реакция ортасын анықтау тәсілдерін үйрету.
ә) дамытушылық: гидролиз реакция теңдеулерін жүйелі жазуларын, химиялық тілде сөйлеуін, тез ойлау қабілеттерін дамыту.
б) тәрбиелік: олардың концентрациясы және тұздар гидролизі туралы жалпы мысал келтіртіре отырып, есеп шығару арқылы түсіндіру. қауіпсіздік техникасының ережелерін ескеріп, оқушыларға эстетикалық тәрбие беру.

тұздар гидролиз туралы көрсетілім
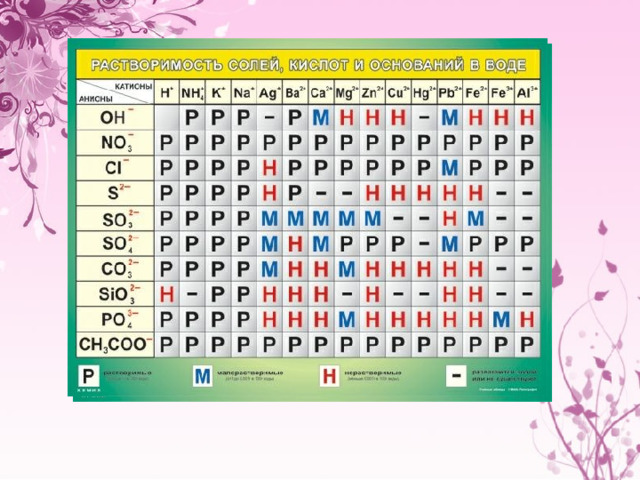

- . Тұз ерітінділерінің гидролизі
- Тұздың гидролизі деп тұздың сумен әрекеттесуін атайды, және оның барысында кейбір өзгерістерге ұшырайды:
- 1) ортаның рН көрсеткіші қышқылдық немесе сілтілі ортаға ығысады;
- 2) әлсіз электролиттің молекуласы немесе ионы (катион немесе анион) түзіледі:
- а) егер гидролиздің бастапқы сатысында оң бөлшек түзілсе ( CuOH+ ), онда гидролиз катион бойынша жүріледі;
- б) егер гидролиздің бастапқы сатысында теріс бөлшек түзілсе ( HCO- ), онда гидролиз анион бойынша жүріледі.
- 3) тұздардың көбісі сатылап гидролизденеді. Сатылар саны әлсіз қышқылдағы сутек иондарының санына немесе әлсіз негіздегі гидроксил иондарының санына тәуелді
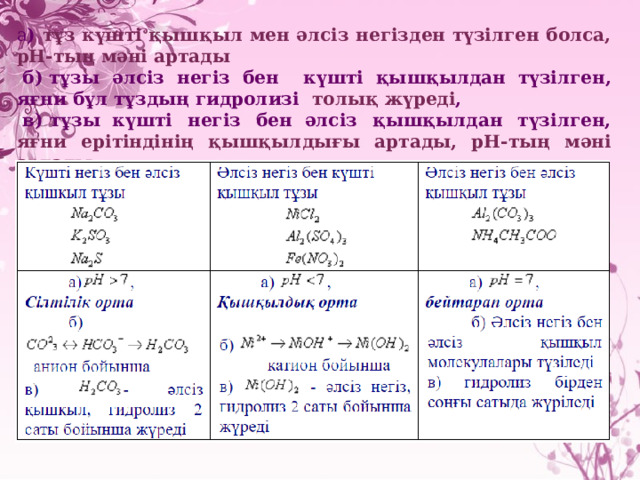
а ) тұз күшті қышқыл мен әлсіз негізден түзілген болса, рН-тың мәні артады
б) тұзы әлсіз негіз бен күшті қышқылдан түзілген, яғни бұл тұздың гидролизі толық жүреді ,
в ) тұзы күшті негіз бен әлсіз қышқылдан түзілген, яғни ерітіндінің қышқылдығы артады, рН-тың мәні артады.






- Гидролизге ұшырайтын тұздардың үш жағдайында да жүйе тепе-теңдікке келіп тұр, олай болса, әрекеттесуші массалар заңын қолданып тепе-теңдік константасын жазуға болады, оны гидролиз константасы деп атайды.
- К г = К Н2О /К қышқ. не К г = К Н2О /К нег. , К Н2О – судың иондық көбейтіндісі. Бұл қатынастардан қышқыл не негіз әлсізірек болған сайын, яғни диссоциация константалары аз болған сайын гидролиз тереңірек жүретіні көрінеді. Гидролиздің қаншалықты жүретіндігін гидролиз дәрежесі һ та көрсетеді, ол
- h = тұздың гидролизге ұшыраған моль саны/тұздың жалпы еріген моль саны .
- h = √К г /С м , бұл теңдеуден тұздың концентрациясы аз болған сайын, гидролиз дәрежесі көп болатындығын көруге болады.
 7 с) pH 6. Қай тұздың ерітіндісінде қышқылдық орта болады? а) Na 2 SO3 б) AI(NO3)3 с) AgCI " width="640"
7 с) pH 6. Қай тұздың ерітіндісінде қышқылдық орта болады? а) Na 2 SO3 б) AI(NO3)3 с) AgCI " width="640"
- IV Бекіту Тест тапсырмалары
- 1.Тұздар гидролизі дегеніміз не?
- ) қышқылдардың сумен реакциясы;
б) тұздардың сумен реакциясы;
с) негіздердің сумен реакциясы;
2. Мына заттардың қайсысы сілтілік орта көрсетеді?
а) KNO3 б) BaCI2 с) K 2 CO3
3. Қай ион лакмустың күлгін түсін қызыл түске ауыстырады:
а) Н+ б) Сa 2+ с) OH-
4. Күкірт қышқылы мен натрий сульфиді арасындағы қысқартылған иондық теңдеу қайсысы:
а) 2H+ + S2- = H 2 S↑
б) Ba 2+ + SO42- = BaSO4 ↓
с) 2H+ + SO32- = H 2 O + SO2↑
5. Гидролиз теңдеуінің ортасы қандай?
K 2 S + HOH =
а) pH = 7 б) pH 7 с) pH
6. Қай тұздың ерітіндісінде қышқылдық орта болады?
а) Na 2 SO3 б) AI(NO3)3 с) AgCI

- 7. Күшті электролиттер қатарын тап:
а) KCI, H 2 S, FeCI3 б) HCIO4, H 2 SO4, HI c) HCN, HCI, K 2 S
8. Әлсіз электролиттер қатарын тап:
а) KCI, NaNO3, H 2 O б) H 2 S, NaOH, NaCI с) Fe(OH) 2 , H 2 S, HCN
9. Гидролизденетін тұздар жұбы:
- FeCI 2 , NaNO3 б) MgSO4, K 2 SO4 с) FeCI3, CrCI3
- 10. Қышқылға тән диссоциациялану теңдеуі:
а) Na+ + HSO4- б) H+ + CI- с) Mg2+ + 2CI-
11. Суда ерігенде гидроксид – ион түзетін заттың атауы:
а) темір ІІІ гидроксиді
б) барий гидроксиді
с) магний гидроксиді
12. Электр тогын өткізетін ерітінді:
а) қант б) натрий сульфаты с) оттек
13. Құрамында 49 г күкірт қышқылы бар ерітіндіге 6,5 г мырыш салғанда бөлінген сутектің көлемі қандай?
а) 22,4 л б) 2,24 л с) 0,22 л
14. Құрамында 49 г күкірт қышқылы бар ерітіндімен 4 г магний оксидін өңдегенде алынған тұздың массасын табыңдар.
а) 13,6г б) 16 г с) 12,5 г

Ұсынылатын әдебиеттер тізімі:
1. Глинка Н.Л. Общая химия.-Москва: Интеграл- Пресс, 2003,-728с.
2. Коровин Н. В. Общая химия: - Москва: Высшая школа, 2000, -557 с.
3. Лучинский Г.П. Курс химии . - Москва: Высшая школа, 1985. - 258 с.
4. Дроб ы шева Т.И. Общая химия.-Ростов н/Д: Феникс, 2004.-448с.
5. Коржуков Н.Г. Общая и неорганическая химия.- Москва: МИСИС: ИНФРА-М, 2004-512с.
6. Гольдбрайх З.Е.Сборник задач и упражнений по химии.-Москва: ООО Издательство «Астрель», 2004,-383с.
7. Зайцев О.С.Задачи, упражнения и вопросы по химии.-Москва, Химия, 1996.-432с.
8. Коровин Н.В., Мингулина Э.И., Рыжова Н.Г.Лабораторные работы по химии.-Москва: Высшая школа, 2001.-256с.



















 7 с) pH 6. Қай тұздың ерітіндісінде қышқылдық орта болады? а) Na 2 SO3 б) AI(NO3)3 с) AgCI " width="640"
7 с) pH 6. Қай тұздың ерітіндісінде қышқылдық орта болады? а) Na 2 SO3 б) AI(NO3)3 с) AgCI " width="640"












