

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока

Ффффююзииииисссссс
Просмотр содержимого документа
«Ффффююзииииисссссс»

 Сѳз башы
Сѳз башы
Физика кесиби боюнча адистиктери боюнча дардоочу жогорку окуу жайларында физиканы окутуу үч циклдан турат.Жалпы физика деп аталат биринчи циклде математикалык аппараты мүмкүн болушунча жѳнѳкѳй түрдѳ жана азыраак колдонуу менен физиклык негизги фактылар баяндалат. Андан соњ теориялык физика курсу жана студенттин адистиги боюнча айтайын курстар окулат.
Атомдук кубулуштарды теориялык физика курсунда баяндоо кванттык механиканын жоболорун колдонуу менен жүргүзүлот . Атомдук физиканы физиканын жалпы курсунда окутууда бир топ кыйынчылыктар орун алат. Буга кошумча атомдук физиканы кыргыз тилинде окууга багышталган окуу китептери жокко эссе десек жанылышпайбыз. Ошондуктан овторлор китепте атомдук кубулуштарды физиканын жалпы курсунун кѳлѳмΥндѳ кванттык кѳзкараштын негизинде баяндоого аракет жасашты.Мында колдон келишинче негизги фактыларды түшүндүрүүгѳ жана азыркы физиканын элестетүүлѳрүнүн калыптанууларына арналган материалдарды берүүгѳ аракет кылдык.
Физиклык кубулуштарды баяндоодо математикалык аппараты зарылдыгына жараша пайландык.Атап айтканда, аныксыздык катнашы , энергиянын,импультун моментинин жана классикалык кѳзкараштардын негизинде болгон натыйжалар кандайча пайда болорун кароодо так ой жүргүзүүлѳр менен кошо математикалык эсептѳѳлѳр менен кошо математикалык эсептѳѳлѳр жүргүзүлдү.
Китеп атомдук физика курсу оптика курсу оптика курсунан кийин, ядролук физика курсунун алдында окутулат деген негизде жазылды. Ошондуктан китепте ядролук физика таптакыр каралган жок. Ошону менен бирге булл курста, адата, оптика курсуна кирип кетүүчү атомдордун оптикалык спектрлери,Зеемандын эффектиси ж.б.у.с бѳлүмдѳр каралды. Бул болүмдѳрдүн атомдук физика курсуна киргизилиши студенттердин материалды ѳздѳштүрүүсүндѳ кошумча кыйынчылыктардын пайда болуусун жоюуга жасаган аракет болуп эсептелет.
Жогорку окуу жайлардын физикалык жана инжинердик адистигиндеги студеттерине багышталган булл китеп атомдук физика курсу оптика курсунан кийин окутулушун талап кылган Кыргыз Республикасынын билим берүү министрлиги тарабынан физика багыты боюнча жогорку билим берүүнү кийин окутулушун талап кылган Кыргыз Республикасынын билим берүү министрлиги тарабынан физика багыты боюнча жогорку билим берүүнүн 1999-жылы кабыл алынган мамлекеттик стандартына ылайык түзүлгѳн типтүү программанын негизинде биринчи ирет кыргызча жазылып отурат.Андыктан анын дурус жактары менен кошо эле, мүчүлүштүктѳрү да болушу мүмкн . Окуу китебинде байкалган мындай калпыстыктар жѳнүндѳгү сын-пикирлерди авторлор ыраазыччылык менен кабыл алып, бул китеп студенттердин билиминин тер ыраазыччылык менен кабыл алып, бул китеп студенттердин билиминин терӊдешине кандайдыр бир дењгээлде ѳбѳлгѳ түзѳт деп үмүттѳнүшѳт.
 КИРИШΥΥ
КИРИШΥΥ
АТОМДУК ФИЗИКАНЫН ӨНΥГΥШΥНΥН ТАРЫХЫ
Байыркы дүйнѳдѳгү атомдук окуу. Атомдор жѳнүндѳ окуу байыркы дүйнѳдѳ эле пайда болгон. Кѳрүнүктүү грек философтору Левкипп (б.з.ч 500) Анаксагор (б.з.ч 500-428-жж) Эмпе докл(б.з.ч 492-432-жж) нерселердин атогмдук түзүлүшү жѳнүӊдѳгү окууну ѳнүктүрүшкѳн. Булардын ичинен Демокриттин эмгеги ѳтѳ зор.Заттардын эӊ кичине бѳлүнбѳс бѳлүкчѳлѳрдѳн атомдордон (грек тин атоммос-бѳлүнбѳс деген сѳзүнѳн) тураары жѳнүндогү ой Демокрит тарабынан тѳмѳндѳгүчѳ айтылган:
Жаратылышта атомдордон жана бош мейкиндиктен башка эч нерсе болбойт
Атомдордун саны жана анын формаларынын ар түрдүүлүгү чексиз болот.
Нерселер атомдордун саны жана ажырашы менен гана пайда полушат жана жлугушат
Нерселердин ортосундагы айырмачылык алардын атомдорунун саны, чон дугу, формасы жна тартиби менен шартталат; атомдордун ортосундагы сапаттуу айырмачылык жок.
Кыймыл кандайдыр бир табияттан тышкары кγчтөр менен эмес, атомдордун өзγнө тиешелγγ кγчтөр менен шартталат
Демокриттин атомдук окуусу өтө терен материалисттик окуу болгон.
Бирок анын көз карашындагы бош мейкиндик жөнγндө ой олуттуу жетишпегендик болгон. Буга байыркы дγйнөнγн көрγнγктγγ ойчул. Аристотель (б.з.ч 384-322-жж) каршы чыккан. Ал материя γзгγлтγксγз деген көз карашка бош мейкиндик болушу мγмкγн эмес деп эсептеген. Бирок ушу менен бирге эле Аристотель бөлγнбөс атомдордун бар экендигин да танган.
Ошентип, байыркы дγйнөдөэле материянын табияты жөнγндөгγ
карама- каршы көзкараштардын курөшγ пайда болгон : бир көзкараш материя бөлγнөт жана γзгγлтγктγγ десе, экинчиси материя γзγлтγксγз болот деп эсептеген. Бул кγрөш көптөгөн кылымдар бою уланып, байыркы дγйнөнγн илиминен физиканын өнγгγшγнγн кийинки мезгилдерине чейин келип жеткен. Ошентип, атомдук көзкараш кылымдар бою ар кандай агымдардын, окуулардын каршылыгына дуушар болуп, аларды женγγ менен өнγгγп, бγгγнкγ кγндөгγ бардык табият таануунун негизи болуп калды. Бγгγнкγ кγндө физика табиятты диалектикалык негизде карама-каршылыктардын бирдиги жана кγрөшγ катарында тγшγнөт: материя γзгγлтγктγγ (атомдук) да γзгγлтγксγз (туташ) да болот.
Демокриттин атомдук окуусу афиналык грек окумуштуусу Эпикур, байыркы римдик философ жана акын Лукреций Кар ( б.з.ч 95-55) тарабынан өнγктγрγлгөн.
Эпикур өзγнγн атомдук окуусунда атом жөнγндөгγ Демокриттин көзкарашына таянат, бирок андан айырмаланып жарартылыштагы табиягый, психикалык жана социалдык кубулуштарды да атомдор менен байланыштырат.
Лукреций атомдор баш аламан кыймылда болушат деп эсептеген,
Аны караӊгы бөлмөдөгү күн шооласындагы байкалган чаӊчалары кыймылына окшоштуруп алардын кыймылынын моделин түзөт. Бул илимдин тарыхында молекулалык кыймылдыөөнүн алгачкысы болгон.
Эпикур-Лукрецийдин атомдук окуусу Демокриттин көзкараштарын уланткан жана өнүктүргөн . Бирок алардын атомдук окуусу Демокриттикине караганда тагыраак жана кеӊирирээк болгон. Демокрит боюнча атом таза геометриялык түзүлүш катарында каралат, алар формасы жана көлөмү менен гана мүнөздөлөт. Ал эми Эпикур жана Кардын окуусунда атом салмакка, тыгыздыкка (катуулукка) жана түз сүзыктуу кыймылдан өз алдынча чет төөчү ички жөндөмдүүлүккө ээ бөлүкчө болуп эсептелет.
Ошентип, байыркы дүйнөдөгү ойчулдар атомду материянын эӊ кичине бөлүкчөсү ддеп эсептешкен. Бирок убакыттын өтүшү менен байыркы атомдук окуу унутулуп калган.
Орто кылымда. Орто кылымдын шартында атом жөнүндөгү илим өнүгө алган эмес, себеби анын негизин түзгөн материалисттик көзкараш ошол кезде дүйнөнү бийлеп турган диний көзкараштарга карама-каршы болгон . Ушуга жана ар кандай алхимия, астрономия ,магия ж.б.у.с жалган илимдер дүркүрӨп өсүшүнө байланыштуу атом жөнүндөгү окуунун өнүгүшү мүмкүн эмес эле.
Кайра Жаралуу доору. XVII жана XVIII кылымдардагы атомдук окуу. Кайра жаралуу доорунда башка илимдер сыяктуу эле, атом жөнүндөгү окуу сезилээрлик ийгиликтерге жетише баштаган. Бул ошол кездеги экономиканын,техниканын, илимдин жана коомдун кыймылынын башка тармактарынын дүркүрөп өсүшү мене шартталат.
Байыркы дүйнөдөгүдөй эле бул мезгилдеги атомдук көзкакраштар тажрыйбага таянган эмес жана анын өнүгүшү ой жүгүртүлөргө негизделген.
Ошондуктан бул мезгилде материянын үзгүлтүктүүлүгү жана үзгүлтүксүздүгү жөнүндөгү маселеге болгон көзкараштар ар кандай болгон . Ошол кездеги белгилүү окумуштуулар – Г.Галилей (1564-1642-жж) жана Р.Декарт (1596-1650-жж) атомдук көзкарашты колдошкон эмес. Бирок Декарттын көзкарашында материянын үзгүлтүксүздүгү жөнүндөгү эскертүү үстөмдүүлүк кылса да ал материянын бөлүкчөлөрдөн тураарын танган эмес.Декарт бош мейкиндиктин бар экенин четке каккае. Декартка тескерисинче П.Гассенди (1592-1655-жж) Демокрит сыяктуу бөлүнбөс атом жанат алардын ортосундагы бош мейкиндик жөнүндөгү көзкарашты өркүндөткөн. Материянын түзүлүшүнө болгон көзкараштардын эки багытынын ортосундагы күрөштө И.Ньютондун (1642-1727-жж) механика жана бүткүл дүйнөлүк тартылуу тармактарындагы белгилүү ачылыштардагы чоӊ мааниге ээ болгон. Ньютондун окуусу кыйыр түрдө атом жөнүндөгү илимдин өнүгүшүнө өбөлгө түзгөн, ал эми Ньютондун жолун жолдоочулар ушул эле убакта Декарттын көзкарашында болушкан. Өздөрүнүн теорияларында алар нерселердин ортосундагы аралыкта аракет этишүү боштук аркылуу ишке ашат деп эсеп тешкен. Ньютондун жолун жолдоочуларынын бири чех окумуштуусу И.Боскович (1711-1787-жж) алыска аракет этүүчү күчтөр тҮшүнүгүнүн негиздеги материянын атомдук элестетилишин иштеп чыккан. Ал алыскы аралыкда бөлүкчөлөр таралышат, жакында – түртүлүшөт деп эсептеген. Бул элестетүүлөрдүн негизинде кристаллдардын түзүлүшүн түшүндүрүүгө жакындоого мүмкүн болгон. Босковичтин идеясы
Жалпысына туура болгон жана кийинчерээк илимий атомистиканын өнүгүшү менен далилденген.
Атомдук окуунун өнүгүшүнө ангилист химиги Р.Бойль (1627-1691-жж), ангилист физиги Р.Гук (1635-1703-жж) жана голландиялык физик Х.Гюйгенстер (1629-1695-жж) чоӊ салым кошкон.
Материянын атомдук түзүлүшү жөнүндөгү илимдин өнүгүшүндөгү орус окумуштуусу М.В.Ломоносовдун (1711-1765-жж) эмгеги зор. Ломоносов ѳзγнγн эмгегинде химиялык элементтер жѳнγндѳгγ элестетγγлѳрдγ иштеп чыккан жана жѳнѳкѳй, татаал нерселердин курамына кирген бѳлγкчѳлѳрдγн ортосундагы айырмачылыктары аныктаган.Ошентип, Ломоносов атомдордон турган татаал бѳлγкчѳлѳр – молекулалар жѳнγндѳгγ элестетγγнγ биринчи болуп сунуш кылган.
XIX кылымда атомдук окуунун ѳнγгγшγ. XIX кылым ѳнѳр жай өндүрүшүнүн дүркүрөп өсүшү.буу кыймылдаткычтарын түзүү
, илимдин бардык тармактарындагы жетишкендиктер менен мүноөздөлөт.
Бул мезгил илимий атомистиканын дкуркүрөп өсүү мезгили болуп эсеп телет. Атом жөнүндөгү илим ири жетишкендиктери үнкөрүнүктүү ангилис химиги Д.Дальтондун (1766-1844-жж) эмгектери менен байланышкан. Атомдук богомолдун негизинде Дальтон химиялык бирикмелердеги эселик катнаш законун ачкан (1808).
1811-ж. Италилялык белгилүү физик жана химик Авогодро (1776 - 1856 -жж.) франция физиги жана химиги Гей-Люссактын (1778-1850-жж.) эмгектерине таянып, бирдей тышкы шарттарда барабар көлөмдөрдөгү бардык газдардын курамында бирдей сандагы молекулалар камтылаары жөнүндөгү законун айткан. Бул эмгегинин натыйждасында атом жөнүндөгү илим божомолдон илимий теорияга айланып, заттын түзүлүшү жөнүндөгү окуунун негизи болуп калды.
Дальтондун көзкарашы боюнча, атом бөүнбөс бөлүкчө болот. Илимий атомистиканы негиздөөчүлөрдүн биринин мындай көзкаршына карабастан. Дальтондун замандашы ангилис окумуштуусу Проут карама-каршы көз карашты айткан: атомдор татаал түзүлүшкө ээ, б.а., авлар башка бөлүкчөлөрдөн турушат. П роут бул бөлүкчөлөр суутектин атому болушат жанап башка химиялык элементтердин атомдору ушул суутектин атомдорунан турат деп эсептеген. Бирок атомдук салмактарды так өлчөөлөр, ошол кезде Проуттун көзкрашы чындыкка жакын болгон далилденген эмес- химиялык элементердин атомдук салмактарыт суутектин атомунун салмагына эселүү болгон эмес.
Нерсенин түзүлүшүнө болгон көзкараштардын өнүгүшүнө XIX кылымда заттын молекулалык-кинетикалык теориясын түзүүгө алып келди. Бул теориянын эн маанилүү абалдары мындан жүз жыл мурун эле орус окумуштуусу Ломоносовы тарабынан эле иштелип чыккан, бирок өз учурунда коомчулукка жетпей, унутулуп калган.
1827-ж. Ангилис окумуштуусу Броун микроскопиялык бөлүкчллөрдүн үзгүлтүксүз баш аламан кыймылын ачат. Броун кыймылы деп аталган, бул кубулушту молекулалык-кинетикалык теориясынын негизинде гана түшүнүгө мүмкүн болгон. Бул теория боюнча Броун кыймылы, байкоо жүргүзүлүүчү бөлүкчөлөр ичинде сүзүп жүргөн суюк заттын баш аламан кыймылдаган молекулаларынын кагылышынын натыйжасы болот.
1860-ж. Кийинки мезгилде заттын молекулалык-кинетикалык теориясын иштеп чыгууга багышталган бир катар фундаменталдык теориялык эмгектер жарык көргөн. Аларга немец физиктери А.Кренигин (1822-1879-жж.) Р.Клаузиусту (1822-1888-жж.), ангилис физиктери Ж.Жоулдун (1818-1889-жж.) Д.К.Максвеллдин (1831-1879-жж.) австриялык физик Л.Больцмандын (1844-1906-жж.), поляк физиги М.Смолуховскийдин (1872-1917-жж.) жана башка окумуштуулардын эмгектерин мисал кылсак болот. Ушул эле мегилде заттын молекулалык-кинетикалык касиетин изилдөл боюнча көптөгөн тажырыйбалар жүргүзүлгөн. Мунун баары нерселердин ккасиетин атомдор менен молекулалардын кыймылы менен түшүндүргөн заттын молекулалык-кинетикалык теориясын ар тарптан өнүктүрүүгө өбөлгө түздү.
Материянын кинетикалык теориясынын жетишкендиктери жана бул багаыттагы укмуштуудай тажырыйбалык ачуулар илимийатомистиканын салтанаты болуп калды. Ушул эле мегилде изилдеген объектилеринин жана кубулуштарынын көптөгөн кокустуктан болуучу процесстердин жыйындысы сыяктуу мүнөзүнө жараша, физикалык процесстерди иизилдөөгө ыктымалдуулук теориясынын ыкмаларын колдонгон статистикалык физика өнүкөн.
Атомдук окуу белгилүү орус окумуштуусу Д.И.Менделеевдин (1834-1907-жж.) 1869-ж. Ачкан химиялык элементтердин мезгилдик закону менен мене байыган. Бул закондун негизинде ал химиялык элементтердин мезгилдик системасын түзглн жана ага таянып, ошол тмезгилге чейин белгизсиз болгон көптөглн химиялык элементтерди алдын ала айткан. Бул закон атомдордун жана молекулалардын түзүлүшкн изилдөөчү татаал маселелерди чечүүдө өтө зор мааниге ээ болгон. Атомдук физиканын кийинчерээк жасалган ачыылары Менделеевдин ачылышын жокко чыгарбастан, аны андан ары бекемдеди.
Электирдеги атом жөнүндө окуу. Атомдук окуунун ири жетишкендигиблуп электирдин корпускулалык, атомдук түзүлүшкн негиздөө эсептелет. Бул окуунун негизинде заттын электрдик теориясы иштелип чыккан. Көрүнүктүү ангилист окуумуштуусу М.Фарадей (1791-1867-жж.) электртогунун суюктук аркылуу өткшүн изилдеп, суюктук каркылуу ӨткӨн электр саны эритмеден электроддорго бөлүнүп чыккан зат менен тыгыз байланышта болорун көргөзгөн. Бул жыйынтыктарды талдоо менен немец физиги Г.Гельмгольц (1821–1894-жж) бул кубулуш качн гана электроллитинт аралашмасындагы заттын бир валенттүү атому аралашма аркылуу электир тогу өтүлма аркылуу электир тогу өткөндө дайыма бир эле элетр зарядын ташыганда болуу мумкун деген жыйынтыкка келген. Эгерде атом эки валенттүү, үч валенттүү ж.б. у.с. болсо, анда ал тейшелүү түрдө эки, үч ж.б. эсе чоӊ электр зарядын ташыйт. Азыркы термин боюнча мындай атомдор (же атомдордун тобу) иондор деп аталышат.Мунун нешгизинде Гельмгольц электр зряддары атомдун түзүлүшүнө ээ деген жыйынтыкка келген. Электдин атому (терс зряддуц) электрон деп аталган.Электрондор кийинчерээк эркин түрдө алынган, ал эми оӊзаряддар дайыма атом менен чогуу болуп, эркин түрдө байкалган эмес. Бир топ убакыттан кийин гана,жыйырманчы кылымда оӊ электрондор – позитрондор ачылган .
Атомдук физканын пайда болушу. XIX-XX кылымдын чегинде атом элементардык бөлүкчѳ эмес, татаал түзүлүшкө ээ экендигин көргөзгөн бир катар ачылыштар жазылган. Алардын эӊ маанилүүлөрү болуп:
Катоддук нурлардын ачылышы (1879);
Фото электрдик эффект(1887);
Ренген нурларыц(1896);
Табигый радиоактивдүүлүк (1896) эсептелген.
Катоддук нурлардын ачылышы. 1879-ж. Ангилялык физик жана химик У.Крукс (18323-1919-жж.) аябай сейректкелген газы бар айнек түтүкчөгл жайгаштырылган электроддорду жогорку чыӊалуунун булагына туташтырса, анда катод такчасынан ага перпендикулярдуу багытта көзгл көрүнбөгөн, бирок түшклн женринде айнектин жаркырашын пайда кылган нурлар бөлүнүп чыгарын ачкан. Бул нурларды катоддук деп аташкан.
Крукси катоддук нурлар укмуштуудай касиетке ээ болорун , атап айтканда , газдардын нурлануусун пайда кылаарын, нерселерди ысытышарын, жлундагы жеӊил нерселерди жылдырышса тургандыгын байкапган. Ббул касиеттери боюнча нурлаодын курамындавгы кандайдыр бир матириалдык нерсе кинетикалык энергияга ээ болорун божомолдоого болот. Бирок Куркс бул нурлардын табиятын тушунгөн эмес. Ал аларды материянын “төртүнчү абалы” деп эсептешкен.
Кийинчерээк, катоддук нурлар электр талаасында оӊ заряддалган, Магинит талаасында терс заряддалган электродду көздөй кыйшаяры байк5алган, мындан нурлар терс зарядды алып жүрөөрү белгилүү болгон.
Катоддук нурлардвын касиети жана мүнөзү катоддунт заттынын жана түтүктү толтурган газдын табиятынан көзкаранды болбойт. Демек, мындан нурду пайда к4ылган нерсе5 каалагандай атомдун курамына уирери жана белгилүү бир шарттар аткаврылганда (мисалы үчүн электр талаасынын аракети астында ) анын курамына чыгып кетерин божомолдосок болот . Ошентип , атом ататаал түзүлүшкл ээ болот экен.
Электродор. 1897-Ж. Англялык физик Ж.Ж.Ж.Томсон (1856-1940-жж.) ушуга чейин ктоддук нурлар жөнүндө белгилүү болгон маалыматтарды жалпылап, алар тэт кичине атомдон да кичине терс заряддалгакн бөлүкчөлөрдүн агымы боло тургандыгы жөнүндө тыянакка келет. Англиялык физик С.Стонейдин сунушу боюнча томсон бул бөлккчөнү электрон деп атаган.
Кийинчерээк элетронду бөлүп чыгаруу жөндөмдүүлүгүнө ысытылган металлдар (термоэлектрондук эмиисия), жогорку температурадакгы газдар жана рентген же ультракызгылткөк нурлардын аракетине дуушар болгон көптөглн заттар джа ээ болушаары белгилүү болот.
Катоддук нурлардын аракети астында катоддук түтүктө газдын оӊ зарядалган бөлккчөллрк – оӊ иондор пайдап болору3да байкалат. Алар электрондордун кыймылына каршы багыттак кыймылдашат(аноддук нурлар). Иондордун пайда болушу, атомдун курамына электрондордун кире тургандыгын дагы биржолу далил дейт.
Атомдун кичине бөлкчл ьбар экендигин ырастоо илимий чөйрөдө өтл чоӊ кызугууну туудурган. Физиктер электрондун зарядынын чоӊдугу эмнеге барабар экендигинаныктоого бир топ араккетерди жасашкан. Акеыркы океыркы он жылдын ичинде Томсон эле бул чоӊдукту ллчөөгл он бир жыл аракет жасап, айырмаланышкан он бюир натыйжаны алган. 1917-жз. Ган бул чоӊдук Р.Миликкен (1868-1953-ж) тарабынан туура аныталган. Электрондун заряды е=1,60*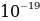 Кл , массасы 9,106*
Кл , массасы 9,106*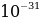 кг га барабар. Электрондун массасы эӊ жеӊнил атом суутектин атомдун какраганда 1836 эхсе кичине болот.
кг га барабар. Электрондун массасы эӊ жеӊнил атом суутектин атомдун какраганда 1836 эхсе кичине болот.
Атомдун алгачкы моделдери. Чогуусунан караганда атом электр –т бейтараптуубөлүкчө болгондуктан, ал эми электрон бардык атомдордун курамына киргендиктенатомдун курамына суммардык заряды электрондордун суммардык терс зарядын теЧогуусунан караганда атом электр –т бейтараптуубөлүкчө болгондуктан, ал эми электрон бардык атомдордун курамына киргендиктенатомдун курамына суммардык заряды электрондордун суммардык терс зарядын теӊдеген оӊ заряддалган Бөлүкчөлөр керек экендиги жөнүндө пайда болот. Мындан бул заряддардын атомдун курамындагы жайланышы кандай ? – дген суроо туулат.
1903-ж. Томсон сунш кеылган алгачкы моделдердин бири боюнчак оӊ зряд атомдун бүт көлөмүнүн ичинде бир калып бөлүштүрклөт, ал эми электрондор тконцентрдик шакектер түрүнл атомдун көлөмү боюнча жайланышып аны бейтараптайт. Б ирок модель эксперименттин натыйжалары мене олуттуу карама-каршы болгондугун жараша (  -бөлүкчөнүн чачырашы, спектрдик түзүлүштөрүндөгү закон ченмдүүлүктөр, ж.у.с.) тез эле четке кагылган . Атомдун тазыркы кездеги түзүлүштөгү көзкараштарды негиздөөнү англиялык физик Э.Резе5рфорд (1871-1937-жж.) баштаган.
-бөлүкчөнүн чачырашы, спектрдик түзүлүштөрүндөгү закон ченмдүүлүктөр, ж.у.с.) тез эле четке кагылган . Атомдун тазыркы кездеги түзүлүштөгү көзкараштарды негиздөөнү англиялык физик Э.Резе5рфорд (1871-1937-жж.) баштаган.
1896-Ж. Беолгилүү француз физиги А.Беккерель (1852-1908-жж.) уран жана анын бирикмелери өзүнөн-өзү фототактачаныкаратууга жөндөмдүү нурларды чыгараарын байкаган. Бул нурлануу эч кандай тышкы шарттардан көзкаранды болбостон, күн сайын бирдей дозада болуп турган. Бул кубулуш радиоактивдүүлүк, ал эми нурлар болсо Беккерлердин нурлары деп аталган.
Радиоактивдүүлүктү андан ары изилдөнүү Беккерлердин жардамчылары П.Кюри (1867-1934-жж.)ждана анын аялы М.Склодовская-КЮРИ (1867-1934-жж.) улантышкан. Көрсө Беккерель нурнларды татаал курамга ээ болушат экен. Бул нурлар эектр талаасынын таасирине баш ийбеген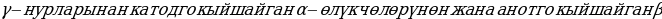 -
-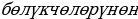 турат.
турат.
Резерфорддун модели жана анын жетишпегендиктери.1911-Ж. Резерфорд радий мене иштеп, аркандай чөйрөдөгү  –
– 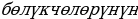 чачырашын изилдеген. Чачыроонун фотосүрөттөрүнүн көбү
чачырашын изилдеген. Чачыроонун фотосүрөттөрүнүн көбү  –
– 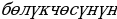 изи түз сызык боюнча калаарын, кээде анча чоӊ эмес бурчка, чанда гана (10 000 учурдун бири нде ) бөлүкчө 120-150⁰ ка, кыйшаярын, ал гана эмес тескери багытка да чачыраарын көргөзгөн.
изи түз сызык боюнча калаарын, кээде анча чоӊ эмес бурчка, чанда гана (10 000 учурдун бири нде ) бөлүкчө 120-150⁰ ка, кыйшаярын, ал гана эмес тескери багытка да чачыраарын көргөзгөн.
Мындан  – бөлүкчөлөрү чоӊ массага ээ, абдан кичине көлөмгө топтолгон өтө күчтүү электр талаасы келип киретболуш керек деген ой туулат. Ошентип, атом оӊ зарядка ээ өзөккө-ядрого ээ болот деп эсеп теген дагы бир модель (ядролук) пайда болот. Бул моделди Резерфорд төмөндөгүчл элестеткен:
– бөлүкчөлөрү чоӊ массага ээ, абдан кичине көлөмгө топтолгон өтө күчтүү электр талаасы келип киретболуш керек деген ой туулат. Ошентип, атом оӊ зарядка ээ өзөккө-ядрого ээ болот деп эсеп теген дагы бир модель (ядролук) пайда болот. Бул моделди Резерфорд төмөндөгүчл элестеткен:
-атом борборунда, анын ичиндеги мейкиндиктин кичине бөлүгүн ээлеген, оӊ заряддалган ядро жайланышат;
-ядронун айланасында тегерек орбита боюнча жалпы саны ядронун оӊ зарядына барабар болгон электрондор айланып жүрүшөт;
-ядро мене электрондун ортосундагы тартылуу күчтөрүү электрондун айлануу кыймылында пайда болгон борбордон четтөөчк күч менен теӊ салмакташатда, электрондор лз орбиталарында кыймылдашып,ядрого келип түшүшпөйт.
Күн системасына окшоштугуна жараша Резерфорддун негизделген бюиринчи модели болуп эсептелет. Ошентип, илимде биринчи жолу атомдун түзүлүшү жөнүндөгү элестетүү киргизилген. Бирок бир катар фактылар Резерфорддун теориясына карама-каршы келген.
Резерфорддун планетардык (ядролук) моделиндеги электрондун орбита боюнча кыймылын классикалык түшүнүктөрүн негизинде кароо туцрактууатомдор болбой тургандыгы жөнүндөгү акылга сыйбаган (пардоксалдык) жыйынтыккаалып келет: классикалык электрдинамика боюнча электрон өзүнүн орбитасында турактуу кыймылдай албайт, себеби айланган электр зряды электромагиниттик толкундарды нурлантып,натыйжада энергиясын жоготушу керек, ошондуктан анын орбитасынын радиусу үзгүлтүксүз азайып, 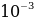 с убактысында электрон тядрого түшүп калмак. Бирок атомдор табиятта турактуулукка ээ болушу менен кезигет.
с убактысында электрон тядрого түшүп калмак. Бирок атомдор табиятта турактуулукка ээ болушу менен кезигет.
Буга кошумча, электрондун орбита боюнча айлануусунун жыштыгынын үзүлтүксүз өзгөрүшү, нурлануунун жыштыгынын үзүлтүксүз өзгөрүсүнө алып келмек. Бирок атомдун оптикалык4 спектрлери жыштыктардын тиешелүү маанилерине ээж сызыктардын мүнөздүү удаалаштыгынан тургакн сызыктуу, үзгүлтүктүү түзүлүшкл ээ болушат. Бул болсо классикалык физиканын закондорун атомдогу электрондордун кыймылын жазууга колдонууга болбойт дегенди билгизет.
Атомдун турактуулугун түшүндүрүү үчүн 1913-ж. Н.Бор (1885-1962-жж.) жылуулук нурлануусун түшүндүрүүдө М.Планк4 (1858-1947-жж.) сунуш кылган, А.Эйнштейн (1879-1955-жж) оркүндөткөн кванттык теориянын жоболорун колдонгон.Планктын теориясы боюнча жарык энергиясын нурлантуу жанажутуу үзгүлтүксүз эмес, белгилүү үлүш – квант түрүндө болот.Кванттын энергиясы нурлануу жыштыгынан көзкаранды болот.
E=hv,
Мында v – нурлануунун жыштыгы h – плактын турактуусу деп аталган , 6,62*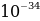 Ж*с га барабар чоӊдук. Планкжарыктын квантык касиети нурлануу жана жутуу учурунда, б.а., ьжарык зат мене аракетенишкенде гана орун алат деп эсептеген.Планк боюнча жарыктын мейкиндикте таралышы классикалык жоболорго баш иет. Планктын кɵзкарашы ɵркүндɵтүп, Эйнштейн жарык мейкиндике таралганда да ɵзүн бɵлүкчɵ катары алып жүрɵт деп эсептеген.
Ж*с га барабар чоӊдук. Планкжарыктын квантык касиети нурлануу жана жутуу учурунда, б.а., ьжарык зат мене аракетенишкенде гана орун алат деп эсептеген.Планк боюнча жарыктын мейкиндикте таралышы классикалык жоболорго баш иет. Планктын кɵзкарашы ɵркүндɵтүп, Эйнштейн жарык мейкиндике таралганда да ɵзүн бɵлүкчɵ катары алып жүрɵт деп эсептеген.
Кванттарды бɵлүп чыгарганда жана жутканда нурланткан нерсенин энергиясы секириктүү ɵзгɵрүшү керек, нерсе жарым жартылай кванты бɵлүп чыгара албайт. Ошентип, жарык корпускулалык касиетке ээ болот жана анын энергиянын эн кичине үлүшү – квантка ээ “бɵлүкчɵсү” фотон деп аталат.
Бор атом ядросунун электр талаасындагы электрондун кыймылы үчүн анын кыймыл санынын моменти да каалагандай мааниге ээ эмес, белгилүү гана (кванталган) маанилерге ээ болот деп божомолдогон. Ал маанилери бирдик кванд 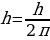 ге эселүү болушу керек.
ге эселүү болушу керек.
Бор, электрон кванттоо шарты мүмкүнчүлүк берген орбиталар боюнча кыймылдаганда (б.а. белгилүү энергиялык денгээлде жайланышканда) жарык толкунун бɵлүп чыгарбасын постулат түрүндɵ айткан. Нурлануу электрон бир орбитадан экинчисине, б.а., энергиянын бир денгээлинен (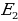 ) кичине энергияга ээ кичинесине (
) кичине энергияга ээ кичинесине (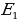 ) ɵткɵндɵ гана байкалып, энергиясы тɵмɵндɵгүгӨ барабар.
) ɵткɵндɵ гана байкалып, энергиясы тɵмɵндɵгүгӨ барабар.
hv=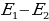
жарытын кванты пайда болот.Атомдун сызыктуу спектри ушинтип пайда болот.Бор суутектин атомунун (жана суутектин атомусыяктуу атомдор үчүн да) спектирдин сызыкчаларынын жыштыгы үчүн мурда ачылган эмпирикалык формулалардын жыйынтыгын камтыган тура формуланы алган.Атомдордо энергиялардын денгээлдердин баардыгы Ж.Франк (1882-1964-жж.) жана Г.Герц (1887-1975=жж.) тарабынан түздɵн-түз далилденген(1913-1914-жж.).
Бордун теориясынын ийгилиги квант теориясынын мурдагы ийгиликтеи сыяктуу эле, теориянын логикалык бүтүндүгүн бузуу менен ишке ашкан; бир жагынан, Ньютондун механикасы колдонулуп, экинчи жагынан , ага чоочун, классикалык электрдинакмикага карама-каршы кванттоонун жасалма эрежеси колдонулган. Буга кошумча, Бордун теориясы татаал атомдор догу (ал гана эмес гелийдеги) электрондордун кыймылын, молекуланы пайда кылган атомдордун ортосундагы байланышты ж.у.с., түшүндүрɵ алган эмес. Бордун “ жартылай классикалык” теориясы электрондун бир денгээлден экинчи денгээлгеɵткɵн учурдагы кыймылы кандай болору жɵнүндɵгү суроого да жооп бере алган эмес. Атомдун теориясынын маселелеринин андан аркы ɵнүгүшү атомдогу электрондун кыймылын классикалык механиканын түшүнүктɵрүнүн негизинде (белгилүү из же орбитадагы кыймыл катары) жазууга болбостугу, электрондун денгээлдердин ортосундагы кыймылы жɵнүндɵгү маселе электрондун атомдук абалын аныктоочу закондор менен коошпой тургандыгы жɵнүндɵгү ишенимге алып келди.
Буга кошумча Бор, жарык тажырыйба жүзүндɵ байкалган белгилүү толкундук кассиеттери (мис., жарыктын интерферон циясы, дифракциясы сыяктуу кубулуштарда байкалган ) мене бирге корпускулалык (бɵлүкчл) касиетке ээ болот,демек, жарык фотондордун агымынан турат, б.а., жарык экилтиктүү (дуализм) ,корпускула- толкундук табиятка ээ деген абалда да таянган.Натыйжада логикалык карама каршылык пайда болду; бир кубулушту түшүндүрүдɵ жарык толкундук касиетке, экинчи кубулушту түшүндүрүүдɵ бɵлүкчɵ ээ деп эсептɵɵ керек экендиги келип чыкты. Бул карама-каршылыкты чечүү кванттык механиканын физикалык негизин түзүүгө алып келди. 1924-жылы француз физиги Л. Де Броль (1892-ж) даниялык окумуштуу Н.Бор тарабынан 1913-жылы айтылган атомдук орбиталардын квантталышын шарттары жɵнүндɵгү постулатты түшүндүрүү үчүн корпускула-толкундук экилтик түүлүгүнүн жалпылыгы жɵнүндɵгү божомолду сунуш кылган. Де броль боюнча ар бир бɵлүкчɵ, анын табияттынан кɵзкарандысыз түрдɵ толку3н узундугү λ бɵлүкчɵнүн импульсу менен
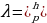 (3)
(3)
Катнашы аркылуу байланышкан толкунду тиешелүү аркылуу керек. Бул божомол боюнча толкундук касиетке жеке эле фотон эмес, бардык кадимки бɵлүкчɵлɵр (эленктрондор, протондор ж.б.) да ээ болушат. Бул божомол 1927-жылы америкалык физиктер К.Девиссон (1881-1958) жана Л.Жермер (1896-1971-жж) тарабынан электрондун дифракциясын тажырыйбада байк4ашы менен джалиденди. Кийинчерээк толкундук касиетке башка бөлүкчɵлɵр да ээ болору байкалат.
Ошентип атомдун баштапкы жана акыркы турактуу (станциоалдык) абалына келүүчү чондуктар кирген жаны теориянын керектиги келип чыккан.
19258-ж. Немец физиги В.Гейзенберг (1901-1976-жж.) курамына электрондун кординаты жана ылдамдыгынын ордуна кандайдыр бир абстрактуу алгебралык чондуктар – матирицалар кирген формалдуу схеманы түзгɵн; матрицалардын жана байкалган чондуктардын жана байкалган чондуктардын (энергиянын денгээлдери ж-а кванттык ɵтүүлɵрдүн интенсивдүүлүгү) ортосундагы байланыш жɵнɵкɵй, карама-каршы болбогон эрежелер аркылуу берилген.Гейзенбергдин эмгеги М.Борн (1882-1973-жж.) жана П.Иордан (1902-198-жж.) тарабынан ɵркүндɵтүлгɵн. Матрицалык механика ушинтип пайда болгон. Кванттык механиканы түзүүдɵ ушул мезгилге таандык Дирактын эмгектери да чон ролду ойногон.
1928-жылы англялык физик П.Дирак (1902-198-жж.) тарабынан ɵркүндɵтүлгɵн. Матирицалык механика ушинтип пайда болгон. Кванттык механиканы түзүүдɵ ушул мезгилге таандык Дирактын эмгектери да чон рол ойногон.
1928-ж., англиялык физик П.Дирак (1902-19*84-жж.) электрондун тышкы күчтүк талаадагы кыймылын мүнɵздɵгɵн релятивдик теңдемесин кыска так баяндаган. Кванттык механиканын Дирак сунуш кылган формасы матирицалык кванттык механикага кошулат. Кванттык механика түшүнүгү физикалык негизге жана ийкемдүү математикалык аппаратка ээ болгон илим катарында Гейзенбергдин (1927) аныксыздык катнашын сунуш кылган эмгеги жарык көргөн кийин толгу менен калыптанып бүттү. Аныксыздык катнашы кванттык механиканын теңдемелерин физикалык маанилерин жана алардын классикалык механика менен байланышын ж.б.у.с. кванттык механиканын принциптүү маселелерин сапаттык натыйжаларын ачып көрсɵттү.
Атомдун спектирлерин тыкандык менен талдоонун негизинде (биринчи жолу америкалык физик Ж.Ю.Уленбек (1900-) жана С.Гаудсмит (102-1979-жж.) киргизи, швейцариялык физик В.Паули (1900-1958-жж) тарабынан ѳркүндѳтүлгѳн) электронго зряд менен массадан башка дагы дагы бир мүнѳздѳмѳ – спин түшүнүгү бергилген. Атомдун, малекулаларын, ядронун, катуу заттын теориясында 1925-ж. Паули тарабынан ачылып, фундаменталдык мааниге ээ болгон тыюу салуу принциби чоң ролду ойногон. 1926- ж. Австриялык физик Э.Шредингер (1887-1961-жж.) бул толкундардын тышкы күчтүк талаалардагы абалын жазуучу теңдемени сунуш кылган.Шредингердин толкундук теңдемеси релятивдик эмес кванттык механиканын негизги теңдемеси болуп эсептелинет.
Шредингердин теңдемеси пайда болгондон кийин тез эле толкундук ( Шредгердин теңдемесине негизделген) жана матрицалык механиканын математикалык эквиваленттүүлүгү кѳргѳзүлгѳн. 1926-ж. Борн де Бройлдун толкундарынын ыктымалдуулук чечмеленишин берген.
Текшерүү үчүн суроолор
1.Байыркы дүйнѳдѳгү атомдук окуунун жолдорун атгыла.Алар ким тарабынан сунуш кылынган жана кимдер ѳркүндѳткѳн?
2.Орто кылымдын шартында атом жѳнүндѳ окуу эмне үчүн ѳнүкѳн эмес?
3.Кайра Жаралуу доорунда атом жѳнүндѳ окууда кандай кѳзкараштар пайда болгон?
4. Материянын атомдук түзүлүшү жѳнүндѳ илимгет киргизген М.Ломоносовдун эмгегин баяндагыла?
5.Молекулалык-кинетикалык теориянын ѳнүгүшүнѳ салым жсаган окумуштуулардын эмгектерин баяндагыла?
6.Броун кыймылынын себебин түшүндүргүлѳ?
7.Атом жѳнүндѳ ѳркүндлшүнѳ Д.Менделеевдин салымын мүнѳздѳгүлѳ?
8.Электрдик кубулуштарды үйрѳнүдѳ атом жѳнүндѳ кандай ѳнүккѳн?
9.XIX-XX кылымдардын чегинде атом элементардык бѳлүкчѳ эмес экенин далилдеген фундаменттик физикалык ачылыштарды мүнѳздѳгүлѳ?
10.Катоддук нурлар деген кандай нурлар?
11.Электрондун тачылышынын тарыхын баяндагыла.
12.Атомдун түзүлүшү жѳнүндѳ эң алгачкы моделдерди сүрѳттѳгүлѳ.
13.Резерфорддун моделин жана анын жетишпегендиктерин айткыла.
14.Кванттын энергиясынын формуласын жазып түшүндүргүлѳ.
15.Жарыктын корпускула-толкундук экилтиктүү (дуализм) табиятын түшүндүргүлѳ.
1-БАП
РЕЗЕРФОРД-БОРДУН АТОМУ
§1. Атомдун моделдери
Томсондун атому. Чогулган эксперименталдык малыматтардын негизинде 1902-ж. У.Томсон (лорд Кельвин) атомдун биринчи моделин сунуш кылган. Кельвиндин модели боюнча атом мейкиндиктин кандайдыр бир анча чон эмес , мүмкүн сфера формасындагы аймагында топтолгон он зарядлардан жана анын ичинде өздөрүнүн теӊ салмактуу абалдарынын жанында термелишкен электрондордон турат . Электрондордун суммардык терс заряды атомдордун оӊ зарядына барабар , ошондуктан атом жалпысынан электр бейтарапту . Термелген электрондор Максвеллдин теориясы боюнча жарыкты нурлантыпты керек , ошондуктан дүүлүкпөгөн абалда бул электрондор жана оӊ заряд тынч абалда болуулары керек . Буга чейин , заряддалган бөлүкчөлөрдүн системасы электрдик күчтөрдүн аракети астында гана тынч абалда боло албастыгы белгилүү болгондуктан , заряддардын мындай бөлүштүрүүсү кандайча тынч абалда болору түшүнүксуз болуучу ; бирок атомдун ичинде кандайдыр бир башка күчтөр да аракет этишет деп божомолдоого болот эле .
[Ж.Ж. Томсон бул моделди өркундөтүп , 1903-ж , атом үчүн өзүнүн моделин сунуш кылат . Томсон боюнча атом , ичине теӊ салмактуу абалдарынын тегерегинде термелишкен электрондор жайланышкан , оӊ заряд менен үзгүлдүксүз заряддатлан радиусу болжол менен 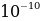 м ге барабар шар түрүндө болот (1.1-сүр.). Жогорудагыдай эле атомдо оӊ заряд электрондордун жалпы терс заряды менен тендешип турат.
м ге барабар шар түрүндө болот (1.1-сүр.). Жогорудагыдай эле атомдо оӊ заряд электрондордун жалпы терс заряды менен тендешип турат.
Томсон оӊ заряд заряддардын системасында электрдик эмес күчтөрдүн





сүрөт
R r
Аракети астында тынч абалда кармалып турат деп божомолдоп , электрондор кандайча жайланышканда тынч абалда болуша тургандыгын изилдеген . Ал электр зарядынын туруктуу жайланышы химиялык активдүү эмес элементтерге. Туруктуулугу анча эмес жайланышуу - активдүүрөк элементтерге тиешелүү болот деген болжомолдоону сунуш кылган . Мунуменен д элементтердин мезгилдик таблицасын
түшүндүргүу келген .
Томсондун атому дүүлүккөндө (мисалы , шамдын жанында ), жеӊил электрондор гана дүүлүгүшүп , оор оӊ заряд тынч абалда калган . Калабы электрондун дал ушул термелүүлөрү байкалган спектрлерди шарттап жана электрондордун ар башка жайланышына атомду мүнөздөөчү спектрдик сызыктардын ар кандай шайкештиги туура келет болуш керек . Атомдор курланткан жарык толкундаарынын өлчөнгөн узундуктарын пайдаланып , Томсон оӊ заряд ээлеген аймакты баалай алган . Томсондун модели классикалык физиканын алкагынан чыкпастан түзүлгөн .
Классикалык элестетүүлөргө ылайык , атом монохроматтык толкунду , качан нурланткан атомдогу электрон гармониялык термелүү жасаганда , демек , теӊ салмактуу абалынын жанында F= - kx түрүндөгү квазисерпилгичтүү күчтүн таасири аркасында кармалып турганда нурланта алмак . Анда бир тектүү заряддалган шардын ичиндеги талаанын чыӊадышы төмөндөгүчө аныкталат:
E(r) = 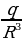 , (1.1)
, (1.1)
Мында q – шардын заряды . R – анын радиусу , r – электрондун теӊ салмактуу абалынан четтенип . Демек , теӊ салмактуу абалынан (шаардын борборунун ) r аралыгында жайланышкан электронго
F=(-e)E= -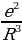 r = - kr (1.2)
r = - kr (1.2)
күчү аркет этет. Мындай шартта кандайдыр бир жол менен теӊ салмактуу абалынан чыгарылган электрон
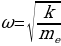 =
= 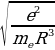 (1.3)
(1.3)
Жыштыгы менен термелүү жасайт , мында е - электрондун заряды , m1 - электрондун массасы , R – атомдун радиусу (1.3) кө ылайык
R = 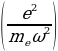 1/3 (1.4)
1/3 (1.4)
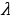 = 6000 A толкун узундугуна (спектердин көрүнгөн аймагы)
= 6000 A толкун узундугуна (спектердин көрүнгөн аймагы) 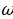
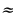
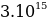 рад/с туура келет. Демек
рад/с туура келет. Демек
R = 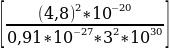 1/3
1/3 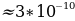 м.
м.
Бирок Томсондун модели кээ бир Физикалык кубулуштарды туура түшүндүргөнү менен кийинчерээк олуттуу карама – каршылыктарга учураган . Ошондуктан атомдун моделин аныктоо аракеттери улантыла берген.
Резерфорддун атому . Атомдун түзүлүшү жөнүндөгү элестетүүлөрдү өнүктүрүүдө Резерфорддун заттардагы  - бөлүкчөсүн изилдөө боюнча жүргүзгөн тажрыйбалары абдан чоӊ мааниге ээ. Нурлануулар же ар кандай бөлүкчөлөрдүн – X – нурлары , электрондор (
- бөлүкчөсүн изилдөө боюнча жүргүзгөн тажрыйбалары абдан чоӊ мааниге ээ. Нурлануулар же ар кандай бөлүкчөлөрдүн – X – нурлары , электрондор (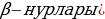 жана
жана  - бөлүкчөлөрдүн заттардан чачыроосу 1910- ж. чейин эле жүргүзүлүп келген . Атомдун түзүлүшүн изилдөө үчүн эӊ ылайыктуусу оор
- бөлүкчөлөрдүн заттардан чачыроосу 1910- ж. чейин эле жүргүзүлүп келген . Атомдун түзүлүшүн изилдөө үчүн эӊ ылайыктуусу оор  – бөлүкчөлөр болгон .
– бөлүкчөлөр болгон .  - бөлүкчөсүнүн массасы болжол менен 6,62*
- бөлүкчөсүнүн массасы болжол менен 6,62*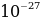 кг , б.а., гелийдин атомунун массасына барабар , анын заряды оӊ жана чондугу боюнча электрондун зарядына караганда эки эсеге чоӊ болору жана радиоактивдүү полонийден бөлүнүп чыккан
кг , б.а., гелийдин атомунун массасына барабар , анын заряды оӊ жана чондугу боюнча электрондун зарядына караганда эки эсеге чоӊ болору жана радиоактивдүү полонийден бөлүнүп чыккан  - бөлүкчөсүнүн ылдамдыгы 1,6*
- бөлүкчөсүнүн ылдамдыгы 1,6*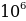 м/с га барабар экендиги белгилүү болгон . Мындан
м/с га барабар экендиги белгилүү болгон . Мындан  – бөлүкчөсү нурлануу процессинде эки электронунан ажыраган гелийдин атому деп болжомолдоого болот. Бул болжоолдоо Резерфорд жана Ройдс тарабынан далилденген . 1911-ж. Резерфорддун сунушу боюнча анын окуучулары Х Гейгер (1882 – 1945-жж.) жана У. Марсден (1889 – 1970-жж.) радиоактиивдүү заттар бөлүп чыгарган
– бөлүкчөсү нурлануу процессинде эки электронунан ажыраган гелийдин атому деп болжомолдоого болот. Бул болжоолдоо Резерфорд жана Ройдс тарабынан далилденген . 1911-ж. Резерфорддун сунушу боюнча анын окуучулары Х Гейгер (1882 – 1945-жж.) жана У. Марсден (1889 – 1970-жж.) радиоактиивдүү заттар бөлүп чыгарган  - бөлүкчөлөрүнүн чачырашын сандык түрдө изилдешкен . Бута катары эсептелген атомдор менен
- бөлүкчөлөрүнүн чачырашын сандык түрдө изилдешкен . Бута катары эсептелген атомдор менен  - бөлүкчөлөрүнүн ортосундагы жекече кагылуушуну мүмкүн болушунча так изилдөө үчүн бутактачасы мүмүкүн болушунча жука болушу керек , антпесе көптөгөн кагылышуулардын натыйжасы жекече кагылышуунун натыйжасы басып кетмек . Мындай тактачаны алтындан жасоого болот . Акырындап жалпайтуу менен калындыгы болгону алтындын 400 атомун кармаган аябагандай жука алтын тактачасы (фольга) даярдалган . Андан соӊ вакуумда жайланышкан бута – тактачасынан
- бөлүкчөлөрүнүн ортосундагы жекече кагылуушуну мүмкүн болушунча так изилдөө үчүн бутактачасы мүмүкүн болушунча жука болушу керек , антпесе көптөгөн кагылышуулардын натыйжасы жекече кагылышуунун натыйжасы басып кетмек . Мындай тактачаны алтындан жасоого болот . Акырындап жалпайтуу менен калындыгы болгону алтындын 400 атомун кармаган аябагандай жука алтын тактачасы (фольга) даярдалган . Андан соӊ вакуумда жайланышкан бута – тактачасынан  - бөлүкчөлөрүнүн чачырашы күкүрттүү- цинк экранында микроскоптун же лупанын жардамы менен байкалган . Экрандын ар кандай бөлүгүн байкоо менен Гейгер бир минута ичинде канча жолу сцинтилляциялар (жылтэтүүлөр) болорун эсептей алган. Бул болсо белгилүү бурч боюнча чачыраган бөлүкчөлөрдүн
- бөлүкчөлөрүнүн чачырашы күкүрттүү- цинк экранында микроскоптун же лупанын жардамы менен байкалган . Экрандын ар кандай бөлүгүн байкоо менен Гейгер бир минута ичинде канча жолу сцинтилляциялар (жылтэтүүлөр) болорун эсептей алган. Бул болсо белгилүү бурч боюнча чачыраган бөлүкчөлөрдүн 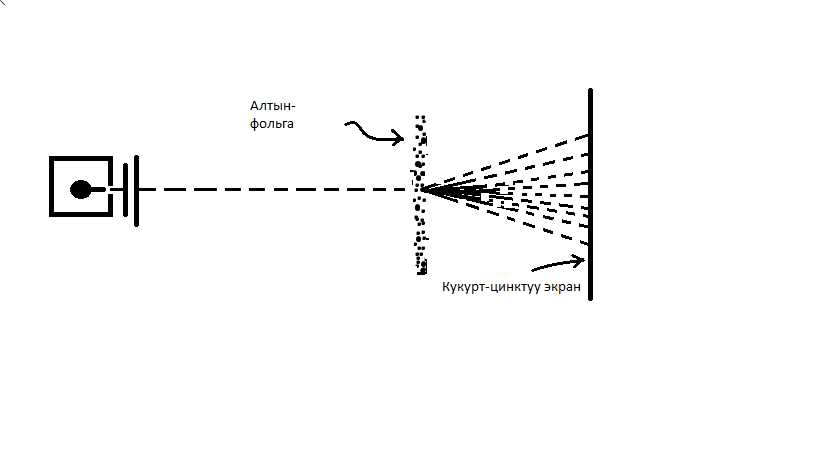 салыштырма санын эсептөөгө мүмкүндүк берген (1.2-сүр.).
салыштырма санын эсептөөгө мүмкүндүк берген (1.2-сүр.).
1.2- сүрөт
Бул тажрыйбадан  - бөлүкчөлөрүнүн басымдуу көпчүлүгү анча чоӊ эмес 1-
- бөлүкчөлөрүнүн басымдуу көпчүлүгү анча чоӊ эмес 1-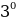 ка барабар бурчка чачыраары аныкталган . Мындай бөлүкчөлөрдүн бурчтук бөлүштүрүлүшү кокустуктуу каталарды мүнөздөгөн Гаусстун (1777-1855-жж.) Ийрлиги менен жакшы сүрөттөлгөн . Бирок , кээ бир
ка барабар бурчка чачыраары аныкталган . Мындай бөлүкчөлөрдүн бурчтук бөлүштүрүлүшү кокустуктуу каталарды мүнөздөгөн Гаусстун (1777-1855-жж.) Ийрлиги менен жакшы сүрөттөлгөн . Бирок , кээ бир  - бөлүкчөлөр 1500 ка жана андан чоӊ бурчтарга чачырай тургандыгы да байкалган . Мындай бөлүкчөлөрдүн салыштырма саны өтө эле аз болгон . Мисалы үчүн калыӊдыгы 1 мкм алтын фольгасы аркылуу өткөндө
- бөлүкчөлөр 1500 ка жана андан чоӊ бурчтарга чачырай тургандыгы да байкалган . Мындай бөлүкчөлөрдүн салыштырма саны өтө эле аз болгон . Мисалы үчүн калыӊдыгы 1 мкм алтын фольгасы аркылуу өткөндө  - бөлүкчөлөрүнүн болжол менен 20 000 ден бири баштапкы багытка салыштырмалуу 1800 ка чейин жеткен бурчка чагылышкан . Тажрыйбалардын жыйынтыгын талдоо менен Резерфорд ,
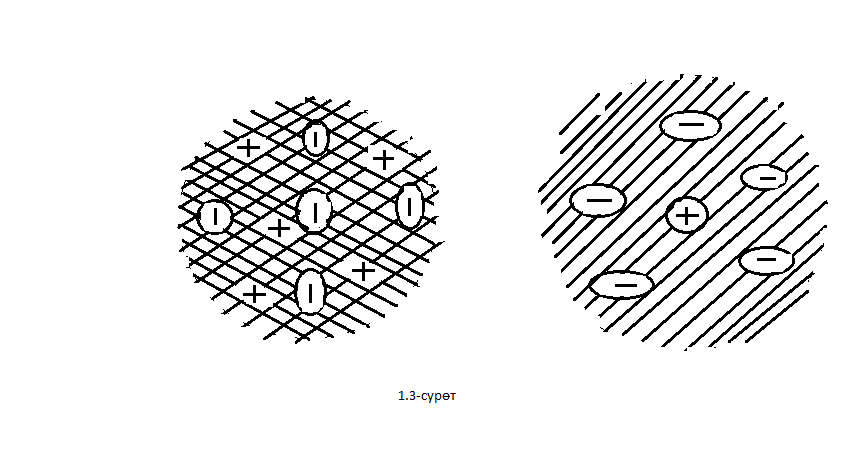
- бөлүкчөлөрүнүн болжол менен 20 000 ден бири баштапкы багытка салыштырмалуу 1800 ка чейин жеткен бурчка чагылышкан . Тажрыйбалардын жыйынтыгын талдоо менен Резерфорд ,  - бөлүкчөлөрдүн баштапкы багыттан мындай күчтүү четтеши , эгерде атомдун ичинде өтө кичине көлөмгө топтолгон чоӊ масса менен байланышкан заряд мүмкүн деген тыянакка келген . Бул тыянакка таянып Резерфорд Томсондун моделинин (1.3.а-сүр.) ордуна өзүнүн ядролук (планетардык ) моделин (1.3.б-сүр.) сунуш кылган . Бул модель боюнча атомду борборунда заряды Ze ге барабар оор , өлчөмү 10-14 м ден чоӊ эмес оӊ ядро жана анын айланасында атом ээлеген бүткүл көлөм боюнча бир калыпта бөлүштүрүлгөн Z электрондор жайланышкан заряддардын системасы катарында кароого болот . Атомдун дээрлик бардык массасы ядродо топтолгон болот.
- бөлүкчөлөрдүн баштапкы багыттан мындай күчтүү четтеши , эгерде атомдун ичинде өтө кичине көлөмгө топтолгон чоӊ масса менен байланышкан заряд мүмкүн деген тыянакка келген . Бул тыянакка таянып Резерфорд Томсондун моделинин (1.3.а-сүр.) ордуна өзүнүн ядролук (планетардык ) моделин (1.3.б-сүр.) сунуш кылган . Бул модель боюнча атомду борборунда заряды Ze ге барабар оор , өлчөмү 10-14 м ден чоӊ эмес оӊ ядро жана анын айланасында атом ээлеген бүткүл көлөм боюнча бир калыпта бөлүштүрүлгөн Z электрондор жайланышкан заряддардын системасы катарында кароого болот . Атомдун дээрлик бардык массасы ядродо топтолгон болот.
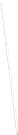
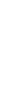


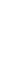

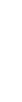
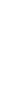
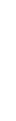
 Резерфорддун тыянагы Вильсондун
Резерфорддун тыянагы Вильсондун
Камерасындагы  - бөлүкчөлөрүнүн издеринин сүрөтүн талдоодо абдан жакшы далилденген . Адатта
- бөлүкчөлөрүнүн издеринин сүрөтүн талдоодо абдан жакшы далилденген . Адатта  - бөлүкчөлөрүнүн издеринин учтары эч кандай өзгөчөлүктөр менен айырмаланышпайт . Бирок кез – кезде издин учтары
- бөлүкчөлөрүнүн издеринин учтары эч кандай өзгөчөлүктөр менен айырмаланышпайт . Бирок кез – кезде издин учтары  түрүндө болгон учурлар байкалат (1.4-сүр.).
түрүндө болгон учурлар байкалат (1.4-сүр.).
Мында  - бөлүкчөсүнүн ядро менен кагылышкан учуру сүрөткө тартылып
- бөлүкчөсүнүн ядро менен кагылышкан учуру сүрөткө тартылып
1.4-сүрөт калган . Кагылышуунун натыйжасында  - бөлүкчөлөрүнүн кыймылынын багыты кескин
- бөлүкчөлөрүнүн кыймылынын багыты кескин
Өзгөрүп , кыймылга келген ядро жаӊы из калтырып , сүрөттө көрүнүп турган  пайда кылышат . Жогоруда келтирилген тыянакка таянып , Резерфорд
пайда кылышат . Жогоруда келтирилген тыянакка таянып , Резерфорд  - бөлүкчөлөрүнүн чачырашынын сандык теориясын иштеп чыккан жана чачыраган бөлүкчөлөрдүн ө бурчунун маанилери боюнча бөлүштүрүлүшүнүн формуласын алган . Бул формуланы алууда Резерфорд төмөндөгүдөй ой жүгүрткөн . Биринчиден
- бөлүкчөлөрүнүн чачырашынын сандык теориясын иштеп чыккан жана чачыраган бөлүкчөлөрдүн ө бурчунун маанилери боюнча бөлүштүрүлүшүнүн формуласын алган . Бул формуланы алууда Резерфорд төмөндөгүдөй ой жүгүрткөн . Биринчиден  - бөлүкчөлөрүнүн баштапкы багытынан четтеши алар менен атомдун ядролорунун ортосундагы кулондук аракет этишүү менен шартталат . Электрондун массасы
- бөлүкчөлөрүнүн баштапкы багытынан четтеши алар менен атомдун ядролорунун ортосундагы кулондук аракет этишүү менен шартталат . Электрондун массасы  - бөлүкчөсүнүн массасына караганда болжол менен 7300 эсеге аз болгондуктан электрон менен аракет этишүү
- бөлүкчөсүнүн массасына караганда болжол менен 7300 эсеге аз болгондуктан электрон менен аракет этишүү  - бөлүкчөсүнүн изинин өзгөрүшүнө салым кошо албайт . Экинчиден , ядронун массасы
- бөлүкчөсүнүн изинин өзгөрүшүнө салым кошо албайт . Экинчиден , ядронун массасы  - бөлүкчөнүн массасына салыштырмалуу чоӊ , ошондуктан ядрону кыймылсыз деп эсептөөгө болот .
- бөлүкчөнүн массасына салыштырмалуу чоӊ , ошондуктан ядрону кыймылсыз деп эсептөөгө болот .  - бөлүкчөлөрүнүн ядронун электр талаасындагы кыймылы Резерфорд тарабынан классикалык физиканын негизинде каралган . Каралган учурда классикалык физиканын колдонулушунун тууралыгы кийинчерээк пайда болгон кванттык механика менен негиздөөгө болот .
- бөлүкчөлөрүнүн ядронун электр талаасындагы кыймылы Резерфорд тарабынан классикалык физиканын негизинде каралган . Каралган учурда классикалык физиканын колдонулушунун тууралыгы кийинчерээк пайда болгон кванттык механика менен негиздөөгө болот .
Резерфорддун тажрыйбасында калыӊдыгы 10-4 – 10-5 см ге барабар абдан жука металл фольгалары пайдаланылган . Ошондуктан бул учурда чоӊ бурчтарга чачыроону караган кезде  - бөлүкчөлөрүнүн атомдун ядролору менен көп жолу кагылышын эске албастан , эӊ кичине аралыкка жакындаган
- бөлүкчөлөрүнүн атомдун ядролору менен көп жолу кагылышын эске албастан , эӊ кичине аралыкка жакындаган  - бөлүкчөсүнүн бир гана ядро менен аракет этишин карасак болот . Ядролор жана атомдун электрондору менен бир нече жолу кагылуушулар чачыроо бурчунун кичине маниилеринде гана кандайдыр бир ролду ойнойт . Мындай бурчтарды биз карабайбыз .
- бөлүкчөсүнүн бир гана ядро менен аракет этишин карасак болот . Ядролор жана атомдун электрондору менен бир нече жолу кагылуушулар чачыроо бурчунун кичине маниилеринде гана кандайдыр бир ролду ойнойт . Мындай бурчтарды биз карабайбыз .  - бөлүкчөсү калган ядролордон бир топ алыс аралыкта учуп өткөндүктөн , алардын ортосундагы аракет этишүү да көӊүлгө алынбайт . Ошентип , Резерфорддун теориясы чечтөө бир ядронун электр талаасы менен шартталып , бул чечтөөгө салыштырмалуу калган бардык чечтөөлөрдү чогуусу менен көнүлгө албай койсо боло турган учурда гана колдонулат . Тиешелүү чачыроо Резерфорддук деп аталат . Чачыроонун натыйжасында
- бөлүкчөсү калган ядролордон бир топ алыс аралыкта учуп өткөндүктөн , алардын ортосундагы аракет этишүү да көӊүлгө алынбайт . Ошентип , Резерфорддун теориясы чечтөө бир ядронун электр талаасы менен шартталып , бул чечтөөгө салыштырмалуу калган бардык чечтөөлөрдү чогуусу менен көнүлгө албай койсо боло турган учурда гана колдонулат . Тиешелүү чачыроо Резерфорддук деп аталат . Чачыроонун натыйжасында  - бөлүкчөсүнүн кинетикалык энергиясы өзгөрбөгүндүктөн , б.а., атомду (атомдун ядросун андан бетер) дүүлүктүрүүгө сарпталбагандыктан , бул чачыроо серпилгичтүү болот .
- бөлүкчөсүнүн кинетикалык энергиясы өзгөрбөгүндүктөн , б.а., атомду (атомдун ядросун андан бетер) дүүлүктүрүүгө сарпталбагандыктан , бул чачыроо серпилгичтүү болот .
 - бөлүкчөсүнүн атомдун ядросунан чачырашы жөнүндөгү маселе планеталардын Күндүн айланасындагы кыймылы
- бөлүкчөсүнүн атомдун ядросунан чачырашы жөнүндөгү маселе планеталардын Күндүн айланасындагы кыймылы
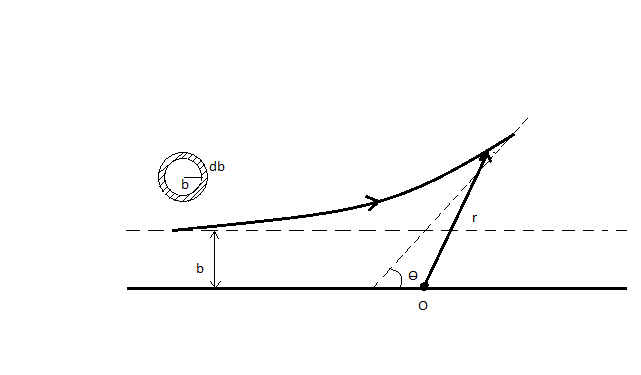
Жөнүндөгү И. Кеплердин (1571-1630-жж.) маселесине окшош . Эки учурда теӊ нерселердин аракет этишүү күчторү борбордук болот жана алардын ортосундагы аралыктын квпдратына тескери пропорционалдуу өзгөрөт . Планеталар учурунда бул тартылуу күчү ,  учурунда - түртүшүү күчү . Натыйжада
учурунда - түртүшүү күчү . Натыйжада  сү (1.5-сүр.) гипербола боюнча кыймылдайт жана чачыроо бурчу θ анын гиперболалык изинин асимптоталарынын ортосундагы бурчуна барабар болот
сү (1.5-сүр.) гипербола боюнча кыймылдайт жана чачыроо бурчу θ анын гиперболалык изинин асимптоталарынын ортосундагы бурчуна барабар болот
ctg 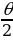 =
=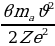 , (1.5)
, (1.5)
мында ma - 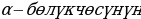 массасы ,
массасы , 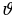 – анын
– анын 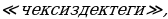 б.а., ядродон алыс жердеги ылдамдыгы , Ze – ядронун заряды , 2е -
б.а., ядродон алыс жердеги ылдамдыгы , Ze – ядронун заряды , 2е -  сүнүн элементардык заряддан эки эсе чоӊ заряды . Z саны ядронун заряддык саны деп аталат . Көпчүлүк учурда бирдик катарында элементардык заряд катары е кабыл алынганын эске алуу менен аны кыскача эле ядронун заряды деп аташат ,
сүнүн элементардык заряддан эки эсе чоӊ заряды . Z саны ядронун заряддык саны деп аталат . Көпчүлүк учурда бирдик катарында элементардык заряд катары е кабыл алынганын эске алуу менен аны кыскача эле ядронун заряды деп аташат , 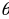 аркылуу мээлөө аралыгы , б.а., ядродон
аркылуу мээлөө аралыгы , б.а., ядродон 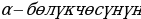 дүүлүкпөгөн түз сызыктуу изине жүргүзүлгөн перпендикулярдык узундугу белгиленет .
дүүлүкпөгөн түз сызыктуу изине жүргүзүлгөн перпендикулярдык узундугу белгиленет .
Атомдук кубулуштардын аймагында (1.5) формуласынын өзү эмес , андан келип чыккан статистикалык натыйжалар эксперимент аркылуу текшерилет . Чачыроонун дифференциалдык эффективдүү кесилиши түшүнүгүн киргизебиз . I аркылуу ядрого учуп келип тийген  сүнүн жалпак жарыш шооласынын интенсивдүүлүгүн , б.а., убакыт бирдиги ичинде агымга перпендикулярдуу бирдик бет аркылуу өткөн
сүнүн жалпак жарыш шооласынын интенсивдүүлүгүн , б.а., убакыт бирдиги ичинде агымга перпендикулярдуу бирдик бет аркылуу өткөн  лөрүнүн санын белгилейбиз . Бул бөлүкчөлөрдүн ичинен агымга перпендикулярдуу do аянтчасы аркылуу dN1 = Ido га барабар
лөрүнүн санын белгилейбиз . Бул бөлүкчөлөрдүн ичинен агымга перпендикулярдуу do аянтчасы аркылуу dN1 = Ido га барабар  сү өтөт . Чачырагандан кийин бул бөлүкчөлөр элементардык dΩ нерселик бурчуна келип тийишет . dΩ нерселик бурчунун чондугу жана анын огунун багыты do аянтцасынын чондугу жана абалы менен аныкталат . Ошондуктан dN1 дин I ге болгон катышы do га барабар жана аянттын өлчөмүнө ээ . Ал ,
сү өтөт . Чачырагандан кийин бул бөлүкчөлөр элементардык dΩ нерселик бурчуна келип тийишет . dΩ нерселик бурчунун чондугу жана анын огунун багыты do аянтцасынын чондугу жана абалы менен аныкталат . Ошондуктан dN1 дин I ге болгон катышы do га барабар жана аянттын өлчөмүнө ээ . Ал ,  лөрдү dΩ нерселик бурчуна чачыратуу үчүн ядронун дифференциалдык эффективдүү кесилиши деп аталат . Бул түшүнүк
лөрдү dΩ нерселик бурчуна чачыратуу үчүн ядронун дифференциалдык эффективдүү кесилиши деп аталат . Бул түшүнүк  сүнүн эле эмес , каалагандай бөлүкчөлөрдүн чачырашына жана бөлүкчөлөр катышкан башка процесстерге да колдонулат . Ошентип , аныктама боюнча
сүнүн эле эмес , каалагандай бөлүкчөлөрдүн чачырашына жана бөлүкчөлөр катышкан башка процесстерге да колдонулат . Ошентип , аныктама боюнча
Dσ = 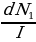 (1.6)
(1.6)
Б.а., атом убакыт бирдиги ичинде dΩ нерселик бурчуна чачыраткан бөлүткүчтөрдүн санынын келип түшкөн бөлүкчөлөрдүн интенсивдүүлүгүнө болгон катышы чачыроонун дифференциалдык эффективдүү кесилиши болот .
Эми  лөрүнүн атомдун жекече ядросунан чачыроосу үчүн дифференциалдык кесилишти карайбыз . мында , чачыроонун натыйжасында
лөрүнүн атомдун жекече ядросунан чачыроосу үчүн дифференциалдык кесилишти карайбыз . мында , чачыроонун натыйжасында  сү кандай чондуктагы dσ аянтчасы аркылуу өткөндө dΩ нерселик бурчунун ичине келип түшөөрүн аныкташыбыз керек болот . X огу катары
сү кандай чондуктагы dσ аянтчасы аркылуу өткөндө dΩ нерселик бурчунун ичине келип түшөөрүн аныкташыбыз керек болот . X огу катары 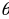 = 0 мээлөө аралыгы туура келген
= 0 мээлөө аралыгы туура келген  сүнүн түз сызыктуу изин алабыз (мындай бөлүкчө ядро менен бетме-бет кагылышмак ). Цилиндрдик симетрияны пайдаланып , жөнөкөйлүк үчүн dσ ны агымга перпендикулярдуу шакектик аянтчага алмаштырабыз dσ = 2
сүнүн түз сызыктуу изин алабыз (мындай бөлүкчө ядро менен бетме-бет кагылышмак ). Цилиндрдик симетрияны пайдаланып , жөнөкөйлүк үчүн dσ ны агымга перпендикулярдуу шакектик аянтчага алмаштырабыз dσ = 2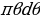 . Мындай аянтчанын ички радиусу
. Мындай аянтчанын ички радиусу 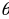 га , тышкысы
га , тышкысы 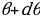 га барабар , ал эми борбору X – огунда жайланышат (1.5-сүр. Үстүндө сол жакта ).
га барабар , ал эми борбору X – огунда жайланышат (1.5-сүр. Үстүндө сол жакта ). 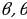 + d
+ d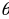 интервалына чачыроо бурчунун θ, θ +dθ интервалы туура келет (1.5) формуласы боюнча
интервалына чачыроо бурчунун θ, θ +dθ интервалы туура келет (1.5) формуласы боюнча
d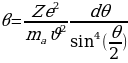
шакектик аянтча аркылуу өткөн  лөрү чачырагандан кийин келип түшкөн dΩ = 2
лөрү чачырагандан кийин келип түшкөн dΩ = 2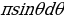 нерселик бурчун киргизип төмөндөгүнү оӊой эле алабыз :
нерселик бурчун киргизип төмөндөгүнү оӊой эле алабыз :
dσ = 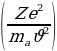 2
2 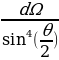 (1.7)
(1.7)
Бул түрдө (1.7) формуласы шакектик эле эмес , калагандай элементардык бет dσ үчүн жарактуу болот . Бул формула Резерфорддун формуласы деп аталат.
Эми (1.7) формуласын экспериментте текшерсе боло тургандай түргө келтиребиз . Ар башка атомдордун  лөрүн чачыратуусу бири-биринен көзкаранды болбойт. Мындан бирдик көлөмдөгү ядорлордун (атомдордун) саны n болсо , анда V көлөмү убакыт бирдиги ичинде dΩ нерселик бурчуна чачыраткан
лөрүн чачыратуусу бири-биринен көзкаранды болбойт. Мындан бирдик көлөмдөгү ядорлордун (атомдордун) саны n болсо , анда V көлөмү убакыт бирдиги ичинде dΩ нерселик бурчуна чачыраткан  лөрүнүн саны
лөрүнүн саны
dN = nVIdσ = nVI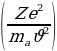 2
2 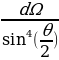 (1.8)
(1.8)
туюнтмасы менен аныкталат . Мына ушул түрдө Резерфорддун формуласы тажрыйбада далилденген . Атап айтканда , тажрыйбадан dΩ турактуу болору, б.а., (1.8) формуласынан көрүнүп тургандай чачыроо бурчу θ дан көзкаранды болбой тургандыгы көргөзүлгөн .
Резерфорддун формуласынын тажрыйбада далилденишин  лөрүнүн жана аны менен аракет этишкен ядролордун борборлору жакындай ала турган кичине аралыктарда Кулондун закону орун ала тургандыгынын кыйыр далилдөөсү катары кароого болот .
лөрүнүн жана аны менен аракет этишкен ядролордун борборлору жакындай ала турган кичине аралыктарда Кулондун закону орун ала тургандыгынын кыйыр далилдөөсү катары кароого болот .
 сү менен атомдун ядросунун ортосунда кулондук аракет этишүү орун ала тургандыгына таянган теориянын тууралыгы баштапкы кыймылынын багытына карама – каршы багытка чагылышкан
сү менен атомдун ядросунун ортосунда кулондук аракет этишүү орун ала тургандыгына таянган теориянын тууралыгы баштапкы кыймылынын багытына карама – каршы багытка чагылышкан  лөрү дагы атомдун ядросунун аймагына кире албай тургандыгын күбөлөйт . Ушуну менен бирге эле ядронун дал өзүн көздөй учуп келе жаткан
лөрү дагы атомдун ядросунун аймагына кире албай тургандыгын күбөлөйт . Ушуну менен бирге эле ядронун дал өзүн көздөй учуп келе жаткан  сү анын борборуна кандай эӊ кичине аралыкка жакындай ала тургандыгын
сү анын борборуна кандай эӊ кичине аралыкка жакындай ала тургандыгын  сүнүн кинетикалык энергиясын бөлүкчө толугу менен токтогон моменттеги
сүнүн кинетикалык энергиясын бөлүкчө толугу менен токтогон моменттеги  сү менен ядронун ортосундагы аракет этишүүнүн потенциалдык энергиясына бараборлоо менен тапсак болот :
сү менен ядронун ортосундагы аракет этишүүнүн потенциалдык энергиясына бараборлоо менен тапсак болот :
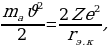 (1.9)
(1.9)
Мында 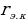
 сү менен ядронун борборлорунун ортосундагы эӊ кичине аралык . Мындан
сү менен ядронун борборлорунун ортосундагы эӊ кичине аралык . Мындан
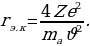 (1.10)
(1.10)
Эгерде Z = 30 , 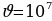 м/c ,
м/c , 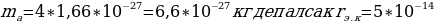 м болот .
м болот .
Мындан көп өтпөй эле борбордук ядронун электрдик заряды (тактап айтканда , чондугу ядронун курамындагы электрондордун суммардык зарядына барабар оӊ заряддын саны) Менделеевдин мезгилдик системасындагы берилген элементтин номерине так дал келери аныкталган . 1913- ж башында бул ой голандиялык физик А.Ван-дер-Брук (1870-1926-жж.) тарабынан айтылган жана бир нече ай кийин Резерфорддун жаш окуучусу Г.Мозли (1887 – 1915-жж.) тарабынан тажрыйба жүзүндө далилденген . Мозли ар башка элементтерге мүнөздүү рентген нурларынын спектрин изилдеген . Көрсө , бул нурлардын толкун узундуктары элементтин мезгилдик системадагы 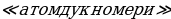 Z өскөн сайын системалуу түрдө азаят экен . Мындан , Мозли бул законченемдүүлүк атомдун зарядынын
Z өскөн сайын системалуу түрдө азаят экен . Мындан , Мозли бул законченемдүүлүк атомдун зарядынын 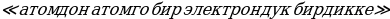 чоӊоюшу менен шартталат жана мындай бирдиктердин саны
чоӊоюшу менен шартталат жана мындай бирдиктердин саны 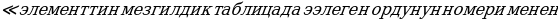
Дал келет 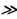 , - деген тыянакка келет .
, - деген тыянакка келет .
Экинчи жагынан , атом электрдик бейтараптуулукка ээ, демек электрондордун терс заряды ядронун оӊ зарядын жоюшу керек . Бул болсо , атомдогу электрондордун толук саны да Z ке барабар дегенди билгизет . Ошентип , Резерфорд атом Күн системасына окшош деген тыянакка келет . өлчөмү 10-14 м ге барабар ядро , борбордук жарык берүүчү - Күнгө окшош , ал эми электрондор орбиталары атомдун өлчөмдөрүндөй , б.а., 10-10 м болгон планеталардын ролун ойнойт . Күн системасынан аыйрмаланып , атомдо ядронун оӊ заряды +Ze электрондук булутчанын заряды -Ze менен жоюшат , ал эми гравитация учурунда эч кандай жоюшуу болушу мүмкүн эмес . Атомдун планетардык модели кийинчерээк көптөгөн жолу далилденип , жалпы кабыл алууга ээ болду .
Резерфорд атомдун планетардык моделин түзүп , илимге зор салым кошту . Анын моделинин сүрөтү XX кылымдын эмблемасы болуп эсептелет . Чындыгында электрондордун орбиталарынын болбой тургандыгы кийинчерээк белгүлүү болду . Бирок ошого карабастан , кванттык механиканы түзүүдө негиз болуп калган Резерфоддун модели тарыхый мааниге ээ.
Атомдун планетардык моделинин көптөгөн ийгилигине карабастан , аны классикалык физиканын негизинде түшүндүрүү өтө кыйын болгон . Атап айтсак , планетардык модель классикалык механиканын жана электдинамиканын закондоруна каршы болот . Кыймылсыз заряддардын системасы туруктуу абалда боло албай тургандыгына байланыштуу , Резерфорд атомдун статистикалык моделинен баш тартып , электрондор ядронун айланасында ийри из боюнча кыймылдашат деп божомолдоого мажбур болгон . Бирок , бул учурда электрон ылдамданууга ээ болуу менен кыймылдайт да , классикалык электрдинамиканын жоболоруна ылайык , ал электрмаггниттик (жарык) толкундарын үзгүлтүксүз нурлантышы керек . Нурлантуу процесси энергиянын жоготулушу менен коштолуп , акырында электрон ядрого түшүп калмак (1.6-сүр). Электрондун өзүнүн орбитасынан ядрого түшүп калуу убактысы болгону секунданын миллиарддан бир бөлүгүн түзөт . Бирок мунун бардыгы күндө көрүп жүргөн заттын атомунун туруктуулугу жөнүндөгү элестетүүбүзгө карама – каршы келет . Буга кошумча , электрондун ядрого түшүп келе жаткандыгы нурлантуусу үзгүлтүксүз болмок жана анын жыштыгы электрондун орбитасынын радиусу кичирейген сайын өсмөк жана атомдун спектри туташ тилке түрүндө болмок . Бирок ар бир атомго мүнөздүү спектр дискреттүү болору экспериметтен белгилүү бол-
уп , ал XIX кылымдагы ар кандай затты химиялык талдоонун негизи
болгон.
1.6-сүрөт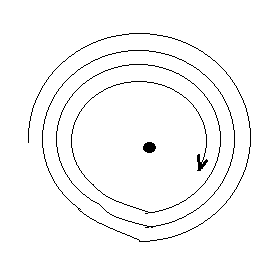
Жогоруда айтылгандардын негизинде атомдун Резерфорд сунуш кылган модели таза классикалык жоболорду колдонуу менен атом дүйнөсүн изиилдөөгө кошулган акыркы салым болгон десек жаӊылышпайбыз
§ 2. Атомдун спектрлериндеги
Законченемдүүлүктөр
И.ньютон кадимки ак жарыкты айнек призмасы аркылуу өткөзгөндө түзүүчүлөргө ажырап спектрди берерин көргөзгөн . Жарыктын ар кандай булактары , жалпысынан алганда , ар башка спектрге ээ болот . Эӊ эле жөнөкөй учурда , жарык буллагынан чыккан белгилүү толкун узундугу 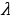 га ээ түстүү нур призмаддан сынгандан кийин эч кандай спектр байкалбайт . Болгону экранда берилген толкун узундугуна тиешелүү жарыктанган ичке тилке байкалат .
га ээ түстүү нур призмаддан сынгандан кийин эч кандай спектр байкалбайт . Болгону экранда берилген толкун узундугуна тиешелүү жарыктанган ичке тилке байкалат .
Ысыган катуу заттар чыгарган нурлануу туташ спектрди берет. Газдарда (туташ аймак менен бирге) сызыктуу жана тилкелүү спектрлар байкалат . Сызыктуу спектр законченемдүү түрдө жайланышкан аздыр – көптүр ичке түзүлүшкө ээ бир катар спектрдик сызыктардан турат . Тилкелүү спектрди жөн көз же ажыратуу жөндөмдүүлүгү кичине спектроскоп менен карагнда тилкелер туташтай болуп көрүнөт , бирок , жогорку ажыратуу жөндөмтүүлүгүнө ээ спектрдик куралды колдонгондо тилкелер бири – бирине тыгыз жайланышкан көптөгөн спектрдик сызыктан турары көрүнөт .
XX кылымдын башында газдардын сызыктуу спектрлери атомдор жана иондор , ал эми тилкелүүлөрү – молекулар тарабынан чыгарылары белгилүү болгон . Ошондуктан аларды атомдук жана молекулалык спектрлер деп да аташат . Суутектин атомунун спектрин вакуумдук суутектик түтүктө электр разряды жүргөн кезде , качан гана молекулаларынын басымдуу көпчүлүгү атомдорго ажыраганда байкай алабыз .
Атомдун көптөгөн спектрдик сызктарга ээ болушу , алардын ички түзүлүшүнүн татаалдыгын көргөзөт . Ошондуктан спектрлерди талдоодо чогулган эмпирикалык көп материалдар XX кылымда атомдун түзүлүшү жөнүндөгу теориянын өнүгүшүнүн негизи болгон .
Спектрдеги спектрдик сызыктын абалы толкун узундугу 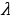 же жыштык v = c/
же жыштык v = c/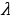 менен мүнөздөлөт . Жыштык спектрдик законченемдүүлүктөрдү туюнтууга ыӊгайлуурак , бирок аны эсептеп чыгуу үчүн жарыктын ылдамдыгы с ны жогорку тактыкта билүүбүз керек . Толкун узундугу
менен мүнөздөлөт . Жыштык спектрдик законченемдүүлүктөрдү туюнтууга ыӊгайлуурак , бирок аны эсептеп чыгуу үчүн жарыктын ылдамдыгы с ны жогорку тактыкта билүүбүз керек . Толкун узундугу 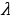 спектрдик куралдын жардамы менен эӊ жогорку тактыкта , үтүрдөн кийинки жетинчи жана андан да жогорку ондук белгиге чейин өлчөнөт . Ошондуктан v нун ордуна спектроскопияда спектроскопиялык толкундук сан деп аталган
спектрдик куралдын жардамы менен эӊ жогорку тактыкта , үтүрдөн кийинки жетинчи жана андан да жогорку ондук белгиге чейин өлчөнөт . Ошондуктан v нун ордуна спектроскопияда спектроскопиялык толкундук сан деп аталган 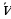 колдонулат .
колдонулат . 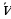 вакуумда 1 см узундукка туура келген толкундун санын көргөзө :
вакуумда 1 см узундукка туура келген толкундун санын көргөзө :
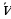 = 1/
= 1/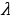 * (1.11)
* (1.11)
Cпектрлерди изилдөө 1860 – ж. немец окумуштуулары Г.Кирхгоф (1824 – 1887 – жж.) жана Р.Бунзендин (1811 – 1899)-жж.) Cпектрди байкоонун жардамы менен химиялык талдоо жүргүзүү аттуу эмгегинин жарык көрүшү менен башталган . Кийинки жылдарда атомдук спектрлерди изилдөөлөр күчөгөн .
Акырындап атомдук спектрлер баш ийген законченемдүүлүктөр табылы баштаган . 1855 – ж . швейцариялык физик , орто мектептин мугалими И.Бальмер (1825 – 1898 – жж.) суутектин спектринин көрүнүүчү аймагында жайланышкан , шарттуу түрдө 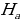 ,
, 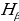 ,
, 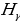 жана
жана 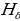 деп белгиленген сызыктардын толкун узундуктарынын ортосунда төмөндөгүдөй жөнөкөй формула
деп белгиленген сызыктардын толкун узундуктарынын ортосунда төмөндөгүдөй жөнөкөй формула
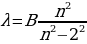 (1.12)
(1.12)
Менен туюнтулган катнаш бар экендигин аныктаган , мындан n – 3,4,5,6 га барабар бүтүн сан , B = 364,70 нм ге барабар турактуу чоӊдук . Бальмердин бул формуласы аны толкун узундугу аркылуу эмес , жарык термелүүсүнүн жыштыгы аркылуу жазганда айкыныраак болот . Жарык толкунун жыштыгы төмөндөгүгө барабар
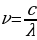 , (1.13)
, (1.13)
Мында с – жарыктын вакуумдагы ылдамдыгы . Бальмер боюнча
_________________________
Азыркы учурда жарык термелүүлөрүнүн жыштыгы сызыктуу эмес оптиканын ыкмаларын колдонуу менен спектроскопияда толкундун узундугун өлчөөгө караганда жогорку тактыкта өлчөӊөт . Ошондуктан спектроскопияда 1/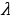 же с/
же с/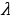 ны колдонуунун принципиалдык айырмасы жок . Спектроскопияда жыштыкты жана спектрдик толкундук санды бир эле v тамгасы менен белгилөө кабыл алынган . Түшүнбөстүктөр болбос үчүн биз жыштыкты v, ал эми спектрдик толкундук санды
ны колдонуунун принципиалдык айырмасы жок . Спектроскопияда жыштыкты жана спектрдик толкундук санды бир эле v тамгасы менен белгилөө кабыл алынган . Түшүнбөстүктөр болбос үчүн биз жыштыкты v, ал эми спектрдик толкундук санды 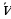 аркылуу белгилейбиз . Дегинкисинен айтканда
аркылуу белгилейбиз . Дегинкисинен айтканда 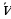 нун ордуна 1/
нун ордуна 1/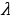 белгилөөсүн колдонуу ыӊгайлуурак .
белгилөөсүн колдонуу ыӊгайлуурак .
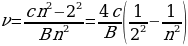 . (1.14)
. (1.14)
Бальмердин ачылшы атомардык суутекти изилдөөгө кызыгууну күчөттү . 1906 – ж . Америкалык физик Т.Лайман (1879-1949-жж.), Ф.Бреккет (1879-1949-жж.), америкалык физик А.Пфунд (1865-1947-жж.) жана башкалар инфракызыл аймакта жайланышкан жаӊы серияларды ачышкан. Ар бир аймактагы спектрдик сызыктардын жыштыктары үчүн туура келген Бальмердин формуласына окшош өзүнчө формулалары бар экендиги аныкталган . Эгерде R = 4с/В белгилөосүн киргизсек , анда Бальмердин төмөндөгүдөй формуласы
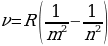 (1.15)
(1.15)
Каалагандай серия үчүн колдонулат, мында m жана n бүтүн сандар жана nm . Бул формула ушундай түрдө швед физиги И.Ридберг (1854 – 1919 – жж.) тарабынан жазылган жана R = 3,29*1015 с-1 турактуусу Ридбергдин турактуусу деп аталат .
Ушуга окшоп зааконченемдүүлүктөр башкача элементтердин , атап ииайтсак , жегич металдардын спектрлерине да табылган .
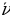 =
= 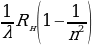 , n = 2,3,4,…. (1.16)
, n = 2,3,4,…. (1.16)
Мында R н = 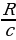 суутектин атому үчүн Ридбергдин турактуусу
суутектин атому үчүн Ридбергдин турактуусу
(Rн = 109678,76 см -1), m =1
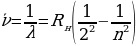 , n = 3,4,5,… (1.17)
, n = 3,4,5,… (1.17)
Формуласы менен мүнөздөлгөн суутектин атомунун спектриндеги Бальмердин сериясы 1.7 – сүрөтүндө көргөзүлгөн . 1- таблицада Бальмердин сериясынын биринчи тогуз сызыгы үчүн толкун узундуктардын байкалган жана эсептелген маанилери келтирилген . өлчөө абада жүргүзүлдүктөн (1.17) формуласы боюнча эсептөөлөр аба үчүн түзөтүүлөрдү киргизүү жүргүзүлдү . Таблицадан (1.17) формуласы өтө жогорку тактыкта тажрыйба менен дал келери көрүнүп турат .
1-1-таблица
Суутектин бальмердик сериясынын толкун узундуктары
| n
| Бел- гиле- ниши
|
|
n | Бел- гиле- ниши
|
| ||
| Эсептел- гени | Байкал-ганы | Эсептел- гени | Байкал-ганы | ||||
| 3 |
| 656,279 | 656,285 | 8 |
| 388,905 | 388,906 |
| 4 |
| 486,133 | 486,132 | 9 |
| 383,539 | 383,540 |
| 5 |
| 434,047 | 434,046 | 10 |
| 379,790 | 379,791 |
| 6 |
| 410,174 | 410,173 | 11 |
| 377,067 | 377,065 |
| 7 |
| 397,008 | 397,007 |
|
|
|
|
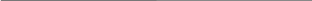
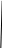
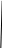
























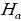
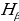
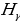
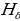
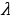 = 653,3 481,1 434,0 410,2 364,7 нм
= 653,3 481,1 434,0 410,2 364,7 нм
1.7 – сүрөт
Пашендин сериясы үчүн
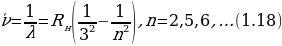
Бул серияны 1908 – ж. комбинациялык принциптин негизинде швейцариялык физик В.Ритц (1878 – 1909- жж.) алдын ала айткан . Бул сериянын сызыктарынын бардыгы Бальмердин сериясы дагы комбинациялоо жолу менен алынат . Каралган серия ушул эле жылы Пашен тарабынан ачылат .
Брекеттин сериясы :
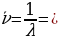
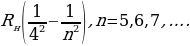 (1.19)
(1.19)
Пфунддун сериясы :
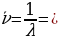
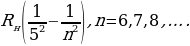 (1.20)
(1.20)
Бул сериялар тиешелүү түрдө 1922-ж. жана 1924-ж. ачылган . Брекеттин сериясы комбинациялоо жолу менен Пашендин , ал эми Пфунддун сериясы – Брекеттин сериясындагы сызыктардан алынат .
Лаймандын сериясы үчүн эӊ чоӊ толкун узундугу n = 2 учуруна тура келет . Ал 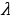 = 4/3Rн = 121,56713 нм ге барабар . Буга тиешелүү сызык суутектин резонанстык (күчөнүү) сызыгы деп аталат . Эӊ чон жыштык (толкундук сан ) (1.16) – (1.19) формулалары боюнча n =
= 4/3Rн = 121,56713 нм ге барабар . Буга тиешелүү сызык суутектин резонанстык (күчөнүү) сызыгы деп аталат . Эӊ чон жыштык (толкундук сан ) (1.16) – (1.19) формулалары боюнча n = 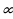 болгое учурда алынат . Бул жыштык сериянын чегарасы деп аталат . Мисалы , Бальмердин сериясы үчүн сериянын чегарасы төмөндөгүгө барабар:
болгое учурда алынат . Бул жыштык сериянын чегарасы деп аталат . Мисалы , Бальмердин сериясы үчүн сериянын чегарасы төмөндөгүгө барабар:
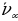 =
= 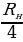 = 27419,69 см-1 же
= 27419,69 см-1 же 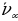 =
= 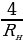 = 364,70142 нм.
= 364,70142 нм.
Чегарага жакындаган сайын спектрдик сызыктардын сериясы тыгыздала баштайт жана алардын ортосундагы толкун узундуктардын айырмасы асимптотикалык түрдө нөлгө умтулат , бул учурда сызыктардын интенсивдүүлүктөрү да нөлгө умтулат . Бул законченемдүүлүк суутектин эле спектрдик сериясында эмес , башка элементтердин спектрдик серияларында да байкалат . Мында , ары жагында туташ спектр башталган чегара да орун алат.
§3. Бордун постулаттары
§ 2 де сериялар үчүн келтирилген формулалар эмпирикалык жол менен тандалып алынганына жана тажрыйбада өтө жогорку тактыкта далилденгендигине карабастан теориялык негизге ээ болушкан эмес . Жогоруда келтирилген сериялык формулалардын түрлөрү , аларда бүтүн сандардын укмуштуудай кайталанышы , Ридбергдин турактуусунун универсаалдулугу табылган законченемдүүлүктөр өтө терен физикалык мааниге ээ экендигин жана аны чечмелөө классикалык физиканын алкагында мүмкүн эместигин күбөлөйт .
Атомдун жаӊы сапатка ээ – кванттык - теориясын түзүүнүн биринчи аракетин 1913 – ж. Н.Бор жасаган . Бор сызыктуу спектрлердин эмпирикалык законченемдүүлүктөрүн , Резерфорддун ядролук моделин жана жарыкты нурлантуунун жана жутуунун кванттык мүнөзүн бириктирүүгө аракет кылып , Төмөндөгүдөй үч постулатты сунуш кылат .
Бордун биринчи постулаты (туруктуу абалдардын постулаты ):
Электрондор атомдо мүмкүн болгон классикалык орбиталардын ичинен белгилүү радиуска ээ орбиталар боюнча гана кыймылдай алышат .
Станционарду же туруктуу деп аталган бул орбиталарда электрондун импульсунун моменти h/(2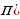 ге эселүү болот (орбиталардын радиусун кванттоо шарты) :
ге эселүү болот (орбиталардын радиусун кванттоо шарты) :
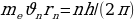 , (1.21)
, (1.21)
Мында me - электрондун массасы 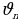 – n- орбитадагы анын ылдамдыгы,
– n- орбитадагы анын ылдамдыгы, 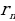 – n –орбитанын радиусу, n – бүтүн (n = 1,2,3,…) маанилерге ээ кванттык сан , h – планк турактуусу .
– n –орбитанын радиусу, n – бүтүн (n = 1,2,3,…) маанилерге ээ кванттык сан , h – планк турактуусу .
Электрон стационардуу орбиталар боюнча кыймылдаганда энергияны нурлантпай (жутпайт).
Электрон бир стационардуу абалдан экинчисине өткөндө , энергиясы тиешелүү стационардык абалдардын энергияларынын айырмасына барабар
h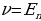 -
-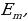 (1.22)
(1.22)
бир фотон бөлүнүп чыгат (жыштыктар шарты ), мында 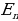 жана
жана 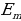 тиешелүү түрдө атомдун нурлантканга (жутканга) чейинки жана кийинки энергиялары
тиешелүү түрдө атомдун нурлантканга (жутканга) чейинки жана кийинки энергиялары 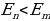 болгондо атом фотонду нурлантат (атом энергиясы чоӊ абалдан энергиясы кичине абалга , б.а., электрон ядродон алысыраак жайланышкан орбитадан жакыныраак жайланышкан орбитага өткөндө ),
болгондо атом фотонду нурлантат (атом энергиясы чоӊ абалдан энергиясы кичине абалга , б.а., электрон ядродон алысыраак жайланышкан орбитадан жакыныраак жайланышкан орбитага өткөндө ), 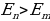 болгондо атом фотонду жутат (атом энергиясы чоӊ
болгондо атом фотонду жутат (атом энергиясы чоӊ
_________________________
Латындын postulatum- талап кылынган деген сөзүнөн . Постулат деп , илимий теорияны түзүү үчүн негиз катары алынган , далилдөөсүз кабыл алынган ырастама айтылат .
абалга , б.а., электрон ядродон алысыраак жайланышкан орбитага өткөндө ) Кванттык өтүүлөрдүн мүмкүн болгон дискреттүү 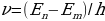 жыштыктарынын топтому атомдун сызыктуу спектрин аныктайт.
жыштыктарынын топтому атомдун сызыктуу спектрин аныктайт.
§ 4. Франк жана Герцтин тажрыйбасы
Атомдордун энергиялары дискреттүү маанилерге ээ боло тургандыгын 1913 – ж. Франк жана Г.Герц электрондор менен атомдордун кагылышууларын кармоочу потенциал ыкмасы аркылуу изилөө менен далилдешкен . Бул тажрыйбалардын принциптик схемасы 1.8 – сүрөтүндө көргөзүлгөн .
Б балонунда 102 Па басым
астында сымаптын буусу кармалып турат . Ысытылган К катоду менен С торчосунун ортосундагы потенциалдардын айырмасы (чыӊалуу) U1 V вольтмери менен өлчөнөт. U1 ди П патонциометринин жардамы менен өзгөртүүгө болот ; С торчосу менен А электродунун (анод) ортосундагы анча чоӊ эмес мааниге ээ утурлоочу потенциалдарынын айырмасы 0,5
1.8 – сүрөт В ко барабар . Катод бөлүп
чыгарган электрондор КС мейкиндигинде чыӊалуусу U1 ге
барабар электр тааласы менен ылдамтылат да , А электродун көздөй кыймылдашат да, А электродун көздөй кыймылдашат . Эгерде торчо аркылуу учуп өтүп бараткан кездеги электрондордун кинетикалык энергиясы 0,5 эВ тон чоӊ болсо , анда алар U2 = 0,5 В ко барабар токтотуучу чыӊалуунун аракетин женип , А электродуна жетишет да , чынжырда ток жүрө баштайт . Бул ток күчү G гальванометри менен өлчөнөт .
Гальванометрдеги ток күчү IG нын U1 ден көзкарандылыгы-


15 U1,B
IG
нын Франк – Герц тарабынан алынган графиги 1.9 – сүрөтүндө көргөзүлгөн . U1 чыӊалуусун нөлдөн баштап чонойткондо , ток күчү башында өсө баштайт да, андан соӊ U1 = 4,9 В ко жеткенде кескин төмөндөйт . U1 ди андан ары чоӊойтсок IG ток күчү кайтадан өсө баштайт да , U1 = 24,9В = 9,8В болгондо кайтадан кескин тө –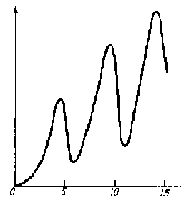
1.9-сүрөт
мөндөйт ; андан соӊ IG нын төмөндөшү U1 = 34,9В = 14,7В то байкалат ж.б.у.с. Графиктеги жанаша максимумдардын ортосундагы аралык U1 дин 4,9 В ко өзгөрүшүнө туура келет (1.9-сүр). 1В ко барабар потенциалдардын айырмасы электронго 1 эВ ко барабар кинетикалык энергия берерин эске сала кетебиз , демек U1 дин 4,9 В ко көбөйүшү электрондун кинетикалык энергиясынын 4,9 эВ ко чоноюшуна туура келет.
Графиктин мындай мүнөзү , электрондор (торчону көздөй учуп бара жаткан) сымаптын атомдору менен кагылышканда , алар энергиянын чоӊдугу 4,9 В ко барабар дискреттүү үлүшүн гана жутаары менен түшүндүрүлөт .
Электрондордун энергиясы 4,9 В тон кичине (U1 серпилггичтүү болот да , электрондордун кинетикалык энергиялары иш жүзүндө өзгөрбөйт . Мындай кагылышууларда атомдун ички энергиясы да өзгөрбөйт . Натыйжада электрондор С торчосуна токтотуучу потенцмалдардын айырмасы U2 ни жеӊгенге жеткидей энергия менен келип жетет . Ошондуктан U1 дин өсүшү IG нын өсүшү менен коштолот .
Качан U1 4,9 В ко жеткенде , торчого учуп жеткен электрондордун энергиясы 4,9 эВ ко барабар болот. Бул учурда электрондор менен атомдордун кагылышуулары серпилгичүү эмес болур калат да , электрон өзүнүн энергиясынын баарын (4,9 эВ) сымаптын атомуна берет , себеби сымаптын атому энергиянын мындай үлүшүн алууга жөндөмдүү болот . Бул учурда атом жакынкы дүүлүккөн абалга (б.а., жакынкы жогорку энергиялык деӊгээлге ) өтөт , ал эми кинетикалык энергиясын жоготкон электрон А электрондоруна чейин жетпей калат . Ошентип , А электродуна чейин атомдор менен серпилгичтүү кагылышкан электрондор гана келип жетет . Натыйжада А электродуна келип жеткен электрондордун саны азаят , б.а., IG ток күчү кескин кичирейип , графикте биринчи максимумдун пайда болушун шарттайт .
U1 чыналуусунун мааниси , серпилгичтүү эмес кагылуушуга катышкан электрондордун жетишерлик саны токтотуучу потенциалдардын айырмасы U2 ни женгендей чондукка жеткенде Ic ток күчү кайтадан өсө баштайт . Бирок U1 = 9,8 В болгон учурда , электрон биринчи серпилгичтүү эмес кагылышуудан кийин (К дан С га чейинки жолдун ортосунда) торчого чейин учуп жеткиче атом менен экинчи жолу серпилгичтүү эмес кагылышканга жеткидей энергияга (4,9 эВ) ээ болот . Мындай серпилгичтүү эмес кагылышууга катышкан электрондор А электродуна жете алышпайт , натыйжада IG кайтадан кескин төмөндөйт . Графиктеги экинчи максимумдун пайда болушу ушуну менен түшүндүрүлөт . Кийинки максимумдардын пайда болушун (U1 = 14,7 В ж.б.) ушуга окшош эле түшүндүрсөк болот .
Дүүлүккөн атомдор мурдагы энергиялык деӊгээлине кайтканда hv = 4,9 эВ ко барабар энергиянын квантын нурлантышат . Бул нурлануунун жыштыгын Бордун үчүнчү постулаты боюнча (1.22 формуласы ) оной эле тапсак болот :
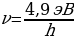 = 1,18*1015 Гц.
= 1,18*1015 Гц.
Бул чондук жыштыктын сымаптын буусунун нурлануу спектриндеги тиешелүү сызык үчүн спектроскопиялык ыкманы колдонуп түздөн – түз аныкталган мааниси менен дал келет .
Франк – Герцтин кийинки тажрыйбаларында атомдор жуткан (нурланткан) энергиянын дискреттүү маанилери натрийдин , гелийдин буулары үчүн да аныкталган .
§5. Суутектин атомунун спектри
(Бордун теориясы)
Суутектин атомунда бир элементардык оӊ зарядка ээ ядронун (протондун) тегерегинде терс элементардык -е зарядына ээ бир электрон айланат. Ядронун массасы электрондун массасынан 1840 эсе чоӊ болгондуктан , аны кыймылсыз деп эсептейбиз жана биринчи жакындатууда электрондун орбитасын айлана деп алабыз . Протон менен электрондун ортосунда кулондук гана күч аракет этишкендикткен электрондун кыймылы үчүн төмөндөгүдөй тендемени жазып алабыз :
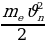
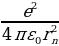 (1.23)
(1.23)
мында mе - электродун массасы , 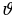 n – электрондун n – орбитадагы ылдамдыгы ,
n – электрондун n – орбитадагы ылдамдыгы , 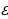 о = 8,85*10-12 Ф/м – электрдик турактуулук .
о = 8,85*10-12 Ф/м – электрдик турактуулук .
(1.22) жана (1.23) тендемелерин чогуу чыгарып , жөнөкөй өзгөртүп түзүүдөн кийин суутектин атомунун орбиталарынын радиустары үчүн төмөнкүдөй туюнтманы алабыз :
rn = 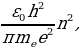 (1.24)
(1.24)
мында n – кванттык саны 1,2,3,… бүтүн маанилерге ээ болот . (1.24) формуласы боюнча каалагандай стационардык орбитанын радиусун эсептесек болот . Мисалы үчүн ядрого эӊ кичине аралыкка жайланышкан орбитанын (n = 1) радиусу (биринчи Бордук радиус )
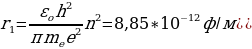
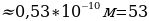 пм
пм
(1.24) формуласынын оӊ жагындагы n ден башка бардык чоӊдуктар турактуу болушат . Демек , турактуу орбиталардын радиустары өз ара натуралдык катардын сандарынын квадраттарындай , б.а., 1:4:9:16 ж.б.у.с. катышат .
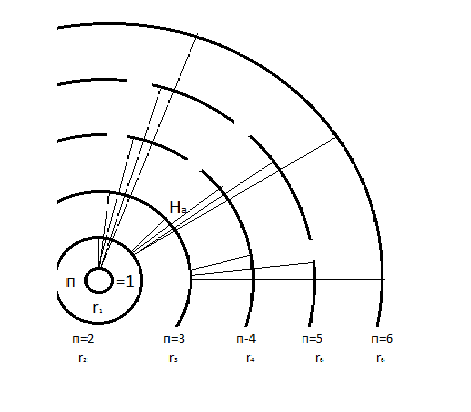
(1.24) формуласы боюнча эсептелген суутектин атомунун орбиталары 1.10 – сүрөтүндө көргөзүлгөн . Радиустун пикометр боюнча туюнтулган маанилери төмөндөгүдөй болушут : 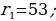
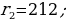
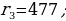
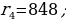
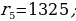 жана
жана 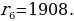
Эми атомдогу электрондун толук энергиясы 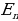 ди тарабыз .
ди тарабыз .
Ал электрондун орбита боюнча алга умтулуу кыймылынын кинетикалык энергиясы 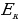 нын жана электрондун ядрого тартылуусунун потенциалдык энергиясы
нын жана электрондун ядрого тартылуусунун потенциалдык энергиясы 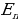 нын суммасынын турат .
нын суммасынын турат .
(1.23) формуласынын эске алып , төмөнкүнү алабыз :



Пашендин сериясы
Бальмердин сериясы
Лаймандын сериясы
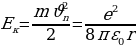 (1.25)
(1.25)
Электрондун потенциалдык энергиясы терс жана төмөндөгүгө барабар болот :
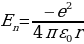 (1.26)
(1.26)
Ошентип толук энергия Еn төмөнкүчө аныкталат :
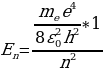 . (1.27)
. (1.27)
Бул формула боюнча электрондун энергиясын каалагандай турактуу орбита үчүн тапсак болот . Мисалы , ядрого эӊ жакын жайгашкан орбита үчүн (n=1)
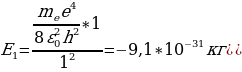
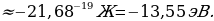
Стационардык орбитада жайланышкан электрондун толук энергиясы атомдун энергиясынын деӊгээли же энергиялык деӊгээл деп аталат . 1.11- сүрөтүндө суутектин атомунун (1.27) формуласы боюнча эсептелген энергиялык деӊгээлдеринин схемалык сүрөттөлүшү жана аларга тиешелүү энергиянын маанилери көргөзүлгөн .
Ошентип , (1.27) формуласына ылайык , атомдун энергиясы n кванттык санынын өсүшү , б.а., электрондун орбитасынын радиусунун өсүшү менен чоӊоёт экен .
Атом эӊ кичине энергияга (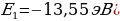 электрон ядрого эӊ жакын жайгашкан орбита (n=1) боюнча кыймылдаганда , ал эми энергиянын эӊ чон маанисине (
электрон ядрого эӊ жакын жайгашкан орбита (n=1) боюнча кыймылдаганда , ал эми энергиянын эӊ чон маанисине (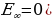 – электрон эӊ алыскы орбита ( n =
– электрон эӊ алыскы орбита ( n = 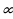 ) боюнча кыймылдаганда , б.а., атом иондошкон учурда ээ болот.
) боюнча кыймылдаганда , б.а., атом иондошкон учурда ээ болот.




























Дүүлүккөн
деӊгээл
w=-0,84 эВ
W=-0,54 эВ
W =-0,38 эB
w = 0
n = 4
n = 5
n = 6
Нормалдуу
деӊгээл
Лаймандын
сериясы
Бальмердин
сериясы текст
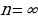



n = 3
Пашендин
сериясы



W=-13,55
W=-1,50 эВ
n = 2
Электрон экинчи орбитадан (n = 1) биринчи орбитага (n = 1) өткөндө атом hv2-1 = - 3,38 эВ – (-13,55 эВ) = 10,17 эВ энергиясына ээ квантты нурлантат , ал эми электрон үчүнчү орбитадан (n = 3) экинчисине (n = 3) өткөндө 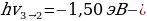 3,38 эВ) = 1,88 эВ энергиясына ээ квант нурланат . Бул нурланууларга жыштыктардын (толкун узундуктардын) төмөндөгүдөй маанилери туура келет :
3,38 эВ) = 1,88 эВ энергиясына ээ квант нурланат . Бул нурланууларга жыштыктардын (толкун узундуктардын) төмөндөгүдөй маанилери туура келет :
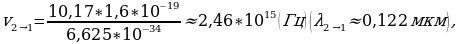
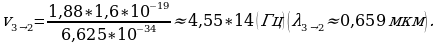
Электрон алыс жайланышкан орбитага , б.а., атомдук жогорку энергиялык деӊгээлде өзүнөн – өзү өтүшү мүмкүн эмес . Мындай өтүү болуш үчүн атомго тыштан энергиянын белгилүү санын беришибиз , б.а., атомду дүүлүктүрүү керек . Мисалы үчүн , электрон биринчи стационардык орбитадан экинчисине өтүшү үчүн , атом 10,17 эВ ко барабар энергияны жутушу керек .
Атомдун нормалдуу абалы болуп , электрон ядрого эӊ жакын орбита (n = 1) боюнча кыймылдаган учур эсептелет . Мында атом квантты нурланта албайт , себеби бул орбитада кыймылдаган электрон ядрого андан ары жакындай албайт . Атомдун нормалдуу абалына туура келген энергиялык денгээл 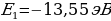 нормалдуу деӊгээл; калган деӊгээлдердин баары дүүлүккөн деп аталышат .
нормалдуу деӊгээл; калган деӊгээлдердин баары дүүлүккөн деп аталышат .
Атомдун нурлануусунун жыштыгы үчүн жалпы формуланы чыгарабыз . Бул үчүн энергиянын (1.27) туюнтмасын жыштыктар шартынын туюнтмасы (1.22) ге коёбуз :
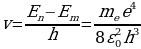
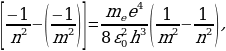 (1.28)
(1.28)
мында n жана Еn - атомдун баштапкы абалына (нурлантканга чейинки) туура келген кванттык сан жана энергия , m жана Еm – атомдун акыркы абалы (нурланткандан кийин) үчүн ошол эле мүнөздөмөлөр . (1.28) формуласынын оӊ жагындагы көбөйтүүчү Ридбергдин турактуусуна барабар болот :
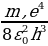 =
= 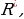 (1.29)
(1.29)
анда (1.28) формуласы
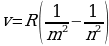 (1.30)
(1.30)
түрүндө ээ болот .
(1.30) формуласынын эмпирикалык түрдө алынган сериалдык (1.17) – (1.20) формулалары менен салыштыруу , алар (1.30) формуласынын жекече учурлары экендигин көргөзөт .
_______________________
* спектроскопияда 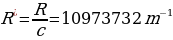 чондугу колдонулат .
чондугу колдонулат .
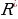 да Ридбергдин турактуусу деп аталат .
да Ридбергдин турактуусу деп аталат .
Демек , Лаймандын сериясынын спектралдык сызыктары электрон экинчи , үчүнчү , төртүнчү ж.б орбиталардан биринчисине; Бальмердин сериясынын сызыктары үчүнчү , төртүнчү , бешинчи ж.б орбиталардан экинчисине ; Пашендин сериясынын сызыктары электрон төртүнчү , бешинчи , алтынчы орбиталардан үчүнчүсүнө ж.б.у.с. өткөн учурларга туура келет .
Газ ар кандай дүүлүгүшкөн көптөгөн атомдордон тургандыктан , анда бир эле убакытта электрондун мүмкүн болгон бардык өтүүлөрү орун алат .
Ошондуктан суутектин атомунун спектринде бир эле убакытта бардык сериялардын сызыктары байкалат .
Лаймандын , Бальмердин жана Пашендин спектрдик серияларынын пайда болушу (1.10) жана (1.11) сүрөтүндө көргөзүлгөн .
(1.30) формуласынан Ридбергдин турактуусуннун физикалык мааниси келип чыгат ; эгерде n = 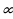 жана m = 1 болсо , анда v = R , б.а., Ридбергдин турактуусу суутектин атомунун нормалдуу абалга өткөн кездеги нурлантуусунун жыштыгына барабар .
жана m = 1 болсо , анда v = R , б.а., Ридбергдин турактуусу суутектин атомунун нормалдуу абалга өткөн кездеги нурлантуусунун жыштыгына барабар .
Суутектин атомунун түзүлүшү жөнүндөгү Бордун теориясы суутек сымал , б.а., бир эле электронду курамына камтыган (мисалы 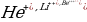 иондошкон атомдор үчүн да орун алат . Бирок бул учурда ядронун зарядын е эмес , Ze (Z – элементтин атомдук номери) деп түшүнүүбүз керек .
иондошкон атомдор үчүн да орун алат . Бирок бул учурда ядронун зарядын е эмес , Ze (Z – элементтин атомдук номери) деп түшүнүүбүз керек .
Суутек сымал атомдор үчүн Бордун (1.30) спектрдик формуласы төмөндөгүдөй түргө ээ болот
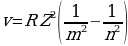 (1.31)
(1.31)
Бордун теориясы суутектин атомунун спектрин абдан жакшы түшүндүргөн , бирок көп электрондуу атомдордун спектрин түшүндүрүү үчүн Бордун теориясын колдонууга мүмкүн эмес болгон .
Көп электрондуу атомдордун спектрлеринде бир сызыктын ордуна бири – бирине жакын жайланышкан эки же андан көп спектрдик сызыктар байкалган . Бул кубулуш мультиплеттүүлүк деп аталат . Мультиплеттүүлүк берилген n кванттык санына туура келген энергиялык деӊгээлдин чегинде электрондор энергиялары боюнча бир аз айырмалана тургандыгын күбөлөйт .
Айлана түрүндөгү орбиталарга негизделген Бордун теориясы бул кубулушту түшүндүрө алган эмес . Мындан атомдогу электрондун бардык мүмкүн болгон энергиялык деӊгээлдеринин мүнөздөө үчүн бир эле кванттык сан жетшсиздик кылаары келип чыккан .
1916 – ж . Немец физиги А.Зоммерфельд (1868 – 1951 – жж.) электрон жеке эле айлана боюнча эмес эллипстик орбита боюнча да кыймылдашы мүмкүн деп болжолдогон . Эллипстин фокусунда жайгашкан ядродон ар кандай алыстыкта электрондун ылдамдыгы өзгөрөт . Салыштырмаалуулук теориясына ылайык кыймылдаган нерсенин массасы 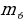 ылдамдыктын чоӊоюшу менен өсөт жана
ылдамдыктын чоӊоюшу менен өсөт жана
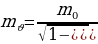
Формуласы менен аныкталат , мында с - жарыктын ылдамдыгы , 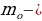 нерсенин тынч абалдагы массасы .
нерсенин тынч абалдагы массасы .
Демек электрондун кыймылынын ылдамдыгынын өзгөрүшү анын массасынын өзгөрүшүнө алып келет бул болсо электрондун кыймыл санынын моменти 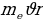 дин өзгөрүүсүн шарттайт . Мына ушуну менен бир кванттык сан менен мүнөздөлгөн энергиялык деӊгээлдин чегинде электрондун энергиялык мүнөздөмөлөрүнүн ар башка болушун түшүндүрүүгө болот . Эгерде айлана формуласындагы орбитаны мүнөздөөгө анын радиусун аныктоочу бир эле кванттык сан n жетиштүү болсо , эллипстик орбита үчүн эки чондукту - эллипстин чоӊ жана кичине жарым окторун билүү керек болот . Жарым октордун ортосундагы катнаш каалагандай болбойт , алар секириктүү гана өзгөрө алышыт , б.а., квантталат . Бул учурда чоӊ жарым ок n кванттык санына , ал эми кичине жарым ок k кванттык санына туура келет . Мында n башкы кванттык сан деп аталат жана бүтүн сандарга барабар болот , k - кошумча кванттык сан деп аталып , башкы кванттык сандан чоӊ эмес бүтүн сандарга барабар мааниге ээ болот . Ошентип , ар бир энергиялык деӊгээл , кошумча кванттык сандарга туура келген энергиялардын деӊгээлдерине ажырап кетет .
дин өзгөрүүсүн шарттайт . Мына ушуну менен бир кванттык сан менен мүнөздөлгөн энергиялык деӊгээлдин чегинде электрондун энергиялык мүнөздөмөлөрүнүн ар башка болушун түшүндүрүүгө болот . Эгерде айлана формуласындагы орбитаны мүнөздөөгө анын радиусун аныктоочу бир эле кванттык сан n жетиштүү болсо , эллипстик орбита үчүн эки чондукту - эллипстин чоӊ жана кичине жарым окторун билүү керек болот . Жарым октордун ортосундагы катнаш каалагандай болбойт , алар секириктүү гана өзгөрө алышыт , б.а., квантталат . Бул учурда чоӊ жарым ок n кванттык санына , ал эми кичине жарым ок k кванттык санына туура келет . Мында n башкы кванттык сан деп аталат жана бүтүн сандарга барабар болот , k - кошумча кванттык сан деп аталып , башкы кванттык сандан чоӊ эмес бүтүн сандарга барабар мааниге ээ болот . Ошентип , ар бир энергиялык деӊгээл , кошумча кванттык сандарга туура келген энергиялардын деӊгээлдерине ажырап кетет .
Бордун теориясы атомдун теориячын өнүктүрүүдө ири кадам болгон . Бул теория классикалык физиканын жоболорун атомдун ичиндеги кубулуштарга колдонууга болбостугун жана микродүйнөдө башкы орунга жаны механика – кванттык механиканын
закондору чыгаарын көрсөттү
Жогоруда биз баяндаган элементардык теория андан ары такталып жана өркүндөтүлгөн . Аларды кароонун кажети жок , себеби азыркы учурда Бордун теориясы тарыхый гана мааниге ээ .
Алгачкы ийгиликтерден кийин теориянын улам жаӊы жетишпегендиктери чыга берди . Теориянын өзгөчө чоӊ кемчилиги, ал суутектин атомунан кийин жайланышкан эӊ жөнөкөй атомдордун бири гелийдин атомунун түзүлүшүн түшүндүрө албаганы болгон .
Бул жетишпегендиктер Бордун теориясынын эӊ эле начар жагы , анын ички логикалык карама – каршылыктары менен түшүндүрүлөт : Бордук теория толугу менен классикалык же кванттык болгон эмес . Заттардын толкундук касиети ачылгандан кийин классикалык механикага таянган Бордун теориясы атомдук кубулуштардын ыраттуу теориясын түзүүдөгү өткөөл этабы боло тургандыгы түшүнүктүү болуп калды .
Текшерүү үчүн суроолор
Атомдун түзүлүшү жөнүндө Томсондун моделин мүнөздөгүлө
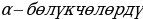 чачыратуу боюнча Резерфорддун тажрыйбасын түшүндүргүлө .
чачыратуу боюнча Резерфорддун тажрыйбасын түшүндүргүлө .
Бул тажрыйбадан Резерфорд кандай таянактарды чыгарган ?
Резерфорддун формуласын жазып түшүндүргүлө .
Атомдун спектрлериндеги законченемдүүлүктөр жөнүндө айтып бергиле .
Спектроскопиялык толкундук сан деп эмнени айтабыз ? Формуласын жазгыла .
Суутектин спектрин мүнөздөгөн Бальмердин сериялык формуласын жазып түшүндүргүлө . Башка сериялык формулаларды мүнөздөгүлө .
Бордун постулаттарын атагыла .
Франк жана Герцтин тажрыйбасынын схемасын чийип түшүндүргүлө . Аны мүнөздөгөн графигин сызгыла .
Суутектин атомунун спектрин мүнөздөгөн Бордун теориясы жөнүндө айтып бергиле .
Атомдун энергиялык деӊгээлинин формуласын жазып түшүндүргүлө .
Суутек сымал атомдор үчүн Бордун спектрдик формуласын жазып түшүндүргүлө .
Ридбергдин турактуусунун физикалык маӊызын түшүндүргүлө.
Мультиплеттүүлүк деген кандай кубулуш ?
4-БАП
БИР ӨЛЧӨМДҮҮ КЫЙМЫЛ
Кванттык теориянын жоболорун изилдөөдөн, талдоодон мурун, биз Шредингердин теӊдемеси менен толук таанушуубуз керек. Ал үчүн бир өлчөмдүү физикалык системанын толкундук механикасын окуп үйрөнөбүз. Бир өлчөмдүү маселелерди кароодо, биринчиден эӊ жөнөкөй моделдерди пайдаланып толкундукмеханиканын кээ бир өзгөчөлүктөрү менен таанышабыз. Бул өзгөчөлүктөр менен кийинчерээк татаал учурларды караган кезде дагы кездешебиз; экинчиден, толкундук механиканын көптөгөн татаал маселелери тийиштүү өзгөртүп түзүүлөрдөн кийин бир өлчөмдүү учурдагы Шредингердин теӊдемесине окшош теӊдемелерди чыгарууга алып келет.
§1. Түпсүз тереӊ потенциалдык
Чуӊкурдагы бөлүкчө
Бул учурда кванттык эффектилердин байкалышы үчүн потенциал де Бройлдун толкунунун узундугундай өлчөмдөгү аралыкта байкалаарлык түрдө өзгөрүүсү керек. Бул шартты канаатандыруучу потенциалдардын эӊ жөнөкөй учуру болуп тик бурчтуу потенциалдар эсептелет. Бул потенциалдар кээ бир чекиттерде биринчи тартиптеги үзгүлтүксүз үзүлүүсүнө ээ,ал эми бул чекитттердин ортосунда опотенциалдын мааниси турактуу болот. Демек, х огу бир нече интервалдарга бөлүнүп, ал интервалдардын ичинде потенциал кандайдыр бир анын турактуу мааниге ээ.


U=∞![]() ∞
∞
U=∞![]()
![]()






Потенциалдык
чуӊкур
m
О
4.1-сүрөт
Анда биздин маселедеги потенциалдык энергия төмөндөгүдөй чектик шартты канаатандырышы керек:
U=0 качан 0˂х ˂L,
U=∞ качан х≤,
U=∞ качан х≥L.
Маселенин шартынын мындай берилишинде бөлүкчө потенциалдык чуӊкурдун ичинде гана болушу керек жана бөлүкчө чуӊкурдун ичинде гана болушу керек жана бөлүкчө чуӊкурдун тышына чыга албайт. Анда толкундук функция төмөндөгүдөй чектөөчү шартты канааттандырышы керек
Ψ(х)=0 качан 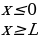 (4.2)
(4.2)
жана
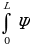 (х)Ψ(х)dx=1.
(х)Ψ(х)dx=1.
Бөлүкчөнүн убакыттын ар кандай моментинде потенциалдык чуӊкурдун кай жеринде боло тургандыгын так көрсөтө албайбыз. Ошондуктан бөлүкчөнү мүнөздөө үчүн убакыттан көз каранды чоӊдуктарды пайдаланууга болбойт. Демек, потенциалдык чуӊкурдун ичиндеги бөлүкчөнү сүрөттөө үчүн Шрендингердин турактуу теӊдемесин колдонушубуз керек.
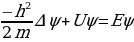
Бир өлчөмдүү учур үчүн
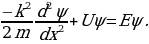
Потенциалдык чуӊкурдун ичинде U=0, анда
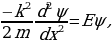 (4.3)
(4.3)
Жөнөкөй өзгөртүп түзүүдөн кийин
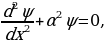 (4.4)
(4.4)
Мында
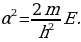 (4.5)
(4.5)
(4.4) теӊдеси чуӊлурдун ичиндеги бөлүкчөнүн абалын мүнөздөөчү экинчи тартиптеги, бир тектүү дифференциалдык теӊдемелерди чыгаруу үчүн, адатта, бул теӊдемелерди мүнөздөөчү теӊдемелери түзүлөөрү бизге математикалык талдоо курсунан белгилүү. Биз
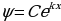 , (4.6)
, (4.6)
Болссун дейли. Анда
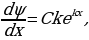

Бул маанилерди (4.4) кө коюп, окшош мүчөлөрүн кыскартып жиберсек, төмөндөгүдөй мүнөздөөчү теӊдемени алабыз
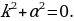 (4.7) мында мүнөздөөчү теӊдеменин тамырлары төмөндөгүгө барабар болот.
(4.7) мында мүнөздөөчү теӊдеменин тамырлары төмөндөгүгө барабар болот.
K1.2=±iα. (4.8)
Демек, (4.4) теӊдемесин канаатандыруучу толкундук функция (4.8) деги тамырлардын маанисин (4.6) га коюуда келип чыгат.
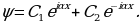 (4.9)
(4.9)
Бул толкундук функция х огу боюнча карама-каршы багытта таралган эки толкундун суперпозициясын көргөзүүчү толкундук функция болуп эсептелет. Бул барабардыктын оӊ жагындагы биринчи мүчө х огу боюнча солдон оӊго, экинчи мүчө болсо потенциалдык чуӊкурдун дубалчасынан чагылып оӊдон солго таралган толкундарды мүнөздөшөт. Ошентип, тоолкундук функция туруучу толкундун функциясы түрүндө алынды.
Эми (4.9) формуласындагы анык эмес С1 жанаС2 турактуулары эмнеге барабар экендигин аныктайбыз. Бул үчүн чектик шартын пайдаланабыз.
Эгер х=0 болсо, 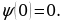 Анда (4.9) теӊдемеси төмөндөгүдөй түргө ээ болот
Анда (4.9) теӊдемеси төмөндөгүдөй түргө ээ болот
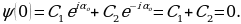
Демек,
С1=-С2
Ошондуктан
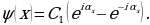
Эйлердин
e±iαx=cosαx±isinαx.
Формуласын колдонуп, бул функцияны төмөндөгүчөөзгөртүп түзүп алсак болот:
Ψ(x)=C1[(cosαx+isinαx)-(cosαx-isinαx)]=2iC1sinαx.
Эми экинчи чектик шартын колдонобуз. Эгер x=L болсо, Ψ(L)=0.
Ψ(L)=2iC1sinαL=0.
Мында C1≠0, ошондуктан sinαL=0, анда
αL=arcsin0=nπ; n=0,1,2,3…
наиыйжада,
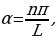 n=0,1,2,3… (4.10)
n=0,1,2,3… (4.10)
α чоӊдугунун маанисин (14.5)ке койсок
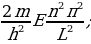
Же
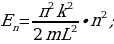 n=1,2,3… (4.11)
n=1,2,3… (4.11)
Бөлүкчө энергиянын (4.11) катышы менен аныкталуучу маанилерине гана ээ болот. Жөнүндө энергия дискреттик маанилерге квантталат, же болбосо бөлүкчө көптөгөн дискреттик абалдардын бирөөндө жайланышат деп айтышат. Убакыттын кандайдыр бир моментинде бөлүкчө мүмкүн болгон энергиялардын бирөөнө гана ээ болот. Бөлүкчөнүн энергиясы өзгөрүш үчүн, башкача айтканда, бөлүкчө башка деӊгээлге өтүшү үчүн ал кандайдыр бир сандагы энергияны алышы же бериши керек. Мында эки учурда теӊ алынган жана берилген энергия бөлүкчөнү башка мүмкүн болгон деӊгээлге которууга жетиштүү болушу керек.
Жогоруда (4.11) барабардыгында n=0,1,2,3,…маанилерине биз n=0 чоӊдугун алган жокпуз. Себебеби n=0 болсо (4.11) формуласынан Е=0 болушу керек. Бирок андай болушу мүмкүн эмес, тактап айтканда потенциалдык чуӊкурдун ичиндеги бөлүкчөнүн энергиясы нөлгө барабар болушу мүмүкүн эмес. Энергияны эӊ кичине мүмкүн болгон маанисин качан n=1 болгон байкалат.
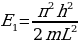 (4.12)
(4.12)
Эгер n=0 болсо, анда |Ψ|2=0: башкача айтканда потенциалдык чуӊкурда бөлүкчө жок дегенди билдирет. Бул болсо масенин шартына карама-каршы болгондуктан, мындай учур болушу мүмкүн эмес.
Энергиянын калган n=2,3,4,… үчүн маанилери 4Е1, 9Е1, 16Е1… ж.б.у.с. барабар болушат. Мында энргиянын минималдуу мааниси Е1нөлдөн жеитшээрлик аырмаланып турат.
Энергиянын n=1учурдагы маниси Е1 бөлүчөнүн негизги абалынын энергиясы (нөлдүк энергия) энергия болот. Бул жыйынтык классикалык механиканын жоболоруна карама-каршы жана ал аныксыздык катнашынан келип чыгат. Бөлүкчө чектеринде потенциал чексиз болгон аймакта гана болушу мүмкүн болгонудуктан, анын абалын ∆х=Lтаксыздыгы менен аныктап алсак болот. Демек, Гейзенбергдин аныксыздык принцибинен импульсту аныктоонун таксыздыгы 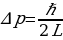 болушу керек. Демек энергия эч качан нөлгө барабар болушу мүмкүн эмес, себеби энергия нөлгө барабар болушу үчүн ∆р=0 болушу керек.
болушу керек. Демек энергия эч качан нөлгө барабар болушу мүмкүн эмес, себеби энергия нөлгө барабар болушу үчүн ∆р=0 болушу керек.
Эми толкундук функцияны карап көрөлү. Аныкталган L коэффициентинин маанисин пайдалансак
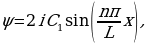
анда
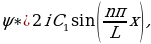
Демек ыктымалдуулуктун тыгыздыгы төмөндөгүгө барабар болот:
W=Ψ*Ψ=4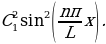 (4.13)
(4.13)
Бөлүкчөнүн потенциалдык чуӊкурдун ичинде бар экендигин аныктаган нормалоо шартын колдонобуз:
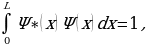
Же
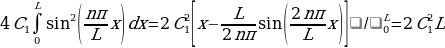
Ошондуктан
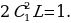
Анда,
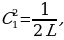
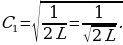
Демек нормаланган өздүк функциялар төмөндөгүгө барабар болот:
Ψn(x)=i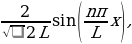
Же
Ψn(x)=i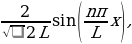 (4.14)
(4.14)
Ошгентип, бөлүкчөнүн түпсүз тереӊдиктеги потенциалдык чуӊкурда жайланышкандыгы, х1=0, х2=L маанилери менен чектелген кичинекей интервалдагы табылуу ыктымалдуулугу төмөӊдөгүгө барабар:
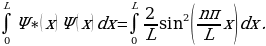 (4.14)
(4.14)
Жогоудагы маселенин чыгаылышын жыйынтыктап, жалпылап таблицага түшүрөбүз.
Таблицада келтрилген жыйынтыктарды колдонуп, ыктымалдуулуктун тыгыздыгынфн графигин n=1,2,3,... маанилери үчүн көргөзүүнү окурмандардын өздөрүнө сунуш кылабыз. Бул графиктер төмөндөгүдөй болушат (4.2-сүр.). Жогоруда n=1 учурундагы толкундук функция үчүн бөлүкчөнү 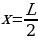 чекитинде табуу ыктымалдуулугу башка жерге караганда жогору. Бирок тескерисинче n=2 учурундагы толкундук функция үчүн бөлүкчөнү
чекитинде табуу ыктымалдуулугу башка жерге караганда жогору. Бирок тескерисинче n=2 учурундагы толкундук функция үчүн бөлүкчөнү 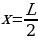 чекитинде табуу ыктымалдуугу нөлгө барабар, башкача айтканда, бөлүкчө Е2 энергиялык деӊгээлин ээлесе, анда ал
чекитинде табуу ыктымалдуугу нөлгө барабар, башкача айтканда, бөлүкчө Е2 энергиялык деӊгээлин ээлесе, анда ал 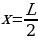 чекитинде жайланыша албайт.
чекитинде жайланыша албайт.
| n | Ѳздүк функция Ѱ(х) | Ыктымалдуулуктун тыгыздыгы Ѱ*Ѱ | Энергиялардын маанилери Еn |
| 1 |
|
|
|
| 2 |
|
|
|
| 3 |
|
|
|
| . . . | ………………………………… ………………………………… ………………………………… | ………………………………… ………………………………… ………………………………… | ………………………………… ………………………………… ………………………………… |
| n |
|
|
|






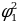
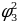

n=1 X n=3 X




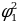
4.2-сүрөт
X
n=2
§ 2. Гармониялык осциллятор
Белукчелердун абалын мунездеенун жалпы учурларын кароочу кванттык механиканын жекече учуру классикалык механика болуп эсептелет. Эки механиканын ортосундагы айырмачьшыкты эн женвкей, кызыктуу физикалык маселе -гармониялык осцилляторду изилдввдв айкын кврвбуз. Идеалдык гармониялык осциллятор Шредингердин тендемесин колдонуу менен чечмеленуучу саналуу маселелердин бири болуп эсептелет. Бул проблеманы чечуудв алынган жыйынтыктар физикалык татаал маселелердин бири болгон молекуланын термелуу энергиясын биринчи жакындаштыруу боюнча аныктоодо ийгиликтуу колдонулат (тактап айтканда, кванттык механиканын ыкмалары менен так суроттелуучу бирден бир модель болуп эркин болукченун модели эсептелет).
Алгач гармониялык осциллятор женундогу маселенин классикалык механиканын алкагында чечилишин карап корелу. Массасы m болгон болукчо тен салмактуулук абалынан х аралыгына жылуу менен женокей гармониялык термелууго ээ болсун дейли. Мында белукче томондогудой кучтун аракет астында кыймылдайт:
F = -kx, (4.16)
Мында, к - турактуу чондук, F - бардык учурда тен салмактуулук абалга багытталган кучтун абсолюттук мааниси. Ньютондун экинчи законун колдонуп, бул тендемени томендегучо жазып алсак болот:
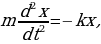 (4.17)
(4.17)
Же
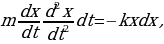
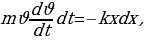
mϑdϑ=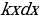 .
.
Интегралдасак
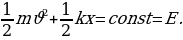 (4.18)
(4.18)
Мында 1-мучо - белукчонун кинетикалык энергиясы
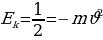 (4.19)
(4.19)
2-муче - белукчонун потенциалдык энергиясы болот
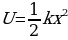 (4.20)
(4.20)
Ошентип, системанын толук энергиясы турактуу:
EK+U = E = const. (4.21)
Энергиянын каалагандай чектүү маанисинде бөлүкчө эки чекиттин ортосунда термелүү кыймылында болот. Мында А1 чекитинин координатасы х = L жана А2 чекитинин координа-тасы х = -L. Энергия (х жана 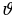 дан көзкаранды) каалагандай мааниге ээ болгондуктан, энергиянын (Е) мүмкүн болгон маанилеринин спектри үзгүлтүксүз болот.
дан көзкаранды) каалагандай мааниге ээ болгондуктан, энергиянын (Е) мүмкүн болгон маанилеринин спектри үзгүлтүксүз болот.
Төмөндөгүдөй белгилөөнү киргизебиз:
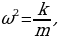 (4.22)
(4.22)
анда (4.17) тендемесин башка түрдө жазсак болот
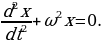 (4.23)
(4.23)
Бул тендеме мурунку параграфтагы толкундук тендемеге окшош. Ошондуктан анын чыгарылышын толкундук тендеме-нин чыгарылышына окшош жазабыз:
Х=Аеiωt+Be-iωt. (4.24)
А жана В турактууларынын маанилери бөлүкчөнүн баштапкы моменттеги координаттарынын жана ылдамдыгынын маанилерин колдонуу менен аныкталат. Жогорудагы чыгарылышты Эйлердин формуласын колдонуп өзгөртүп түзөбүз
х = A(cosa)t+isincot) + B(cosωt-isinωt) =
= (A+B)cosωt + (A-B)isinωt = Ccosωt+Dsinωt, (4.25)
Мында
С = A + В, D = i(A - В)
Жогорудагы (4.25) тендемеси бөлүкчөнүн абалынын убакыттан көзкарандылыгын мүнөздөйт. Бөлүкчөнүн ылдамдыгы убакыттын ар кандай моментинде
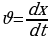 =- Ccosωt+Dsinωt (4.26)
=- Ccosωt+Dsinωt (4.26)
формуласы боюнча аныкталат. Белукче убакыттын t - 0 моментинде х = L чекитинде болсун жана бул учурдагы ылдамдыгы 9 = 0 дейли. Мындай баштапкы шартты колдонуп (4.25) жана (4.26) тендемелери томендвгуге ээ болот: С = L, D = 0. Анда бул эки тендеменин аяккы турун жазып алсак болот.
x(t) = Lcosωt. (4.27)
ϑ(t) = -Lωsinωt. (4.28)
Анда белукченун толук энергиясы
Е = 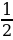 mL2ωsin2ωt +
mL2ωsin2ωt +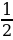 kL2ωs2ωt. (4.29)
kL2ωs2ωt. (4.29)
Белукче эн чон ϑЭ ч = coL ылдамдыгына тең салмактуулук абалы х = 0 аркылуу өтүп бара жаткан кезде ээ болот. Тең салмактуулук абалында бөлүкчөнүн потенциалдык энергиясы U = 0, ал эми толук энергия төмөнкүгө барабар болот:
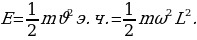 (4.30)
(4.30)
Качан бөлүкчө эң четки абалдарда, А, жана А2 чекиттеринде жайланышканда анын ылдамдыгы ϑ = 0, кинетикалык энергиясы Ек = 0. Бул абалдарда толук энергия потенциалдык энергияга барабар
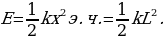 (4.31)
(4.31)
§ 3. Кванттык механикадагы гармониялык осциллятор
Гармониялык осцилляторду кванттык механиканын ыкмалары менен изилдөө Шредингердин тиешелүү теңдемесин чыгаруу аркылуу ишке ашырылат. Демек, биз жогорудагы гармониялык осцилляторду мүнөздөөчү теңдемени түзүүбүз керек. Бирок кванттык механикалык кароодо толкундук функция х огунун кандайдыр бир чекитинде топтошпой тургандыгын, башкача айтканда, бөлүкчөнүн убакыттын ар кандай моментиндеги так абалын аныктоо мүмкүн эмес экендигин эстен чыгарбообуз керек. Бизге белгилүү болгондой, Ψ*Ψ көбөйтүндүсү бөлүкчөнү х огундагы эң кичинекей dx интервалында табуунун ыктымалдуулугунун тыгыздыгын берет. Ошентип, бөлүкчөнүн абалынан көзкаранды күчтү камтыгын тендеме жогоруда классикалык гармониялык осциллятор үчүн (4.16) тендемесин колдонгон сыяктуу колдонууга ээ болбойт. Чындыгында эле, кванттык механикалык модель үчүн күч жөнүндөгү түшүнүк өзүнүн маанисин жоготот. Бирок биз мындан ары деле импульс, энергия түшүнүктөрүн колдоно беребиз. Ушул эле ой жүгүртүүлөрдөн классикалык осциллятор үчүн алынган (4.22) жана (4.23) теңдемелерине окшош, бөлүкчөнүн абалын жана анын ылдамдыгын убакыттан функция катары көргөзүүчү катнашты кванттык механикада ала албасыбыз көрүнүп турат.
Бирок биз системанын энергиясын карайбыз, анткени бул чоңдук классикалык жана квантмеханикалык маселелерде х координатасынын функциясы болгон потенциалдык энергия аркылуу берилет. Классикалык механикада потенциалдык энергия үчүн (4.20) формуласы, аракет эткен күчтүн формуласынан Ньютондун экинчи законунун жардамы аркылуу алынган. Бирок квантмеханикалык чечмелөөдө
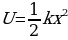 (4.32)
(4.32)
потенциалдык энергиясы механикалык системаны мүнөздөөчү негизги жана баштапкы чоңдук болуп эсептелет. Демек, бул кырдаал U = U(x) функциясын аныктоону жаныча карообузду талап кылат. Жогоруда (4.31) формуласы хэч= L абалын ээлегенде бөлүкчөнүн толук энергиясы анын потенциалдык
энергиясына барабар деген божомолдоонун негизинде алынган. Бирок мындан координаттын хэч маанисин толук энергия аркылуу туюндуруучу формуланы алууга мумкун эмес. Ошондуктан U(x) функциясына жаны шарттарды колдонбосок, анын аныктоо областы х = ±∞ ге чейин кеңейиши мүмкүн. Бул чексиздикте чектүү маанилерге ээ толкундук функцияны алууга болот дегендикке жатпайт, себеби аны нормалоого мүмкүн эмес жана анын жардамы менен бөлүкчөнү мейкиндиктин чектүү областарында табуунун ыктымалдуулугунун тыгыздыгын аныктоого болбойт. Ошентип, толкундук функцияга төмөндөгүдөй чөкөөо коёбуз: Ψ(х)-»0 качан х-+∞.
Эми бөлүкчөнүн кыймылы, бөлүкчө кандайдыр бир чекиттин чөлкөмүндө абсолюттук мааниси бөлүкчөнүн тең салмактуу абалынын жанындагы которулушуна пропроционалдуу болгон серпилгичтүү күчтүн таасири астында термелген мурдакы учурга окшош эмес. Тактап айтканда, жогорудагы бөлүкчөнүн кыймылынын формасын (4.32) формуласы менен туюнтулуучу потенциалдык «чуңкурдун» ичиндеги толкундардын системасы катарында карасак болот. Мында бөлүкчөнү ар кайсы областта, потенциалдык чуңкурдун ичинде, тышында табуунун ыктымалдуулугун эсептөөгө жана чуңкурдун формасы менен берилүүчү ар кандай шарттарда бөлүкчөнүн энергиясы эмнеге барабар деген суроого жооп берүүгө болот. Ал эми кандайдыр бир жол менен бардык тарабынан чектөөгө дуушар болгон толкундардын системасы чуңкурдун ичиндеги туруучу толкун болуп эсептелет.
Демек, маселенин негизи болуп туруучу толкундардын ар кандай мүмкүн болгон системасын мүнөздөөчү Ψп - өздүк функцияларын табуу жана бул функцияларга туура келүүчү Еп энергияларын, б.а., өздүк маанилерин аныктоо эсептелет.
Сызыктуу гармониялык осциллятордун биз караган моделин ар кандай сандагы өлчөмгө ээ учурлар үчүн жалпылоого болот жана ал кванттык механикада көп кезигүүчү потенциалдык чуңкур жөнүндөгү маселелердин мүнөздүүлөрүнүн бири болуп эсептелет.
Эгер потенциалдык чуңкурдун формасы классикалык
гармониялык осциллятордун потенциалдык энергиясы U = 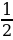 kх2
kх2
менен аныкталса, анда Шредингердин тецдемеси төмөндөгүчө жазылат.
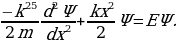 (4.33)
(4.33)
Бул толкундук теңдеменин чыгарылышы аны физиктер реалдуу физикалык системаларга колдонгонго чейин эле математиктерге белгилүү болгон. Биз жетишээрлик татаал болгон теңдемени чыгаруу процессине токтолбостон, түз эле бетгилүү өздүк маанилерди жана өздүк функцияларды талдоого өтөбүз.
Жогорудагы (4.33) теңдемесинин өздүк маанилери (энергиянын мүмкүн болгон маанилери) төмөндөгү формула менен аныкталат:
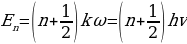 (4.34)
(4.34)
Мында ω = 2nv жана n = 0,1,2,3,…. Демек, классикалык механикадагы үзгүлтүксүз спектрден айырмаланып кванттык механикадагы гармониялык осциллятордун энергиясынын маанилеринин спектри дискреттүү (үзгүлтүкүү) болот. Бул спектрдеги энергиялык деңгээлдердин ортосундагы айырма hv га барабар.
Квантмеханикалык гармониялык осциллятор жөнүндөгү маселеден дагы бир кызык жыйынтык - осциллятордун энергиясы нөлгө барабар болбой тургандыгы келип чыгат. Жогорудагы (4.34) теңдемесинен энергиянын эң кичине мааниси нөлгө барабар эмес экендиги жана нөлдүк энергия деп аталган
энергия (качан n = 0 болгондо) 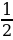 hv болоору көрүнүп турат (ушундай абал § 1 де талданган).
hv болоору көрүнүп турат (ушундай абал § 1 де талданган).
Төмөндөгү таблицада гармониялык осциллятор үчүн энергиянын өздүк маанилерин жана ага тиешелүү өздүк функциялардын маанилерин көргөзүп кетебиз.
4-2-таблица
| № | Энергиянын өздүк Мааниси En | Нормаланган өздүк функция Ψn(x) |
| 0 | | |
| 1 | | |
| 2 | | |
| . . . | ……………………………. ………………………… …………………………….. | ……………………………………… ………………………………………… …………………………………….. |
| n. | | Ψn= |
| Мында | ||
Жогорудагы көп мүчөлөр
H0=1
H1=2αx
H2=4α2x2-2
H3=8α3x3-12αx
………....
………....
………....
Hn=(-1)neξ2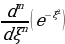 ,
,
мында ξ= αх, эрмиттин көп мүчөлөрү деп аталат да, математика боюнча окуу китептеринин көбүндө каралат.
Бөлүкчөнү х огундагы берилген аймакта табуунун ыктымалдуулугунун тыгыздыгы Ψ*Ψ көбөйтүндүсү же адаттагы белгилөө боюнча |Ψ|2 түрүндө аныкталат. Энергиянын кээ бир мүмкүн болгон маанилери үчүн ыктымалдуулуктун тыгыздыгынын болуштурулушу 4.3-сүрөтүндө көргөзүлгөн. Бул сүрөттө сызыктуу гармониялык осциллятордун U(x) потенциалдык энергиясынын графиги көргөзүлгөн. Мында А жана А', В жана В' ж.б.у.с. чекиттери, n - кванттык сандарынын берилген манилеринде потенциалдык энергия, толук энергиянын мүмкүн болгон маанилерине барабар чекиттер болуп эсептелинет. Классикалык осциллятор бул чекиттерден «сырткы» аймактарга чыга албайт (4.31). Кванттык осциллятор үчүн болсо ыктымалдуулуктун тыгыздыгы бул четки чекиттердин ары жагында да чектүү маанилерге ээ, башкача айтканда, аз да болсо бөлүкчөнү потенциалдык чуңкурдун сыртындагы аймактарда табуунун чектүү ыктымалдуулугу бар болот экен.










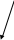




Классикалык механикада
Тыюу салынган аймак
Е0
Е1
Е2
Е3
§ 4. Потенциалдык тосмо.
Туннелдик эффект
Жогорудагы 4.3-сүрөтүндө көрсөтүлгөндөй, толкундук функция потенциалдык чуңкурдун сыртында нөлгө барабар болбойт. Демек, бөлүкчөнү классикалык чектин, тактап айтканда, потенциалдык чуңкурдун сыртынан табуунун ыктымалдуулугу чектүү мааниге ээ. Потенциалдык чуңкурдун ичиндеги ыктымалдуулуктун тыгыздыгы ар бир мүмкүн болгон энергиялык деңгээлге тиешелүү өздүк функция менен сүрөттөлүүчү, туруучу толкундардын системасынан түзүлөт. Ал эми туруучу толкун чагылдыруучу беттин ортосунда карама-каршы багытта таралуучу толкундардын кошулушунун жыйынтыгы катарында каралгандыктан, толкундук функцияны чагылдыруучу беттердин кайсынысына болбосун келип түшүүчү жана чагылуучу толкунду мүнөздөөчү функция катарында карасак болот. Бул учурда толкун потенциалдык чуңкурдун дубалынын ичинде бир аз аралыкка чейин таралат, ошондуктан чагылуу дубалдын бетинен жана ички катмарынан байкалат.
Толкундук функция кире баштаган чекитте потенциалдык чуңкурдун дубалы аябай жука, башкача айтканда, 4.3-сүрөтүндөгү А же В же С чекитинин ары жагында потенциалдык энергия өтө тездик менен нөлгө чейин төмөндөйт (4.3-сүрөттө В чекитинин жанында үзгүлтүктүү сызык менен көрсөтүлгөн,) дейли, толкундук функция ушул чекитте чектүү амплитудага ээ болушу мүмкүн. Ушул чекиттин кичине арыраак жагында толкундук функция кандай болот?
Бул суроого жооп берүү үчүн потенциалдык тосмо (барьер) деп аталуучу жука потенциалдык дубал жөнүндөгү түшүнүктү пайдаланып, төмөндөгүдөй жөнөкөй моделди карайбыз. Биз х огунда жатуучу анча чоң эмес аймакты карайлы, бул аймактын чектеринде потенциал кескин секирик жасасын: бирөө нөлдөн кандайдыр бир чектүү U маанисине чейин, экинчиси U дан нөлгө чейин. 4.4-сүрөтүндө потенциалдык тосмо |UE| көрсөтүлгөн: биринчи секирик х = 0 чекитинде (баштапкы чекит), экинчи секирик х = А чекитинде байкалат. Натыйжада, х огу үч аймакка бөлүнөт:
I аймак: хU1= 0,
II аймак: 0l, U11 = U ≠ 0,
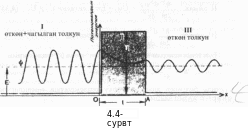
III аймак: х l, U111 = 0.
4.4-сүрөт
Толкун тосмого сол жактан келип түшсүн дейли. Биз тосмонун калыңдыгын кирүү тереңдигинен кичине кылып түзүп алабыз, ошондуктан тосмонун оң жагындагы III аймакта толкун кандайдыр бир чектүү амплитудага ээ болушу керек.
Жогорудагы 4.4- сүрөтүндө биз гармониялык осциллятор үчүн келтирилген энергиялык деңгээлдин бирин (4.3- сүрөтүн кара) көрсөттүк. Деңгээлдин толук энергиясы (мисалы Е,) үзүлмө сызык менен көргөзүлгөндөй, В чекитинен бир аз оң жакта жаткан х чекитинин жанында биз айланып өткөн тосмонун бийиктигинен кичине экендигин белгилей кетебиз. Тосмонун эң чоң потенциалдык энергиясы ушул деңгээлдеги бөлүкчөнүн толук энергиясына Караганда чоң, бирок ошону менен бирге толкундук функция тосмонун ары жагында чектүү амплитудага ээ экендигин айта кетүүбүз керек. Бул болсо, потенциалдык тосмонун чегинен сырткы аймакта бөлүкчөнү табуунун ыктымалдуулугу бөлүкчөнүн толук энергиясы тосмонун бийиктигинен аз болсо да кандайдыр бир чектүү мааниге ээ болорун билгизет: III аймактагы толкундук функциянын чектүү амплитудасын 4.4-сүрөтүндөгүдөй көргөзүүбүз керек. I, II жана III аймактагы толкундук функцияларды Ψ1, Ψ2 жана Ψ3 аркылуу белгилеп алып, ар бир аймак үчүн Шредингердин теңдемесин төмөндөгүчө жазып алабыз
I аймак: 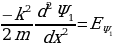 , анткени U1=0;
, анткени U1=0;
II аймак:  анткени U11=U; (4.35)
анткени U11=U; (4.35)
III аймак: 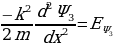 , анткени U111=0;
, анткени U111=0;
Бул теңдемелерди өзгөртүп түзүп α2 жана β2 чоңдуктарын
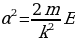 ;
; 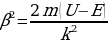
түрүндө белгилеп алып, жогорку теңдемелерди төмөндөгүчө өзгөртүп жазып алабыз:
I аймак: 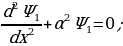
II аймак: 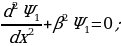 (4.36)
(4.36)
III аймак: 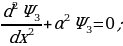
Бул теңдемелерди чыгаруу жолдору жөнүндөгү маалымат § 2 де айтылгандыктан, түздөн-түз чыгарылыштарын жазабыз
I аймак: Ψ1=Aeiαx+Be-iαx;
II аймак: Ψ2=Fe-βx+Geβx; (4.37)
III аймак: Ψ3=Ceiαx+De-iαx;
Мында A,B,F,G,C,D - толкундардын тиешелүү түзүүчүлөрүнүн амплитудалары. Алардын маанилери төмөндөгүчө:
А - тосмого солдон келип түшкөн толкундун амплитудасы,
В - I аймакта чагылган толкундун амплитудасы,
F - тосмо аркылуу II аймакка өткөн толкундун амплитудасы,
G - II аймактагы чагылган толкундун (тосмонун экинчи дубалынын А чекитинен) амплитудасы,
С - III аймакка өткөн толкундун амплитудасы,
D - III аймактагы чагылган толкундун (чындыгында мындай толкун жок) амплитудасы.
Жогоруда 4.4-сүрөтүндө биз толкундук функцияны үч аймакта, ал х огундагы каалаган чекитте үзгүлтүксүз, бир маанилүү аныкталгандай кылып, көрсөтүп алдык. Бул шарттын аткарылышы бизге тендемелерди чыгаруу менен жогорудагы амплитудаларды бөлүкчөнүн энергиясы, тосмонун бийиктиги жана калыңдыгы аркылуу туюнтууга мүмкүндүк берет.
Толкундук функция менен байланышкан ыктымалдуулуктун тыгыздыгы бул функциянын амплитудасынын квадратына пропорциялаш болгондуктан, биз тосмонун тунуктугунун коэффициентин аныктап алсак болот
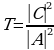 (4.38)
(4.38)
х = 0 чекитиндеги тосмонун бети үчүн чагылдыруу коэффициенты төмөндөгүчө аныкталат:
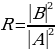 (4.39)
(4.39)
Эгерде тосмо бөлүкчөнүн толук энергиясына Караганда бийик же анын калындыгы тиешелүү толкундук функциянын толкун узундугуна салыштырмалуу чоң болсо, анда тунуктук коэффициенти төмөндөгүгө барабар болот:
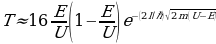 , (4.40)
, (4.40)
мында 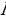 - тосмонун калыңдыгы.
- тосмонун калыңдыгы.
Жогоруда каралгандардан төмөндөгүдөй тыянак чыгарабыз: эгерде энергиясы Е болгон бөлүкчө бийиктиги Е ден чоң, жука потенциалдык тосмого келип түшсө, анда бөлүкчөнүн тосмодон өтүп кетүүсүнүн ыктымалдуулугу чектүү мааниге ээ болот. Туннелдик эффект деп аталуучу бул кубулуш кванттык механикада гана түшүндүрүлөт, ал эми классикалык механика бул кубулушту чечмелей албайт.
Радиоактивдүүлүктөгү α-ажыроону түшүндүрүүдө Г.А. Гамов (1904-1968-жж.) (1928-ж.) жана өз алдынча Кондон (1902-1924-жж.) менен Гёрни (1899-1953-жж.) (1929-ж.) туннелдик эффектини колдонушкандыктары кванттык механиканын ийгиликтүү чечмелөөлөрүнүн алгачкы мисалдарынын бири болуп эсептелет. Эгерде ядродогу α бөлүкчө ядрону чогуу кармап турган күчтөрдүн потенциалдык тосмосуна ич жагынан келип тийсе, анда туннелдик эффекттинин теориясынын негизинде жүргүзүлгөн эсептөөлөр көргөзгөндөй, 1038 бөлүкчөнүн бирөө тосмодон өтүп, ядродон чыгып кетиши мүмкүн. Ал эми α бөлүкчөсүнүн ядродон бөлүнүп чыгуусу бизге белгилүү радиоактивдүү α нурлануусу болуп эсептелет.
Ядронун диаметри болжол менен 10-14м, ядронун ичиндеги α бөлүкчөсүнүн ылдамдыгы 107 м/с, ошондуктан потенциалдык тосмо менен α бөлүкчөсүнүн ортосунда секундасына 1021 ге жакын кагылышуусу болот. Анда 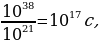 башкача айтканда, α бөлүкчөсү ядродон бөлүнүп чыгышы үчүн 3*109 жыл убакыт керек болот. Ошондуктан урандын радиоактивдүү жартылай ажыроосу үчүн миллиард жылдан көбүрөөк убакыт керек.
башкача айтканда, α бөлүкчөсү ядродон бөлүнүп чыгышы үчүн 3*109 жыл убакыт керек болот. Ошондуктан урандын радиоактивдүү жартылай ажыроосу үчүн миллиард жылдан көбүрөөк убакыт керек.
Полонийдин ядросунун потенциалдык тосмосунун бийиктиги урандын потенциалдык тосмосунун бийиктигине Караганда жапыз, ошондуктан бул учурда тосмо менен α бөлүкчөнүн 1017 кагьшышуусунда 1 бөлүкчө бөлүнүп чыгат. Кагьшышуунун жыштыгы дагы эле 1021с-1 десек, полонийдин ядросунан α бөлүкчө ар бир 10-4с сайын ажырап чыгып турат.
Кванттык механикада α ажыроонун туннелдик эффект теориясын колдонуу менен эсептеелер көргөзгөндөй, потенциалдык тосмонун бийиктигинин кичине эле өзгөрүшү радиоактивдүү изилдөөлөр үчүн жашоо мөөнөттөрүнүн жетишээрлик айырмаланышына алып келет.
Текшерүү үчүн суроолор
Потенциалдык чуңкурдун ичиндеги бөлүкчөнү сүрөттөөчү Шредингердин турактуу теңдемесин жазып түшүндүргүлө.
Классикалык механикадагы гармониялык осциллятор деген эмне?
Гармониялык осциллятордун толук энергиясынын формуласын жазып түшүндүргүлө.
Гармониялык осциллятор үчүн Шредингердин теңдемесин жазып бергиле.
Кванттык механикадагы гармониялык осциллятордун энергиясы нөлгө барабар болбой тургандыгын түшүндүргүлө.
Потенциалдык тосмо (барьер) дегенди кандай түшүнөсүңөр? Ал кандай аймактарга бөлүнөт?
Потенциалдык тосмонун аймактары үчүн Шредингердин тендемесин жазып тушундургуле.
Потенциалдык тосмонун тунуктугунун коэффициентинин формуласын жазгыла. Тосмонун бети үчүн чагылдыруу коэффициентин жазгыла.
Кванттык механикадагы туннелдик эффект деп эмнени айтабыз?
Туннелдик эффектин радиоактивдүүлүк кубулушун түшүндүрүүдө колдонулушу жөнүндө баяндагыла.
Ар кайсы радиоактивдүү элементтердин жарым ажыроо мезгилинин ар кандай узактыгын кандай түшүнөсүнөр?
15




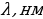
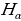
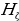
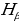
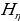
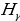
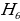
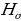
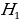
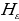
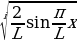
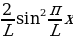
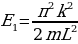
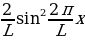
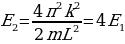
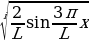
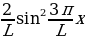
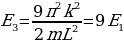
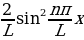
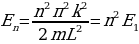
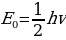
 =
=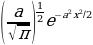
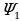 =
=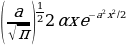
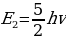
 =
=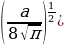
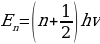
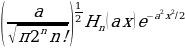
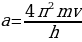 жана Hn+1=2(αx)Hn-2nHn-1
жана Hn+1=2(αx)Hn-2nHn-1









