Просмотр содержимого документа
«Fierul lectie ppt pentru chimie»

Fierul
Dancu, 2017

„ Nu este suficient să dobândeşti
înţelepciune,
trebuie să ştii de asemenea
cum s-o foloseşti”
Mark Cicero Thulium

Importanța
Cea mai importantă funcţie
a fierului în organism este
producerea hemoglobinei,
substanţa care dă celulelor
roşii culoarea specifică.
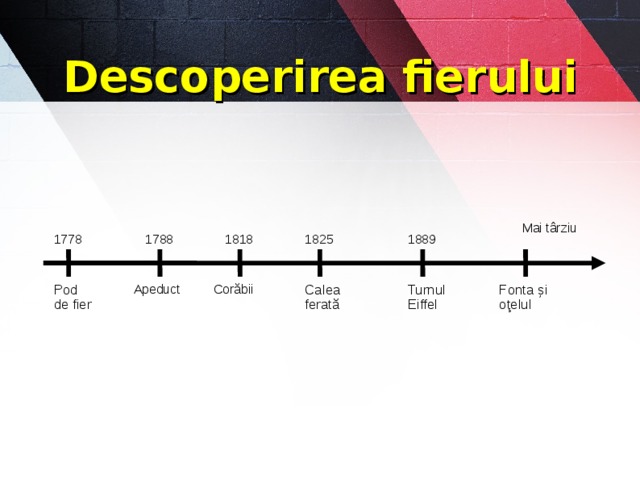
Descoperirea fierului
Mai târziu
1788
1889
1825
1818
1778
Pod de fier
Apeduct
Corăbii
Calea ferată
Turnul Eiffel
Fonta și oţelul

Structura atomului

Poziția în sistemul periodic

Răspândirea în natură
Fe este al II-lea metal (după aluminiu) şi cel mai răspândit metal greu
- Ocupă locul al patrulea dintre toate elementele
(după oxigen 49%, siliciu 26% şi aluminiu 7,5%)

Răspândirea în natură
Liber – în meteoriţi
În combinaţii
- – oxizi
- Fe2O3 hematit
- Fe2 O3∙H2O limonit
- Fe3O4 magnetit
- - sulfuri
- FeS2 pirita
- CuFeS2 calcopirita
- - carbonat - FeCO3 siderit

Proprietățile fizice
În stare pură fierul:
- este un metal cenuşiu,
- prezintă luciu metalic,
- densitatea 7,8 kg/dm3, fiind un metal greu,
- este bun conductor de căldură şi electricitate,
- este maleabil şi ductil,
- temperatura de topire 1538 ºC
- este atras de magnet

Proprietățile chimice
Fierul interacționează cu substanţele simple și cu substanţele compuse:
- Cu oxigenul.
- Clorul.
- Sulful.
- Apa ( la încălzire).
- Acidul clorhidric.
- Sărurile.

Proprietăți chimice
- 3Fe+2O2=Fe3O4+Q
- 2Fe+3Cl2=2FeCl3+Q
- Fe+S=FeS
Reacţionează cu apa la încălzire
3Fe+4H2O=Fe3O4+4H2
Reacţionează cu acizii
- se degajă H2.
Fe +2HCl =FeCl2 +H2
H2SO4+Fe=FeSO4+H2
Fierul poate substitui metalul mai puțin activ din săruri.
Fe+CuSO4=FeSO4+Cu


Obținerea fierului
a. Prin tratarea cu hidrogen la încălzire:
Fe2O3 + 3H2 = 2Fe + 3H2O
b. Prin metoda aluminotermică:
Fe2O3 + 2Al = 2Fe + Al2O3

Utilizarea fierului
Obiecte din oțel

Utilizarea fierului
- BRANCUSI - COLOANA INFINITULUI
Are o înălţime de 29,33 metri şi o masă de 29173 kg. Este construită din plăci din fontă. Trunchiurile de piramidă, goale pe dinăuntru, sunt fixate cap la cap pe un miez central de oţel, cu secţiune pătrată, uniformă pe toată înălţimea Coloanei Infinitului.

Utilizarea fierului
Un exemplu al măiestriei indiene în domeniul metalurgiei este şi coloana de fier din Delhi, care este constituită în proporţie de 98% din fier forjat şi a fost ridicată la sfârşitul secolului al IV-lea sau începutul sec. al V-lea.

Temă pentru acasă
- Paragraful 2.9, pag.51-53,
ex. 4 pag. 51.
- * Eseu:
- ” Importanţa Fierului la rezolvarea problemelor contemporanităţii şi pentru îmbunătăţirea calităţii vieţii”.


































