Физика - Поурочные разработки 11 класс - 2017 год
Состав ядра. Ядерные силы - ФИЗИКА АТОМНОГО ЯДРА - КВАНТОВАЯ ФИЗИКА
Физика атомного ядра — важный и обширный раздел современной физики, для которого особенно характерно соединение теоретических и экспериментальных методов исследования. В нём широкое применение наряду с законами и формулами классической механики и электродинамики находят законы и формулы релятивистской динамики, квантовой механики. Ввиду сложности строения атомного ядра как системы, состоящей из значительного числа нуклонов, при изучении ядра используются специальные модели. Среди них капельная модель ядра, оболочечная модель и др.
Изучение ядерной физики в школе существенно не только из-за её практические приложения, но и потому, что в этом разделе расширяются наши представления о фундаментальных силах природы, о глубинных законах строения материи. При изучении строения ядра человеку открывается новый мир физических объектов — мир элементарных частиц.
При построении учебного процесса рационально реализовать системный подход в отборе содержания уроков. Поэтому сначала изучают атомное ядро как физическую систему с определённым составом и взаимодействием элементов, затем рассматривают различные процессы — ядерные реакции. При этом параллельно рассматривают характеристики объектов и явлений, изучают экспериментальные средства их определения. В самом конце темы изучают практические следствия. Предлагаемый вариант планирования достаточно экономный, но всё же первый и второй уроки можно объединить. Проведение лабораторной работы программой предполагается, хотя она и не приведена в учебнике. В принципе после двух первых уроков далее содержание можно прямо планировать по логике учебника.
Урок 1. Состав ядра. Ядерные силы
Задачи урока: изучить протонно-нейтронную модель ядра — основу всех выводов в школьном курсе о строении и свойствах ядра; ввести понятия о новых силах, существенно отличающихся от ранее известных учащимся.
Ход урока
Урок можно провести в форме школьной лекции, дополнив рассказ учителя работой с учебником, таблицами.
I. Изложение нового материала.
Ранее было показано, что большая часть массы вещества сосредоточена в ядре — части атома очень малых размеров. Данный раздел посвящён изучению строения и свойств атомных ядер.
1. Что мы уже знаем о ядре? Размеры ядра, как это следует из опытов Резерфорда, имеют порядок r = 1014—1015 м. Заряд ядра положителен и равен Ze, где Z — порядковый номер элемента в таблице Менделеева, а е = 1,602189 ∙ 1019 Кл — положительный заряд, по абсолютному значению равный заряду электрона.
Какова же форма ядра атома? В настоящее время установлено, что форма ядер всех элементов близка к сферической, хотя бывают и слегка вытянутые или сплюснутые ядра.
Известны и массы ядер. Для определения массы ядра из массы атома надо вычесть массу электронов:

2. Наблюдается важная закономерность: масса любого ядра превышает массу ядра водорода приблизительно в целое число раз. Так, масса ядра гелия почти в четыре раза больше массы ядра водорода, масса ядра урана почти в 238 раз больше, и так для всех ядер. Можно предположить, что ядра многоэлектронных атомов состоят из ядер атомов водорода. Так ли это? Так или иначе, но после открытия атомного ядра встал вопрос о его строении.
В 1919 г. Э. Резерфорд, продолжая изучение ядер вещества, обнаружил среди частиц, выбитых из атомного ядра, частицу с единичным положительным зарядом и массой, равной массе ядра водорода. Она была названа протоном. Это подтверждает предположение, что ядро водорода входит в состав других ядер. Ядро водорода — это один протон. В ядро гелия должно входить два протона, так как заряд ядра гелия Z = 2. Вообще число протонов в ядре должно быть равно заряду ядра Z, совпадающему с порядковым номером элемента в периодической таблице Менделеева.
Кроме протонов в ядрах всех атомов, за исключением водорода, должны быть ещё какие-то частицы, так как массы ядер больше чем Zmp. В самом деле, ядро гелия имеет заряд, в два раза больший заряда протона, а масса ядра гелия почти в четыре раза больше массы протона. Из какого же числа протонов состоит ядро гелия — из двух или из четырёх? Решение этого вопроса сначала привело учёных к протонно-электронной модели атома. Согласно этой модели ядро атома гелия состоит из четырёх протонов и двух электронов, находящихся внутри ядра, так что общий заряд ядра оказывается равным 4е - 2е = 2е.
В дальнейшем выяснилось, что электронов в ядрах атомов вещества нет, они не могут входить в состав такой малой по размерам системы, как ядро, в силу своих волновых свойств.
3. В 1932 г. ученик Резерфорда английский физик Д. Чедвик открыл новую элементарную частицу. Она оказалась нейтральной и очень близкой по массе к протону. Назвали её нейтроном. В том же году советским физиком Д. Д. Иваненко и немецким физиком В. Гейзенбергом была предложена протонно-нейтронная модель ядра.
Сумма числа протонов и числа нейтронов называется массовым числом и обозначается буквой А. Если обозначить число нейтронов N, то мы получим формулу, связывающую три числовые характеристики ядра:
А = Z + N.
Теперь понятно, почему масса ядра приблизительно в целое число раз превышает массу протона:
Мя ≈ Аmр,
так как mn ≈ mp.
С помощью таблицы периодической системы элементов можно определить число протонов и нейтронов для ядер нескольких элементов. Вводим обозначение ядра:
AZX.
Ядра атомов элементов обозначаются той же буквой, что и сами эти элементы в химии, но дополнительно снабжаются индексами: Z — внизу, А — вверху.
Далее вводят понятие изотопа. Рассматривают изотопы водорода 11Н, 12Н (дейтерий), 13H (тритий), изотопы урана 23892U, 23392U, 23592U и другие изотопы.
4. Следующий этап изложения материала — знакомство с новыми фундаментальными силами — ядерными. Знания о ядерном взаимодействии систематизированы в таблице 43.
Таблица 43
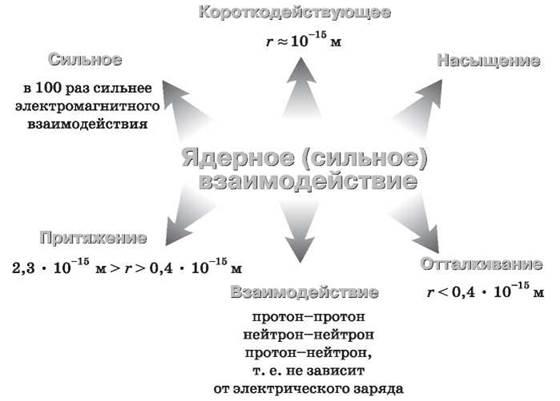
II. Для закрепления изучаемых понятий на уроке предлагают задания.
1. Определите плотность ядерного вещества.
2. Определите состав ядра углерода 146C.
3. Чем различаются ядра двух изотопов хлора с атомными массами 35 и 37?
III. Домашнее задание: § 78; упр. на с. 302 (ЕГЭ); упр. на с. 309 (1, 3).
Физика - Поурочные разработки 11 класс - 2017 год Модель ядерного взаимодействия. Решение задач - ФИЗИКА АТОМНОГО ЯДРА - КВАНТОВАЯ ФИЗИКА
После повторения материала предыдущего урока организуют работу с учебником: фронтальное повторение качественных вопросов, построение конспекта параграфа, запись уравнений реакций, выполнение блок-схем и др.
В заключение решают типичные задачи по выбору учителя.
Домашнее задание: § 79*, 81* (1, 2).


















