Урок физики в 11-м классе "Состав ядра. Ядерные силы"
Практикант:___________
Учитель:_____________
Методист:____________
Кол-во отсутствующих:________
Кол-во присутствующих:_______
Цели урока:
Изучить протонно–нейтронную модель ядра – основу всех выводов в школьном курсе о строении и свойствах ядра;
Познакомить учащихся с силами- ядерными, существенно отличающиеся от ранее известных.
Тип урока: урок связи теории с практикой.
Метод оборудования: словесный
Вид занятия: комбинированное
Форма обучения: групповая.
Ход урока.
Строение атома
Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. Открыли электрон, измерили его массу. Мысль об электронном строении атома, впервые высказанную В. Вебером в 1896 г., развил Х. Лоренц. Именно он создал электронную теорию: электроны входят в состав атома.
Опираясь на эти открытия, Дж. Томсон в 1898 г. предложил модель атома в виде положительно заряженного шара радиусом 10(-10) м, в котором плавают электроны, нейтрализующие положительный заряд(рис.1).
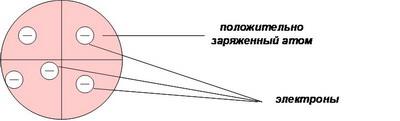
Рис.1
Экспериментальная проверка модели атома Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом (рис. 2).
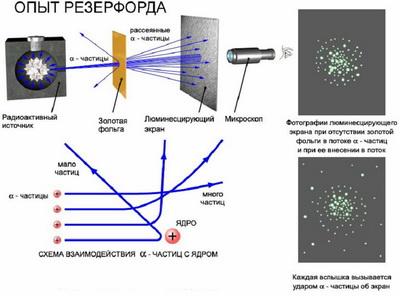
Рис.2
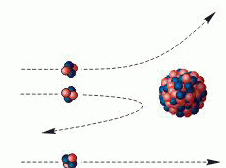
Рис.3
Пропуская пучок Альфа - частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил, что какая-то часть частиц отклоняется на довольно значительный угол от своего первоначального направления, а небольшая часть – отражается от фольги. Но согласно модели атома Томсона, частицы могли отклоняться только на углы около 200, но появлялись частицы, угол отклонения которых был больше 900 (рис. 3).
Резерфорд показал, что модель Томсона находится в противоречии с его опытами. Обобщая результаты своих опытов (рис. ).
Резерфорд предложил ядерную (планетарную) модель строения атома:
Атом имеет ядро, размеры которого малы по сравнению с размерами самого атома.
В ядре сконцентрирована почти вся масса атома.
Отрицательный заряд всех электронов распределен по всему объему (рис. 3, 4)
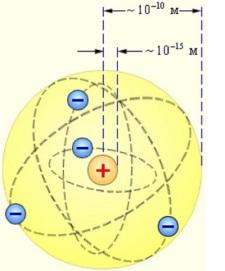
Рис. 4
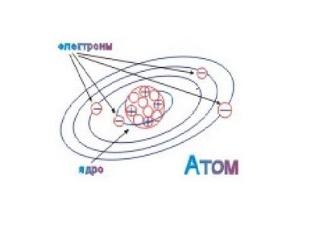
Рис. 5
Открытие нейтрона
Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил группе своих учеников во главе с Дж. Чедвиком заняться поиском такой частицы.
Через 12 лет в 1932 г. Чедвик экспериментально исследовал излучение, возникающее при облучении бериллия? - частицами, и обнаружил, что это излучение представляет собой поток нейтральных частиц с массой, примерно равной массе протона. Так был открыт нейтрон. На рис.5 приведена упрощенная схема установки для обнаружения нейтронов.
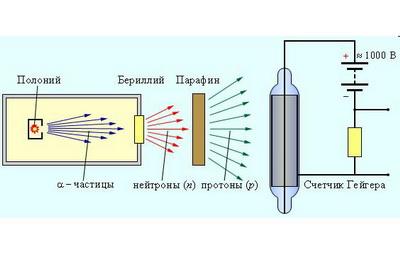
Рис. 6
Рис.2 – это элементарная частица.
Это не протон-электронная пара, как первоначально предполагал Резерфорд. По современным измерениям масса нейтрона mn = 1,67493·10–27 кг = 1,008665 а.е.м.
В энергетических единицах масса нейтрона равна 939,56563 МэВ.
Масса нейтрона приблизительно на две электронные массы превосходит массу протона.
Протон-нейтронная модель ядра
Сразу же после открытия нейтрона российский ученый Д. Д. Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении атомных ядер, которая полностью подтвердилась последующими исследованиями.
По современным измерениям, положительный заряд протона в точности равен элементарному заряду e = 1,60217733·10–19 Кл, то есть равен по модулю отрицательному заряду электрона. В настоящее время равенство зарядов протона и электрона проверено с точностью 10–22. Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление и остается одной из фундаментальных загадок современной физики.
Масса протона, по современным измерениям, равна mp = 1,67262·10-27 кг.
Протоны и нейтроны в ядре принято называть нуклонами.
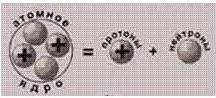
Рис. 7
Символическое обозначение ядра атома
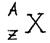
А - число нуклонов, т.е. протонов + нейтронов (или атомная масса)
Z - число протонов (равно числу электронов)
N - число нейтронов (или атомный номер )
N = A – Z
Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны удерживаться внутри ядер огромными силами, во много раз превосходящими силы нуклоновского отталкивания протонов.
Силы, удерживающие нуклоны в ядре, называются ядерными.
Особенности ядерных сил:
Ядерные силы примерно в 100 раз превосходят электростатические силы и на десятки порядков превосходят силы гравитационного взаимодействия нуклонов.
Важной особенностью ядерных сил является их короткодействующий характер. Ядерные силы заметно проявляются, как показали опыты Резерфорда по рассеянию a-частиц, лишь на расстояниях порядка размеров ядра (10–14–10–15 м). Ядерные силы очень быстро спадают с расстоянием.
Радиус их действия порядка 0,000 000 000 000 001 метра.
Для этой сверхмалой длины, характеризующей размеры атомных ядер, ввели специальное обозначение Фм (в честь итальянского физика Э. Ферми, 1901-1954).
Все ядра имеют размеры нескольких Ферми.
Радиус действия ядерных сил равен размеру нуклона, поэтому ядра - концентрация очень плотной материи. Возможно, самой плотной в земных условиях. Ядерные силы - сильные взаимодействия.
На больших расстояниях проявляется действие сравнительно медленно убывающих кулоновских сил.
На основании опытных данных можно заключить, что протоны и нейтроны в ядре притягиваются не зависимо от наличия заряда т. е. ядерные силы не зависят электрического заряда.
ЯДЕРНЫЕ СИЛЫ
Рис. 8
ЗНАЕШЬ ЛИ ТЫ?
В середине XX века теория ядра предсказала существование стабильных элементов с порядковыми номерами Z = 110 - 114.
В Дубне был получен 114-й элемент с атомной массой А = 289, который "жил" всего 30 секунд, что невероятно долго для атома с ядром такого размера. Сегодня теоретики уже обсуждают свойства сверхтяжелых ядер массой 300 и даже 500.
Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева
они расположены в одной клеточке (по-гречески изос - равный, топос - место).
Химические свойства изотопов почти одинаковы. Если элементов всего в природе - около 100, то изотопов - более 2000.
Многие из них неустойчивы, то есть радиоактивны, и распадаются, испуская различные виды излучений.
Изотопы одного и того же элемента по составу отличаются лишь количеством нейтронов в ядре (рис.7).
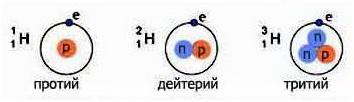
Рис. 9
Решение задач:
1. Сколько нуклонов, протонов и нейтронов содержится в ядрах следующих элементов:
11 Na23 A = 23 N = 23 – 11 = 12 Z = 11
11Na21 A = 21 N = 21 – 11 = 9 Z = 11
4B9 A = 9 N = 9 – 4 = 5 Z = 4
Самостоятельно: 8O16 3Li7 6C12 7N14 9F19 13Al27 92U235 82Pb207
2. Чем отличаются следующие элементы:
8О17 и 8О16 92U235 и 92U239
Домашнее задание: п. 105 упр. 14 (4).
Домашнее задание:

























