Тема урока: «Ионные реакции»
Класс: 9 класс
Разработка урока «Ионные реакции» составлена в соответствии УМК О.С.Габриэлян, Химия, 9 класс
Цель урока: сформировать у обучающихся понятие об ионных реакциях между электролитами в свете теории электролитической диссоциации, ознакомить с условиями их протекания, свойствами ионов.
Задачи урока:
Образовательная: совершенствовать умение составлять молекулярные, полные ионные и сокращенные ионные уравнения реакций обмена.
Развивающая: развивать логическое и критическое мышление, умение планировать работу, выбирать и применять необходимую информацию для выполнения задания, способность наблюдать, делать выводы.
Воспитательная: способствовать расширению кругозора обучающихся, воспитывать самостоятельность, аккуратность.
Тип урока: урок открытия новых знаний.
Методы обучения: беседа, наглядный, частично-поисковый, исследовательский.
Оборудование и реактивы:
Таблицы: «Периодическая система химических элементов Д.И. Менделеева», «Растворимость солей, кислот и оснований в воде», компьютер, мультимедийный проектор, экран, презентация «Реакции ионного обмена», алгоритм составления ионных уравнений реакций, инструктивные карточки.
Пробирки и реактивы для демонстрации опытов: соли, кислоты, щелочи, индикаторы.
Ход урока
1.Организационный момент.
Приветствие обучающихся. Создание положительной эмоциональной атмосферы.
2. Мотивация учебной деятельности.
На экране: Игра «Третий лишний»:
Задание: найти лишнюю формулу и объяснить по какому признаку она лишняя:
a) НСI б) H2SO4 в) H2SiO3
a) Cu(OH)2 б) Ba(OH)2 в) KOH
a) Na2CO3 б) CaCO3 в) CuSO4
3. Актуализация знаний учащихся.
- Что называется электролитической диссоциацией?
- Какие вещества относятся к электролитам? Дайте определение.
- Какие вещества относятся к неэлектролитам? Дайте определение.
- Чем обусловлена электропроводность растворов?
Чем обусловлена электропроводность растворов?
- Поясните, почему раствор поваренной соли проводит электрический ток, а раствор сахара нет.
-
 Назовите формулы сильных кислот, какие общие ионы образуются при диссоциации кислот?
Назовите формулы сильных кислот, какие общие ионы образуются при диссоциации кислот?
- Назовите формулы сильных оснований, какие общие ионы образуются при диссоциации оснований(щелочей)?
Назовите формулы сильных оснований, какие общие ионы образуются при диссоциации оснований(щелочей)?
- Все ли соли являются электролитами? Какие ионы образуются при диссоциации солей?
- Какие частицы называются: ионами, катионами, анионами?
4 . Изучение нового материала.
. Изучение нового материала.
Ребята! Мы уже изучили механизм электролитической диссоциации и знаем, что при взаимодействии электролитов соединяются только противоположно заряженные ионы. Это происходит тогда, когда образуется новое вещество в виде осадка, газа, малорастворимого вещества, слабого электролита. Такие реакции считаются необратимыми или протекают до конца. Их называют ионными и записывают ионными уравнениями реакций обмена.
Вывод: Реакции в водных растворах электролитов называют ионными.
Правила составления ионного уравнения реакции:
1.Растворимые в воде электролиты записываются в виде ионов.
2. Вещества практически нерастворимые, малодиссоциирующие, газы, оксиды записывают в виде молекул.
3. Образование осадка показывают знаком↓, газа ↑, после формулы вещества справа.
4. В сокращенном ионном уравнении записывают формулы только тех частичек, которые фактически взаимодействуют между собой.
5. В правильно записанном ионном уравнении реакции обмена, сумма зарядов ионов в левой и правой частях уравнения должна быть равна нулю.
Проблемный вопрос: Как узнать идет ли химическая реакция обмена до конца?
Ответ на этот вопрос можно найти в таблице: «Растворимость солей, кислот и оснований в воде».
Демонстрационный опыт:
Лабораторный опыт №1: Реакции, в результате которых образуется осадок.
Рассмотрим реакцию взаимодействия AgNO3 и NaCI.
| Алгоритм составления ионных уравнений | Уравнения реакций |
| 1.Напишите молекулярное уравнение реакции, расставьте коэффициенты. | AgNO3 + NaCI = AgCI + NaNO3 |
| 2.По таблице растворимости определите растворимость веществ и под формулами напишите – Р, Н, М | AgNO3 + NaCI = AgCI + NaNO3 Р Р Н Р |
| 3.В уравнении реакции образование осадка покажите знаком↓.
| AgNO3 + NaCI = AgCI↓ + NaNO3 Р Р Н Р |
| 4.Сосставьте полное ионное уравнение реакции обмена.
| Ag+ + NO3 - + Na + + CI- = AgCI ↓+ Na+ + NO3- |
| 5.Сравните левую и правую часть полного ионного уравнения реакции, вычеркните одинаковые ионы, которые не изменились, не участвовали в реакции. |     Ag+ + NO3 - + Na + + CI- = AgCI ↓+ Na+ + NO3- Ag+ + NO3 - + Na + + CI- = AgCI ↓+ Na+ + NO3-
|
| 6.Напишите сокращенное ионное уравнение, в котором остались ионы участвующие в реакции. | Ag+ + CI- = AgCI↓ |
| 7.Сделайте вывод. | Реакция ионного обмена прошла до конца с образованием белого осадка. Краткое ионное уравнение показывает между какими ионами фактически прошла реакция, связывание ионов в осадок. |
Ребята! Вы уже знаете, что ионы отличаются от атомов по строению и свойствам. Некоторые ионы бесцветные, другие окрашивают растворы в определенный цвет.
Цвет некоторых ионов:
Cu2+ - голубой Ni2+ - зеленый
Fe2+ - светло-зеленый Co2+ - розовый
Fe3+ - желто-коричневый MnO4- -фиолетовый
Когда такие ионы осаждают, они придают цвет веществу, которое выпадает в осадок. Например: чтобы осадить ионы Cu2+ из раствора, необходимо добавить раствор содержащий ОН-, в результате выпадает синий осадок Cu(ОН)2↓.
Cu2+ + 2ОН- = Cu(ОН)2↓
Такие реакции называют – качественные. Их использование помогает доказать наявность в растворе того или иного иона.
Лабораторный опыт №2: Реакции, в результате которых образуется газ.
В пробирку налить 2-3 мл раствора Na2CO3 и добавить немного HCI.
Задание: Составить молекулярное, полное ионное и сокращенное ионное уравнение.

 Na2CO3 + 2HCI = 2NaCI + H2 CO3 СО2↑ Молекулярное уравнение
Na2CO3 + 2HCI = 2NaCI + H2 CO3 СО2↑ Молекулярное уравнение
Н2О

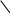
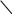 2Na+ + CO3 2- + 2H + 2CI- = 2Na+ + 2CI- + СО2 ↑ + Н2О Полное ионное уравнение
2Na+ + CO3 2- + 2H + 2CI- = 2Na+ + 2CI- + СО2 ↑ + Н2О Полное ионное уравнение
CO3 2- + 2H + = СО2 ↑ + Н2О Краткое ионное уравнение
Вывод: Реакция прошла до конца с выделением газа.
5.Первичное осмысление новых знаний.
Лабораторный опыт №3. Инструктивная карта.
Повторим правила безопасности:
1.Выполнять опыт по инструкции.
2.Работать над столом.
3.Быть внимательным и аккуратным.
4.Фиксировать результаты наблюдений.
| Лабораторный опыт | Уравнения реакций | Вывод или вопрос |
| №3: Реакции, в результате которых образуется малодиссоциирующее вещество. Задание: В пробирку налейте 2-3 мл NaОН, добавить 1-2 капли фенолфталеина. Цвет изменился на малиновый. Прилейте раствор HCI до обесцвечивания раствора.
|
|
|
6. Закрепление знаний и способов действий.
Пользуясь алгоритмом составьте уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде, которые протекают до конца:
| Реагирующие вещества | Уравнения реакций |
| молекулярное | Полное ионное | Сокращенное ионное |
| 1.Гидроксид натрия и сульфат меди(II)
|
|
|
|
| 2.Сульфит натрия и соляная кислота |
|
|
|
| 3.Гидроксид калия и азотная кислота |
|
|
|
| 4.Хлорид магния и сульфат натрия |
|
|
|
7. Подведение итогов урока.
Сегодня на уроке, опытным путем, мы наблюдали механизм протекания ионных реакций, идущих до конца, ознакомились со свойствами ионов.
8.Домашнее задание. Параграфы 6,7
9. Рефлексия.
- На уроке я научился(лась) –
- Испытывал(а) трудности, когда –
-Мое настроение к концу урока …
-Я считаю, что урок прошел …






 Чем обусловлена электропроводность растворов?
Чем обусловлена электропроводность растворов?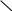
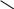
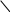
 Ag+ + NO3 - + Na + + CI- = AgCI ↓+ Na+ + NO3-
Ag+ + NO3 - + Na + + CI- = AgCI ↓+ Na+ + NO3-
 Na2CO3 + 2HCI = 2NaCI + H2 CO3 СО2↑ Молекулярное уравнение
Na2CO3 + 2HCI = 2NaCI + H2 CO3 СО2↑ Молекулярное уравнение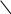

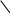
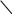 2Na+ + CO3 2- + 2H + 2CI- = 2Na+ + 2CI- + СО2 ↑ + Н2О Полное ионное уравнение
2Na+ + CO3 2- + 2H + 2CI- = 2Na+ + 2CI- + СО2 ↑ + Н2О Полное ионное уравнение









