Открытая Конференция исследовательских и проектных работ учащихся
«Исследователь нового века»
Секция: юный исследователь
Исследовательская работа
Эффективность Цинк-Гальва-Спрея от коррозии
Выполнил: Кожевников Артем,
ученик 6 класса образовательного центра «Академия Мир»
Руководитель: Феклисова Ольга Витальевна, заместитель директора по УВР и безопасности образовательной деятельности, учитель химии ГБОУ УР «Лицей № 41»
Ижевск, 2026
Оглавление
Введение 3
Глава 1. Что такое коррозия 5
1.1. Как происходит коррозия 5
1.2. Способы защиты металлов от коррозии 7
2. Практическая часть 10
Заключение 17
Список источников информации 19
Введение
Актуальность: Современная жизнь человека невозможна без металлов. Из них изготавливаются транспортные средства: от велосипедов до самолетов, промышленное оборудование: от простого молотка до высокоточных станков, стройматериалы: от гвоздей до сложных строительных конструкций, различные приборы, в том числе электроника, а также посуда, украшения и прочее. К сожалению, окружающая среда может воздействовать на изделия из металла, что может привести к их разрушению.
Ежегодно до 20% выплавленного металла и воплощенного в конструкции и различные изделия (мосты, автомобили, теплоходы, трубы, болты и т.д.) разрушаются от коррозии. Коррозия ежегодно уничтожает до 3 % ВВП (валовой внутренний продукт) России - три триллиона рублей буквально растворяются в ржавчине [4]. Несколько примеров: «Катастрофа в Норильске в 2020 году. 20 000 тонн дизельного топлива вытекло из резервуара на ТЭЦ-3 и разлилось по окрестностям. 6 000 тонн ушли в грунт и отравили подземные воды, отдельные ядовитые «хвосты» протянулись до самого Карского моря. Причина - коррозия, которая за несколько лет успела источить стенку резервуара, в котором хранилось топливо» [8] В 2005 году в Чусовом (Пермский край) обрушилась крыша бассейна «Дельфин». Погибло 14 человек, из них 10 детей. Следствие установило: разрыв несущей балки, металл которой был полностью поражён коррозией. [3] Обе катастрофы показали: недооценка коррозии превращает инженерную ошибку, неполадку в экологическую катастрофу, в человеческую трагедию.
Для защиты металлов от коррозии разработано множество методов, которые направлены на изменение свойств металла, свойств окружающей среды или характера взаимодействия металлического изделия и среды на границе контакта. Все ли методы эффективны?
Цель исследования: Определить эффективность Цинк-Гальва-Спрея для защиты железных гвоздей от коррозии в различных средах: кислой, нейтральной и щелочной.
Гипотеза: предполагаем, что Цинк-Гальва-Спрей (далее спрей) предназначен для защиты металлических изделий от коррозии в пресной воде, он не защитит железные гвозди в кислой и щелочной среде, так как цинк более активный металл, чем железо.
Объект исследования: эффективность Цинк-Гальва-Спрея для защиты железных гвоздей от коррозии.
Предмет исследования: зависимость эффективность Цинк-Гальва-Спрея для защиты железных гвоздей от коррозии от среды растворов: кислой, нейтральной и щелочной.
Задачи:
Узнать, как происходит коррозия, какие есть способы защиты металлов от нее.
Экспериментальным путем выявить процесс образования коррозии на железных гвоздях, обработанных спреем, и не обработанных в растворах: соды, уксуса и фильтрованной воде.
Глава 1. Что такое коррозия Как происходит коррозия
Коррозия – это самопроизвольное разрушение материалов и изделий из них под воздействием различных состояний окружающей среды [2,6].
Примеры:
ржавчина на стали
зеленый налет на меди
Есть два основных вида коррозии: химическая и электрохимическая.
Химическая коррозия происходит в среде, которая не проводит электрический ток. Металл разрушается под действием окислителей — неэлектролитов, например, газов (кислорода, хлора и других) при повышенной или даже обычной температуре. Процесс происходит на границе фаз "металл - окружающая среда". Например, если оставить железный гвоздь на воздухе, со временем он начнёт ржаветь — это и будет химическая коррозия [6].
4Fe + 3O2 + 6H2O 4Fe(ОН)3
Реакция превращает металл в другой материал: железо превращается в гидроксид железа (порошок красно-коричневого цвета), теряя прочность.
Для течения коррозии железа достаточно присутствия воды и воздуха. В результате во влажном воздухе на железе образуется неплотный, рыхлый слой ржавчины, пронизанный многочисленными трещинами и порами, сквозь которые легко проникают воздух и влага, вызывая дальнейшее разрушение металла. [2,6].
Электрохимическая коррозия – это вид коррозии, связанный с протеканием электрохимических реакций на поверхности металла или его сплава при их контакте с раствором электролита. Электролиты - это вещества, растворы которых проводят электрический ток (например, минеральные соли, содержащиеся в морской воде, растворы кислот, щелочей). Особенно активно электрохимическая коррозия развивается при контакте металлов разной активности. [5,6].
Например, если соединить два металла (цинк и железо), и погрузить их в воду, начнётся электрохимическая коррозия (связано с переходом электронов). У цинка и железа разная химическая активность - склонность к отдаче электронов: цинк более активно отдаёт электроны, чем железо. В такой ситуации: цинк будет анодом - участком, где происходит окисление металла (отдача электронов): железо будет катодом - участком, где электроны принимаются. (рис.1).
В водной среде электроны переходят от цинка к железу. Из-за этого цинк разрушается (растворяется), а железо защищено от коррозии. Этот процесс называется гальванической коррозией. [6].
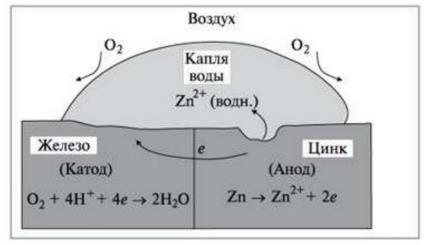
Рисунок 1. Схема электрохимической коррозии при контакте железа и цинка. [6].
Таким образом, при контакте двух разных металлов в водной среде более активный металл (в данном случае цинк) «жертвует» собой, защищая менее активный металл (железо) от разрушения.
Главное отличие в том, что химическая коррозия происходит в среде, не проводящей электрический ток, а электрохимическая — в растворах, которые могут проводить электрический ток. Также при химической коррозии не происходит перехода электронов, а при электрохимической — происходит.
Активаторами коррозии являются растворы солей, кислот, перепады температуры окружающей среды и наличие примесей в металле. [2,6].
Итак, коррозия — это серьёзная проблема, которая может привести к разрушению металлических конструкций, например, мостов или труб. Поэтому люди придумывают разные способы защиты металлов от коррозии, например, покрывают их красками или специальными веществами и др. [5,6].
Способы защиты металлов от коррозии
Для защиты металлов от коррозии используют разные способы, которые включают легирование, нанесение защитных покрытий, изменение состава среды и электрозащиту. Полностью исключить коррозию невозможно, но можно замедлить её с помощью этих методов. [6,7].
Защитные покрытия (неметаллические): Нанесение красок, лаков, эмалей, смазок или полимеров (резина, пластик, водоотталкивающие спреи) для изоляции от влаги и воздуха.
 Рисунок 1. Радиатор, покрытый краской. [6]
Рисунок 1. Радиатор, покрытый краской. [6]
Металлические покрытия: Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. Например, лужение — это нанесение на поверхность стали тонкого слоя олова. Применяют также оцинковывание, хромирование, никелирование, позолоту и т. д. [6,7].
 Рисунок 2. Хромированное изделие [6]
Рисунок 2. Хромированное изделие [6]
Легирование: это введение в состав сплава веществ, повышающих его устойчивость к коррозии. В качестве таких добавок используются металлы, которые на воздухе покрываются оксидной плёнкой. Это хром, никель, алюминий, вольфрам, молибден, титан и другие. Наиболее известные легированные сплавы - нержавеющие стали, из которых изготавливают медицинские инструменты, кухонную посуду, детали машин. [6,7].
 Рисунок 3. Хирургические инструменты [6]
Рисунок 3. Хирургические инструменты [6]
Использование коррозионностойких материалов (нержавеющих сталей, содержащих специальные добавки). Этот метод защиты от коррозии считается самым надёжным.
Протекторная защита (один из способов электрохимической защиты): заключается в прикреплении к металлическому изделию кусков более активного металла (протектора). Например, к стальным трубопроводам, корпусам кораблей приваривают магний или цинк. Более активный металл (протектор) разрушается, а сталь от коррозии защищена. Например, оцинкование. Это самый распространенный и самый эффективный способ защиты железа от коррозии. [6,7].
 Рисунок 4. Протекторная защита [6]
Рисунок 4. Протекторная защита [6]
Используются также заклёпки или детали из протектора. На фотографии показано использование протектора для защиты корпуса лодки. Детали из более активного металла окисляются, на них заметен налёт продуктов коррозии. Стальные части корпуса защищены, следов ржавления не видно [6,7].
Универсальных методов нет — их подбирают для каждого конкретного объекта, исходя из условий эксплуатации, параметров защищаемого металла и других факторов [5]
Практическая часть
Методику проведения эксперимента разработали на основе предложенных экспериментов в кейсе «Внимание, коррозия» из Тетради кейсовых практик: опыт самостоятельных исследований в 7-8 классах [1]
Для эксперимента взяли 24 строительных гвоздя, помыли их с мылом и прокипятили в сковороде (рис.5). Половину гвоздей обработали цинковым спреем. К гвоздям, обработанным спреем, привязали зеленые нитки, к необработанным спреем гвоздям, привязали малиновые нитки.


Рисунок 5. Процесс подготовки гвоздей к эксперименту – кипячение в сковороде. Фото автора.
Рисунок 6. Баллон с Цинк-Гальва-
Спреем. Фото автора
Характеристика Цинк-Гальва-Спрея: предназначен для длительной защиты всех металлических поверхностей (рис.6). Он защищает металлы от коррозии и ржавчины; быстросохнущий и образует плотное сцепление. Покрытие устойчиво к пресной и соленой воде, а также при температуре до +3000С.
23.02.2026 г. в 6 пластиковых бутылок налили равные объемы (0,45 л.) различных жидкостей:
Фильтрованную воду в две бутылки;
Фильтрованную воду с содой (1 чайная ложка) в две бутылки;
Фильтрованную воду с уксусом (1 столовая ложка 9% уксуса) в две бутылки.
Воду пропустили через кувшин с фильтром Аквафор А5 (очищает от хлора, бактерий, нормализует минеральный состав).
Ход эксперимента:
Поместили в каждую бутылку по 4 гвоздя: два гвоздя, опущены в раствор полностью, два гвоздя находятся в жидкости наполовину (смоделировали ситуацию, когда металл контактирует и с жидкостью, и с воздухом).
В три бутылки поместили необработанные гвозди, в три другие – гвозди, покрытые спреем (время отверждения покрытия выдержали 24 ч).
6 бутылок поставили в одном месте (на подоконнике), хранили при комнатной температуре в течение 2 недель.
Наблюдали за изменениями визуально, через оболочку бутылок. Через две недели вынули гвозди из всех бутылок за концы ниток. Фотографировали. Еженедельно не доставали гвозди из растворов, чтобы не было контакта с воздухом тех гвоздей, которые находились в жидкости. Данные наблюдений представлены в фотографиях (рис. 7-22).
Результаты наблюдений:
За 1 неделю в бутылках изменился цвет растворов, кроме растворов с содой (рис.7). В бутылках с водой и раствором уксуса, в которых помещены необработанные гвозди, на дне виден красно-коричневый осадок, на гвоздях виден красно-коричневый или черный налет. На необработанных гвоздях, находящихся в растворе соды есть небольшие участки со следами коррозии. На обработанных спреем гвоздях, помещенных в раствор уксуса и воду, видны единичные небольшие участки металла, подверженные коррозии; сами растворы стали слегка желтоватые. На гвоздях с защитным цинковым слоем, находящихся в растворе соды, следы коррозии видны только на участках рядом с нитками.

Рисунок 7. Результаты эксперимента через неделю – 1 марта. Фото автора
Вывод: скорость коррозии на гвоздях, обработанных Цинк-Гальва-Спреем, за первую неделю намного ниже, это видно во всех исследуемых средах.
| Результаты эксперимента через две недели – 9 марта |
| 
| Рисунок 8. необработанные гвозди находились в фильтрованной воде. | 
| Рисунок 9. необработанные гвозди находились в растворе уксуса. | 
| Рисунок 10. необработанные гвозди находились в растворе соды |
| Результаты эксперимента через две недели – 9 марта |
| 
| Рисунок 11. обработанные спреем гвозди находились в фильтрованной воде. | 
| Рисунок 12. обработанные спреем гвозди находились в растворе уксуса. | 
| Рисунок 13. обработанные спреем гвозди находились в растворе соды |
Полученные результаты и их обсуждения:
За две недели наблюдений растворы соды не изменили свой цвет, остались прозрачными, но на гвоздях, обработанных спреем (рис. 13, табл.1) появились следы коррозии. Это можно объяснить тем, что цинк в отличие от железа может растворяться в растворах со щелочной средой. Но у нас очень слабый раствор соды, поэтому реакция началась не сразу и протекает медленно. Когда цинк растворяется в щелочной среде, и железо остается без защиты - создается контакт двух металлов в растворе – это пример электрохимической коррозии. А на необработанных гвоздях (рис.10, табл.1) практически нет очагов коррозии, потому что на железе в щелочной среде образуется невидимая защитная пленка из соединений железа.
В растворе уксусной кислоты железо сразу начинает растворяться, образуя соли железа красно-коричневого цвета, которые покрывают гвозди, а избыток их падает на дно бутылки (рис. 9, табл.1). Уксусная кислота растворяет и гвозди, покрытые цинком (рис. 12, табл.1); но сначала растворяется цинк, образовавшиеся соли которого бесцветные, а только потом начинается реакция кислоты с железом, когда растворилась защитная пленка (это пример электрохимической коррозии). Поэтому этот раствор кислоты окрасился не так интенсивно, стал желто-коричневым. Но это случаи не образование ржавчины – гидроксида железа, а образование других веществ.
В воде коррозия гвоздей, обработанных спреем и без защиты, началась уже через неделю (рис. 7, 8,11), значит, фильтрованная вода является той средой, в которой возможна коррозия металлов. В водопроводной воде есть растворенный кислород, есть примеси, которые ускоряют процесс коррозии. За две недели больше ржавчины образовалась в воде, где находились гвозди без защиты спреем (рис.8, табл.1). Покрытие Цинк-Гальва-Спреем не предотвратило образование коррозии, но очень замедлило процесс (рис.11, табл.1).
Таблица 1.
Результаты коррозии на гвоздях необработанных и обработанных цинковым спреем за 2 недели. Фото автора
| Гвозди находились 2 неделе в растворе уксуса |
| Гвозди без защитного покрытия | Гвозди с защитным цинковым покрытием |
| 
| 
| 
| 
|
| Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе | Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе |
Продолжение таблицы1.
Результаты коррозии на гвоздях необработанных и обработанных цинковым спреем за 2 недели. Фото автора
| Гвозди находились 2 неделе в фильтрованной воде |
| Гвозди без защитного покрытия | Гвозди с защитным цинковым покрытием |
| 
| 
| 
| 
|
| Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе | Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе |
| Гвозди находились 2 неделе в растворе соды |
| Гвозди без защитного покрытия | Гвозди с защитным цинковым покрытием |
| 
| 
| 
| 
|
| Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе | Гвозди контактируют и с жидкостью, и с воздухом | Гвозди полностью находятся в растворе |
По окончанию эксперимента все гвозди аккуратно вынули из растворов, поместили на бумагу для фотофиксации с использованием портативного цифрового микроскопа WiFi Bestson (увеличение в 50 раз).


Рисунок 14. Внешний вид железного гвоздя до обработки спреем. Фото автора
Рисунок 15. Внешний вид железного
гвоздя, обработанного Цинк-Гальва-Спреем. Фото автора
На фотографиях (рис.14, 15) хорошо видно, что покрытие спреем закрыло неровности на поверхности железного гвоздя.
В микроскоп посмотрели поверхность гвоздей, на которых образовалась ржавчина (рис. 16, 17, 18,19) – это красно-коричневое вещество, рыхлое.
| 
| 
| 
| 
|
| Рисунки 16-19. Очаги ржавчины на поверхности гвоздей, образовавшейся в фильтрованной воде. Фото автора |
На гвоздях, которые находились в растворе уксуса, образовалась не ржавчина (гидроксид железа), а другие соединения железа или цинка, они выглядят по-другому: соединения железа желто-коричневые, соединения цинка светлые. (рис. 20, 21).
| 
| 
| 
|
| Рисунок 20. Поверхность гвоздя, находившегося в растворе уксуса, покрытая соединением железа и уксусной кислоты. | Рисунок 21. Поверхность гвоздя, обработанного спреем, находившегося в растворе уксуса, покрытая соединением цинка и уксусной кислоты. | Рисунок 22. Поверхность железного гвоздя без цинковой защиты, находившегося в растворе соды |
Поверхность гвоздей без цинковой защиты, находившихся в растворе соды, без следов коррозии (рис.22), но отличается от начального вида (рис..14), значит на них образовалась защитная пленка.
Заключение В результате проведенного исследования можно сделать следующие выводы:
Коррозия – это процесс разрушения металлов под воздействием окружающей среды. Защитить металлы от коррозии можно водооталкивающими спреями, красками, лаками, металлическими покрытиями (цинкование, хромирование, позолот и др.)
В результате проведенного эксперимента выяснили, что процесс коррозии железа зависит от среды, в которой оно находится. Обработка железа Цинк-Гальва-Спреем замедляет коррозию, но не предотвращает её полностью, даже в фильтрованной водопроводной воде. Химические процессы, происходящие в разных средах, определяют скорость и характер коррозии железа.
В воде коррозия железа происходит быстрее на необработанных спреем гвоздях, так как созданы идеальные условия для образования ржавчины: контакт с водой и кислородом. Помимо растворенного в воде кислорода, коррозию могут усиливать растворённые соли и примеси. А для гвоздей с цинковой защитой важно сохранение целостности защитного слоя, если он нарушен тогда начинается образование ржавчины.
В кислоте происходит коррозия - растворение и железа, и цинка, но это не образование ржавчины, а образование солей железа и цинка. Коррозия обработанных спреем гвоздей начинается позже, только после растворения в кислоте защитного цинкового слоя.
В растворе соды (щелочной среде) гвозди без защитного цинкового покрытия практически не подверглись коррозии, так как на них образуется защитная пленка. На гвоздях, обработанных спреем, появились небольшие очаги ржавчины, так как цинк растворяется в щелочной среде, и железо остается без защиты. Создается контакт двух металлов в растворе – это пример электрохимической коррозии.
Наша гипотеза подтвердилась частично: Цинк-Гальва-Спрей, предназначенный для защиты металлических изделий от коррозии в пресной воде, не защитил железные гвозди ни в фильтрованной воде, ни в растворах уксуса и соды.
Список источников информации
Азбель А.А. Илюшин Л.С. Тетрадь кейсовых практик: опыт самостоятельных исследований в 7-8 классе. Часть 1.- СПб.: Школьная лига. 2014.
Беликова М.Ю. В царстве «Рыжего дьявола». Коррозия металлов. Защита от коррозии. /Я иду на урок химии: Книга для учителя. -М.: Издательство «Олимп», 1999
Катастрофа в "Дельфине" Под обрушившейся крышей бассейна погибли 14 человек - Текст: электронный. – URL: https://lenta.ru/articles/2005/12/05/dolphin/ (дата обращения 12.12.2025)
Когда ржавчина убивает: катастрофы из-за коррозии, ставшие уроком для инженеров. - Текст: электронный. – URL: https://dzen.ru/a/aU5yVNJHaSg_KWB8 (дата обращения 12.12.2025)
Коррозия «Для чайников». Канал «Инженерные знания» - Текст: электронный. – URL: https://dzen.ru/a/XzONXJptnXEiW7-1 (Дата обращения 01.02.2025)
Коррозия металлов и её виды. - Текст: электронный. – URL: https://www.yaklass.ru/p/himija/11-klass/metally-7200709/khimicheskaia-i-elektrokhimicheskaia-korroziia-sposoby-zashchity-metall_-7161830/re-298a6a26-2b64-482f-a902-36d532986008 (дата обращения 20.01.2026)
Коррозия металлов и способы защиты от нее. - Текст: электронный. – URL: https://chemege.ru/korroziya/ (дата обращения 20.01.2026)
Цинкевич М. «Съела коррозия»: крупнейшие катастрофы мира, случившееся из-за обыкновенной ржавчины. - Текст: электронный. – URL: https://vc.ru/flood/200262-sela-korroziya-krupneishie-katastrofy-mira-sluchivsheesya-iz-za-obyknovennoi-rzhavchiny (дата обращения 12.12.2025)







 Рисунок 1. Радиатор, покрытый краской. [6]
Рисунок 1. Радиатор, покрытый краской. [6] Рисунок 2. Хромированное изделие [6]
Рисунок 2. Хромированное изделие [6] Рисунок 3. Хирургические инструменты [6]
Рисунок 3. Хирургические инструменты [6] Рисунок 4. Протекторная защита [6]
Рисунок 4. Протекторная защита [6]







































