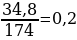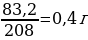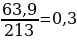Итоговая (стандартизированная) контрольная работа по химии
за курс «Химия. 9 класс»
Вариант № 1
А1. Распределение электронов по энергетическим уровням 2е, 8е, 2е соответствует частице 1) Мg0 2) О2- 3) Мg2+ 4) S2-
А2. В ряду элементов Na – Mg – Al - Si
-
уменьшаются радиусы атомов
-
уменьшается число протонов в ядрах атомов
-
увеличивается число электронных слоёв в атомах
-
уменьшается высшая степень окисления атомов в соединениях
А3. Фактор, не влияющий на скорость химических реакций,
-
природа реагирующих веществ
-
температура
-
концентрация реагирующих веществ
4)тип химической реакции
А4. Наиболее электропроводным металлом из перечисленных является
-
цинк 3) свинец
-
медь 4) хром
А5. Металл, не относящийся к щёлочноземельным,
1)магний 3) стронций
2)кальций 4) барий
А6. Наиболее активно реагирует с водой
-
скандий 3) калий
-
магний 4) кальций
А7. Агрегатное состояние иода при нормальных условиях
-
жидкое 2) твёрдое 3) газообразное
А8.Металл, с которым не взаимодействует концентрированная серная кислота,
1)железо 2)магний 3)цинк 4)натрий
Часть В. Тестовые задания на соответствие.
В1. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
Реагирующие Продукты их
вещества взаимодействия
А) Cu +Cl2 1) Cu(OH)2 и Cl2
Б) CuО + HCl 2) CuCl
В) Cu 2О + HCl 3) CuCl2 и H2O
4) CuCl2
5) CuCl и H2O
В2. Установите соответствие между типами и уравнениями химических реакций.
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
А) соединения, ОВР, необратимая
Б) разложения, ОВР, эндотермическая
В) соединения, ОВР, гомогенная
УРАВНЕНИЯ РЕАКЦИЙ
-
N2(г) + 3H2(г) ↔ 2NH3(г) + Q
-
2КNO3 = 2KNO2 + O2 +Q
-
FeO + C → Fe + CO -Q
-
4Fe + 3O2 + 6H2O = 4Fe(OH)3
-
2Al + Fe2O3 = 2Fe + Al2O3 +Q
Часть С. Задания с развёрнутым ответом.
С1. Запишите уравнения реакций, с помощью которых можно осуществить превращения Zn → ZnCl2 → Zn(OH)2 → ZnO
Для перехода 2 запишите ионное уравнение.
С2. . К 34,8г сульфата калия прилили раствор, содержащий 83,2 г хлорида бария. Определите массу образовавшегося осадка. (5б).
С3.Расставьте коэффициенты в уравнении реакции с помощью электронного баланса. Cu +HNO3→Cu(NO3)2+NO +H2O.
Итоговая (стандартизированная) контрольная работа по химии за курс «Химия. 9 класс».
Вариант № 2
А1. Распределение электронов по энергетическим уровням 2е, 8е, 6е соответствует атому
-
углерода 3) фосфора
-
серы 4) хлора
А2. В ряду элементов С –N - О - F
-
уменьшается высшая степень окисления элементов в соединениях
-
увеличиваются радиусы атомов
-
уменьшается восстановительная способность простых веществ
-
увеличивается высшая степень окисления элементов в соединениях
А3. Фактор, не влияющий на скорость химических реакций,
-
катализатор
-
способ получения реагентов
-
природа реагирующих веществ
-
концентрация реагирующих веществ
А4. Металл, не относящийся к щелочным металлам,
-
калий 3) литий
-
кальций 4) натрий
А5. Свойство ртути, которое ограничивает её применение в бытовых термометрах
-
агрегатное состояние
-
температура плавления
-
токсичность
-
высокая плотность
А6. Водород нельзя получить путём взаимодействия металлов с кислотой
-
азотной 3) соляной
-
серной 4) фосфорной
А7. Свойство, характерное для озона,
-
хорошо растворяется в воде
-
не имеет запаха
-
бактерициден
-
легче воздуха
А8. Вода взаимодействует с каждым из веществ, формулы которых
1)Ca и Na2O 2) Na2O и Cu 3)CuO и N2O5 4)ZnO и SO2
Часть В. Тестовые задания на соответствие.
В2. Установите соответствие между исходными веществами и продуктами реакций.
Исходные вещества Продукты реакции
А) Na и H2O 1) Na2SO3 и H2O
Б) Na2O и H2O 2) NaOH и H2O
В ) NaOH и SO2 3) NaOH и H2
4) NaOH
В2. Установите соответствие между типами и уравнениями реакций.
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
А) замещения, ОВР, эндотермическая
Б) разложения, ОВР, экзотермическая
В) соединения, ОВР, необратимая
УРАВНЕНИЯ РЕАКЦИЙ
-
N2(г) + 3H2(г) ↔ 2NH3(г) + Q
-
2КNO3 = 2KNO2 + O2 +Q
-
FeO + C → Fe + CO -Q
-
4Fe + 3O2 + 6H2O = 4Fe(OH)3
-
2Al + Fe2O3 = 2Fe + Al2O3 +Q
Часть С. Задания с развёрнутым ответом.
С1. Запишите уравнения реакций, с помощью которых можно осуществить превращения MgO→ MgCI2→Mg(OH)2→ Mg(NO3)2
Для перехода 3 запишите ионное уравнение.
С2. К раствору, содержащему 63,9г нитрата алюминия, прилили раствор, содержащий 39,2г фосфорной кислоты. Определите массу фосфата алюминия.
С3. Расставьте коэффициенты в уравнении реакции с помощью электронного баланса. Cu + HNO3→ Cu(NO3)2 + NO2 + H2O
Рекомендации по оцениванию работы
Максимальное количество баллов – 21 балл
Задания базового уровня (А1-А8), только один правильный ответ. (1 балл)
Задания повышенного уровня (В1-В2), найти соответствие. (2 балла)
Задание С1, С2, С3 - требуют полного ответа. (3 балла)
Соответствие баллов, полученных за выполнение заданий, отметке/оценке по пятибалльной шкале оценивания
| Отметка | 2 | 3 | 4 | 5 |
| Число баллов за работу | 0-9 | 10-13 | 14-17 | 18-21 |
Ответы: Итоговая (стандартизированная) контрольная работа по химии за курс «Химия. 9 класс
| Вариант 1. Часть А. -
1 -
1 -
4 -
1 -
1 -
3 -
2 -
1
Часть В. -
А-4, Б-3, В-5. -
А-4, Б-2, С- 1. Часть С. 1. -
Zn + Cl2 = ZnCl2 -
ZnCl2 + 2KOH = Zn(OH)2 + 2KCl -
Zn(OH)2 = ZnO + H2O
2. Задача 34,8г 83,2г х К2SO4 + BaCl2 → BaSO4 + 2KCl 1*174г 1*208г 1*233
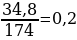 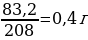
Х = 0,2*233 = 46,6г
-
3. 3Cu⁰+8HN⁺⁵O3(разб.)=3Cu⁺²(NO3)2+2N⁺²O+4H2O
Сu⁰ - 2e⁻ = Cu⁺² | 3 - восстановитель
N⁺⁵ + 3e⁻ = N⁺² | 2 - окислитель
| Вариант 2 Часть А. -
3 -
3 -
2 -
2 -
3 -
1 -
3 -
1
Часть В. -
А-3, Б-4, В-1. -
А-3, Б-2, В- 4. Часть С. 1. MgO+2HCl=MgCl2+H2O MgCl2+2KOH=Mg(OH)2+2KCl Mg(OH)2+2HNO3=Mg(NO3)2+2H2O
2. Задача 63,9г 39,2г х Al(NO3)3 + H3PO4 → AlPO4 + 3HNO3 1*213г 1*98г 1*122г
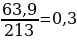 
Х = 0,3*122 = 36,6г
3. Cu⁰+4HN⁺⁵O3(конц.)=Cu⁺²(NO3)2+2N⁺⁴O2+2H2O
Сu⁰ - 2e⁻ = Cu⁺² | 1 - восстановитель
N⁺⁵ + e⁻ = N⁺⁴ | 2 - окислитель
|