Тема: Изопроцессы.
Цели урока:
Образовательные:выяснение условий выполнения изопроцессов; выяснение теоретической зависимости между двумя термодинамическими параметрами при неизменном третьем; практическое доказательство полученного закона.
Воспитательные: Умение планировать и анализировать свою деятельность, воспитание бережного отношения к техническим средствам обучения и мебели кабинета, организованности на уроке, формирование умения рационального использования своего времени.
Тип урока - изучение нового материала.
Ход урока
Учитель: На протяжении нескольких последних уроков мы с вами изучаем основные положения и закономерности «Молекулярно-кинетической теории идеального газа». Сегодня мы приступаем к изучению заключительной темы данной главы. И так открываем тетради, записываем тему урока: «Изопроцессы».
Учитель: Но прежде чем приступить к изучению нового материала я предлагаю сформулировать задачи урока.
Задачи: Выяснить:
Что называется изопроцессом;
Какие изопроцессы возможны.
Дать определение и вывести математические выражения для каждого изопроцесса.
Проверить экспериментально правильность полученного закона.
Научиться применять газовые законы при решении задач.
Учитель: На прошлом уроке мы с вами вывели уравнение состояния идеального газа, связывающее между собой три макроскопических параметра данной массы газа.
Фронтальный опрос:
Как называется это уравнение?
Какие макроскопические параметры связывает данное уравнение?
Записать математическое выражение данного уравнения.
Какие макроскопические параметры следует знать для однозначного определения состояния идеального газа? (при ответе учащихся на данный вопрос макроскопические параметры идеального газа по парно в три колонки записываются на доске (p,V), (p, T), (VT), а подними записывается третий параметр, который определяется с помощью уравнения Клайпейрона - Менделеева).
Изучение нового материала
Учитель: Многие процессы изменения состояния газа в природе и в тепловых машинах происходят так, что один из трех макроскопических параметров (объем, давление или температура) остается (или специально поддерживается) постоянным. Два других параметра при этом изменяется. Такие процессы называются изопроцессами.
Изопроцессы- процессы изменения состояния газов так, что один из трех макроскопических параметров (объем, давление, температура) остается постоянным, а два других параметра при этом изменяются.
а) Изотермический процесс- процесс изменения состояния определенной массы газа при постоянной температуре (m=const, T=const). Из уравнения Менделеева-Клайперона следует закон Бойля-Мариотта PV=CONST=m/V* RT. Это означает, что произведение начального давления Р1 на его первоначальный объем равно произведению этих параметров P2*V2 в произвольной момент времени P1*V1=P2*V2или P1/P2=V2/V1 следовательно Р - 1/V график- гипербола, название - изотерма.
б) Изобарный процесс - процесс изменения состояния определенной массы газа при постоянном давлении (m=const, P=const).Из уравнения Менделеева - Клайперона следует закон Гей-Люссака. V/T=const=mR/MP-это означает, что отношение первоначального объема газа к его температуре Т1 равно отношению этих параметров V2/T2 в произвольный момент времени. V1/T1=V2/T2 или V1*T2=V2*T1 следует V~T.
График - прямая, название - изобара.
в) Изохорный процесс - процесс изменения состояния определенной массы при постоянном объеме(m=CONST, V= CONST). Из уравнения Менделеева - Клайперона следует закон Шарля Р/ Т=const=mR/MV - это означает, что отношение первоначального давления газа Р1 к его температуре равно отношению этих параметров Р2, Т2- в произвольный момент времени Р1/Т1=Р2/Т2 или Р1*Т2=Р2*Т1 следует Р пропорционально Т. График - прямая, название- изохора.
По ходу урока ребята заполняют таблицу:
| Название процесса | Постоянная величина | Ученые, год открытия | Формулировка закона | Запись формулы | Графики изменения P, V, T в осях: |
| P, V | P, T | V, T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Закрепление(работа в парах)
Цель работы: экспериментальным путем проверить верность закона Гей-Люссака (доказать постоянство отношения V/T для данной массы газа).
Виртуальная лаборатория «Исследование изобарного процесса в газах» - http://efizika.ru/html5/18/index.html.
Установка моделирует лабораторную работу «Проверка закона изобарного процесса Гей-Люссака».
Ход работы
Данные исследования занести в таблицу:
| № | М, кг/моль (молярная масса) | m,кг (масса газа) | P0, кПа (давление | V0, м3 (объем | t0,С (температура по Цельсии) | T0,К (температура Кельвина) | V, м3 (объем | t,С (температура по Цельсии) | T,К (температура Кельвина) | V/T, м 3 /К | V0/T0, м 3 /К |
|
|
|
|
|
|
|
|
|
|
|
|
|
Сформулировать вывод.
Подведение итогов
Домашнее задание
§ 65,66, решить задачи 2, стр.220
Подготовиться к теоретическому зачёту:по теме «Газовые законы».
| № | Вопрос | Процесс |
| Изотермический | Изобарный | Изохорный |
| 1 | Определение Процесса | Процесс изменения состояния термодинамической системы при постоянной температуре | Процесс изменения состояния термодинамической системы при постоянном давлении | Процесс изменения состояния термодинамической системы при постоянном объеме
|
| 2 | Условия применения | А) газ идеальный Б)m=const В) | А) газ идеальный Б)m=const В) | А) газ идеальный Б)m=const В) |
| 3 | Закон- Формула | А) Б) В) | А) Б) В) | А) Б) В) |
| 4 | Закон- Формулировка | Для газа данной массы произведение давления на объём постоянно, если температура газа не меняется | Для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется | Для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется
|
| 5 |
| Закон Бойля- Мариотта | Закон Гей-Люссака | Закон Шарля |
| 6 | График | 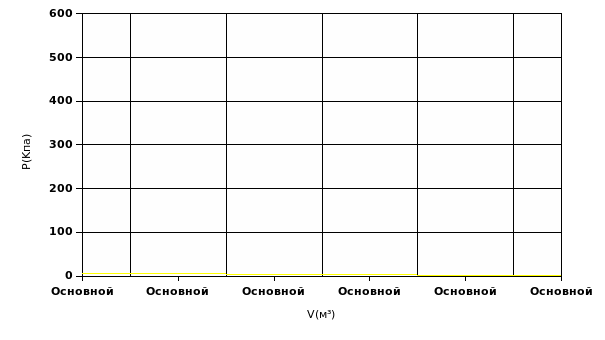 | 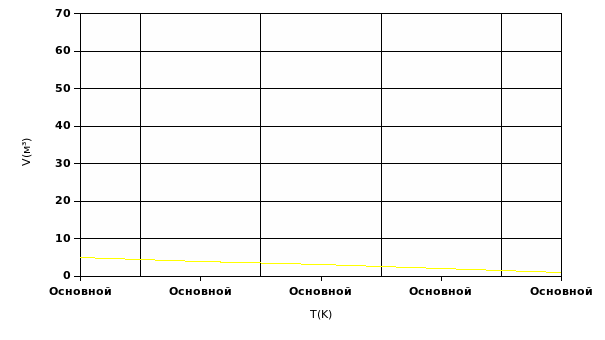 | 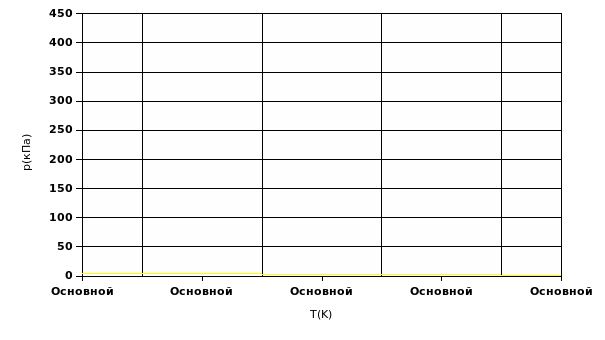 |
|
| Что показывает график |
|
|
|
|
|
|
| Тип зависимости |
|
|
|
|
| Вид графика |
|
|
|
|
| Название | Изотерма | Изобара | Изохора |
|
| Положение аналогичных линий |
|
|
|
| 7 | Другие сведения |
| При Т→Таб.нуля , изобары сходятся к точке О, но это не означает, что объём газа обращается в О; газ превращается в жидкость, в которой закон для идеального газа не применим. | Все изохоры начинаются в точке Т=О, это означает: при абсолютном нуле температуры(Т=О), давление газа равно О (Р=О) |
| 8 | Пример проявления | А) Сжатие воздуха компрессором; Б) расширение газа под поршнем насоса при откачивании газа из сосуда.
| Расширение газа в цилиндре с подвижным поршнем при нагревании цилиндра. | Нагревание газа в любой закрытой емкости, например в электрической лампочке при её включении. |




















