Методическая разработка внеклассного мероприятия
" Химическими тропками…".
Цели:
Обобщение знаний по курсу химии за класс и умение применять их в нестандартных условиях.
Развитие навыков логического и абстрактного мышления, умение обобщать, проводить аналогии, включать интуицию, воображение.
Развивать кругозор учащихся и повышать познавательный интерес к изучению предмета.
Продолжить формирование навыков коммуникативной и самостоятельной деятельности учащихся.
Воспитывать умение работать коллективно, оценивать свои возможности и зная товарищей.
Девиз: “Незнающие – пусть научатся, а знающие вспомнят еще раз”.
Ход мероприятия
Первый конкурс: «Давайте познакомимся». (максимальное количество баллов -10)
Второй конкурс : «Перестрелка». (максимальное количество баллов -5)
Третий конкурс : «Химики – аналитики». (максимальное количество баллов -10)
Четвертый конкурс : « Химиков – технологов». (максимальное количество баллов -10)
Пятый конкурс : « Ребус». (максимальное количество баллов -15)
Шестой конкурс : « Угадайка». (максимальное количество баллов -6)
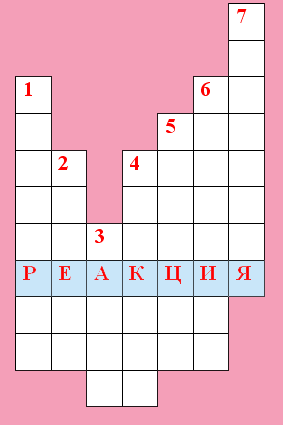
Седьмой конкурс : « Кроссворд». (максимальное количество баллов - 20)
Восьмой конкурс : « Самое сильное звено». (максимальное количество баллов - 44)
Девятый конкурс со зрителями: «Загадки».
1 ученик:
Что? Почему? Зачем? И где?
Живут в земле, в огне, в воде.
Вот в первый раз огонь добыт.
2 ученик: А почему огонь горит?
1 ученик: Зерно под солнцем проросло.
2 ученик: Зачем растению тепло?
1 ученик:
Дым легкий, а скала тверда.
Что значит “лед”, а что “вода”?
Что? Почему? Зачем? И где?
Мы все узнать хотим.
Соль растворяется в воде,
А мел нерастворим.
2 ученик:
Бумага не горит дотла,
В печи останется зола.
А если медь в печи нагреть –
То станет тяжелее медь
С окалиною вместе.
Не верите – так взвесьте!
1 ученик:
Открытый путь – нелегкий путь,
Но человеку не свернуть.
Что? Почему? За ним следят,
Чтоб шел вперед, а не назад.
Вот почему из года в год
Наука движется вперед.
учитель: Именно поэтому мы в очередной раз собрались с вами вместе, чтобы снова и снова окунуться в секреты удивительной науки “химия” и постараться ответить на новые “что?”, “где?”, “когда?”, “зачем?”. Так как эти вопросы должны сопровождать каждого человека, желающего достигнуть определенного роста в своем развитии, а также успехов в различных областях науки.
учитель: Мы приветствуем всех собравшихся в этом зале.
учитель: Итак, в нашем сегодняшнем марафоне “по удивительным химическим дорожкам” участвует 2 команды, в которых собрались представители всех классов нашей школы. Ну а оценить ваши результаты нам поможет жюри.
1 ученик:
Мы рады в нашей школе дорогим гостям.
И маленьким, и взрослым, и учителям.
Вы робость и тревогу прочь гоните,
А лучше все, на что способны, покажите.
2 ученик: Ну а жюри просим к нам не строгим быть, и очень честно оценить.
учитель: Итак, наш первый конкурс: “Давайте познакомимся”.
Командам предлагается дать название своей команды, девиз, маленькую защиту.
Защита команд.
1 ученик:
Как вы химию учили?
Долго ли ее зубрили,
Долго ль голову ломали
Над задачами сидя?
2 ученик:
Вокруг тебя творится мир живой,
Входи в него, вдыхай, руками трогай.
Есть просто газ – легчайший водород,
Есть просто кислород, а вместе это –
Июньский дождь от всех своих щедрот,
Сентябрьские туманы на рассветах.
1 ученик:
Кипит железо, серебро, сурьма
И темно бурые растворы брома,
И, кажется, вселенная сама
Одной лабораторией огромной.
учитель: Следующий конкурс, «Перестрелка». Команды по очереди задают друг другу 5 вопросов, за каждый правильный ответ по 1 баллу
1 команда
1.Способ превращать одно вещество в другое искали давно. Как называли алхимики вещество, с помощью которого надеялись превратить в золото что –нибудь иное ? (Филосовский камень)
2. Самое распространенное вещество на земле, присутствующее во всех организмах, основа всех жизненных процессов, единственный источник кислорода в процессе фотосинтеза (вода)
3. Как определить наличие крахмала в продукте (капля йода – посинение продукта)
4. Как называется токсичный туман (смог)
5. Мел, мрамор, известняк. Что их объединяет? (Состав. Все они являются карбонатом кальция)
2 команда
1. Недостаток какого галогена в организме вызывает кариес? (фтора)
2. Как называется превращение солнечной энергии в химическую в растениях ( фотосинтез)
3. Какое соединение серы имеет запах тухлых яиц? (сероводород)
4.Как называется разрушение металла под воздействием окружающей среды? (коррозия)
5. Кто из русских учёных сказал: « Нефть – не топливо, топить можно и ассигнациями» ? (Д.И. Менделеев)
Ответы команд.
Итоги конкурса.
2 ученик:
Здесь на химических дорожках
Следы химических веществ,
Протопал моль на тонких ножках,
Зашел и в школьный он подъезд.
Здесь стол стоит, пробирок полный,
В пробирках тех реакций волны,
Дым из них валит густой.
учитель: Мы просим от каждой команды выйти по 2 человека и принять участие в конкурсе «Химиков – аналитиков».
Задание для группы химиков – аналитиков:
В четырех пронумерованных пробирках находятся растворы гидроксида натрия, хлорида натрия, соляной кислоты и фенолфталеина.
Как, не используя дополнительных реактивов, распознать эти вещества?
учитель: А в это время оставшимся участникам также будет предложено задание для «Химиков – технологов».
Задание для группы химиков – технологов:
Расставить коэффициенты в уравнении реакции:
2KMnO4 ---- K2 MnO4 + MnO2 + O2
2Al + Fe2 O3 ----- Al2 O3 + 2 Fe
2Fe + 3H2 O ------- Fe2 O3 + 3H2
2NaHCO3 + H2 SO4 -------- Na2 SO4 + 2CO2 + 2H2 O
Итоги конкурса.
учитель: Итак, вы снова вместе собрались. Вас ждет еще одно испытание. «Ребус» – так называется следующий конкурс. (Приложение)
Ответы команд.
Итоги конкурса.
1 ученик:
Взор химика пытлив, ему порядок мил,
Среди своих реторт, мензурок и приборов,
Таких загадочных для любопытных взоров,
Стремится он постичь капризы тайных сил.
учитель:
Ваше следующее испытание называется «Угадай-ка». Чем меньше вы используете подсказок, тем больший балл вы получите.
«Угадайка»
1. Русский учёный.
2.Академик Петербургской АН ( с 1745 г.)
3. Основал первую химическую лабораторию.
4. Автор атомно– корпускулярного учения.
5. Разработал технологию и рецептуру цветных стекол.
6. Именем его назван Московский университет.
( Михаил Васильевич Ломоносов)
1. Галоген.
2. В свободном расстоянии встречается только в вулканических газах.
3. При н.у. – это газ.
4. Газ желто – зеленого цвета.
5. Очень ядовит.
6. В соединениях проявляет степень окисления от – 1 до + 7.
(хлор)
1.Итальянский физик и химик.
2. Создал метод определения молекулярной массы.
3. Вычислил атомную массу кислорода, водорода.
4. Открыл закон, относящийся к объемам газов.
5. Его именем названа универсальная постоянная – число молекул в 1 моль идеального газа.
6. Установил точный количественный атомный состав молекул многих веществ ( воды, водорода, азота)
( Амедео Авогадро)
1. Сложное вещество.
2. Соль.
3. Кислая соль.
4. Используется в медицине.
5. Сода питьевая.
6. Бикарбонат натрия.
(Гидрокарбонат натрия)
1. Газ.
2. Имеет удушливый запах.
3. Газ бурого цвета.
4. Получается при термическом разложении нитратов тяжелых металлов.
5. Промежуточный продукт при производстве азотной кислоты.
6. Оксид элемента со степенью окисления +4.
(Оксид азота IV)
Ответы команд.
Итоги конкурса
1 ученик:
Коль хотите домой воротиться,
То придется еще потрудиться.
Если сделана будет работа,
Мы откроем из царства ворота!
2 ученик:
Не робейте, не вешайте носа.
И отвечайте сейчас на вопросы!
Не ленитесь, не зевайте –
На вопросы отвечайте!
учитель: Наступает время самого сложного конкурса: «Самое сильное звено». Вы получаете лист бумаги с вопросами, необходимо возле вопроса написать свой ответ. За каждый вопрос, по 1 баллу.
Самое сильное звено
1. Метод определения состава вещества путем его разложения. ( Анализ)
2. Вещества, ускоряющие химические реакции. (Катализаторы)
3. Самый распространенный по массе элемент в природе. (Кислород)
4. Химическая реакция, при которой выделение тепловой и световой энергии (Горение)
5. Ученый, экспериментально доказавший состав воздуха. (А. Лавуазье)
6. Реакции, протекающие с выделением теплоты. (Экзотермический)
7. Ученый, который впервые получил водород в чистом виде. (Г. Кавендиш)
8. Сложные вещества, образованные атомами металлов и кислотных остатков. ( Соли)
9. Назовите вещество, формула которого Ca(NO3)2 (Нитрат калия)
10. Однородные системы, состоящие из молекул растворителя и растворенного вещества. (Растворы)
11. Реакция между кислотой и основанием. (Реакция нейтрализации)
12. Оксиды, которым соответствуют кислоты. (Кислотные)
13. Растворимые в воде основания. (Щелочи)
14. Соляная кислота. (HCl)
15. Оксид реагирующий с кислотами и щелочами. (Амфотерные)
16. Автор периодического закона. (Д. И. Менделеев)
17. С чем совпадает порядковый номер элемента? ( С зарядом ядра)
18. Разновидности атомов одного и того же химического элемента. (Изотопы)
19. Свойства элемента оттягивать на себя электроны других элементов. (Электроотрицательность)
20. Связь, образовавшаяся общими парами электронов. (Ковалентная)
21. Зараженные частицы, в которые превращаются атомы при отдаче электронов. (Ионы) 22. Химическая связь, возникшая между ионами. (Ионная)
23. Частицы, находящиеся в узлах атомных кристаллических решеток. (Атомы)
24. Формула фосфорной кислоты. (H3PO4)
25.Назовите вещество, формула которого Ba(OH)2. (Гидроксид бария)
26. Самый электроотрицательный элемент. (Фтор)
27. Процесс отдачи электронов. (Окисление)
28.Величина, показывающая, во сколько раз масса атома больше 1/12 массы атома углерода. (Относительная атомная масса)
29. Число атомов в молекуле обозначают с помощью… (Индекса)
30. Назовите вещество, формула которого Na2 S . (Сульфид натрия)
31. Число Авогадро. (6,03*1023)
32. Молярный объем газов. (22,4 л/моль)
33. Автор цитаты: «Широко распростирает химия руки свои в дела человеческие» (М. В. Ломоносов)
34.Автор теории электролитической диссоциации. (Сванте Аррениус)
35. Вещества, изменяющие свою окраску в зависимости от реакции среды. (Индикаторы)
36. Общее название элементов 8 группы главной подгруппы периодической системы Д. И. Менделеева. ( Инертные элементы, благородные газы)
37. Общее название солей азотной кислоты. (Нитраты)
38. Положительно заряженный ион. (Катион)
39. Вещества, замедляющие химическую реакцию. (Ингибиторы)
40. Уравнения, в которых указан тепловой эффект. (Термохимические)
41. Формула поваренной соли. (NaCl)
42. Нитрат аммония по-другому называется… (Аммиачная селитра)
43. Как называется реакция взаимодействия соли с водой? (Гидролиз)
44. Окраска лакмуса в нейтральной среде (Фиолетовый)
1 ученик:
Перемена, перемена!
Заливается звонок!
Наконец-то он закончен,
Надоедливый урок!
2 ученик:
Дернув серу за косичку,
Мимо магний пробежал.
Йод из класса испарился,
Будто вовсе не бывал.
1 ученик:
Фтор поджег случайно воду,
Хлор чужую книжку съел,
Углерод вдруг с водородом
Невидимкой стать успел.
2 ученик:
Калий, бром в углу дерутся:
Не поделят электрон,
Кислород – шалун на боре
Мимо проскакал верхом.
Учитель: А пока жури подводит итоги, проведем «Конкурс со зрителями».
Не все то аурум, что блестит.
(Не все то золото, что блестит).
Белый, как карбонат кальция.
(Белый как мел).
Куй феррум, пока горячо.
(Куй железо, пока горячо).
Слово - аргентум, а молчание - аурум.
(Слово - серебро, а молчание - золото).
Купрумного гроша не стоит.
(Медного гроша не стоит).
Стойкий станумный солдатик.
(Стойкий оловянный солдатик).
С тех пор много Н2О утекло.
(С тех пор много воды утекло).
Тяжелые плюмбумные тучи.
(Тяжелые свинцовые тучи).
Учитель: Вот и подошло к концу наше путешествие по “химическим дорожкам”. И пора подвести итоги. Слово жюри. Награждение победителей
Задание для группы химиков – технологов:
Расставить коэффициенты в уравнении реакции:
KMnO4 ---- K2 MnO4 + MnO2 + O2
Al + Fe2 O3 ----- Al2 O3 + Fe
Fe + H2 O ------- Fe2 O3 + H2
NaHCO3 + H2 SO4 -------- Na2 SO4 + CO2 + H2 O
Итоги конкурса._____________________
Задание для группы химиков – технологов:
Расставить коэффициенты в уравнении реакции:
KMnO4 ---- K2 MnO4 + MnO2 + O2
Al + Fe2 O3 ----- Al2 O3 + Fe
Fe + H2 O ------- Fe2 O3 + H2
NaHCO3 + H2 SO4 -------- Na2 SO4 + CO2 + H2 O
Итоги конкурса.________________________
Задание для группы химиков – технологов:
Расставить коэффициенты в уравнении реакции:
2KMnO4 ---- K2 MnO4 + MnO2 + O2
2Al + Fe2 O3 ----- Al2 O3 + 2 Fe
2Fe + 3H2 O ------- Fe2 O3 + 3H2
2NaHCO3 + H2 SO4 -------- Na2 SO4 + 2CO2 + 2H2 O
Самое сильное звено
1. Метод определения состава вещества путем его разложения. ( Анализ)
2. Вещества, ускоряющие химические реакции. (Катализаторы)
3. Самый распространенный по массе элемент в природе. (Кислород)
4. Химическая реакция, при которой выделение тепловой и световой энергии (Горение)
5. Ученый, экспериментально доказавший состав воздуха. (А. Лавуазье)
6. Реакции, протекающие с выделением теплоты. (Экзотермический)
7. Ученый, который впервые получил водород в чистом виде. (Г. Кавендиш)
8. Сложные вещества, образованные атомами металлов и кислотных остатков. ( Соли)
9. Назовите вещество, формула которого Ca(NO3)2 (Нитрат калия)
10. Однородные системы, состоящие из молекул растворителя и растворенного вещества. (Растворы)
11. Реакция между кислотой и основанием. (Реакция нейтрализации)
12. Оксиды, которым соответствуют кислоты. (Кислотные)
13. Растворимые в воде основания. (Щелочи)
14. Соляная кислота. (HCl)
15. Оксид реагирующий с кислотами и щелочами. (Амфотерные)
16. Автор периодического закона. (Д. И. Менделеев)
17. С чем совпадает порядковый номер элемента? ( С зарядом ядра)
18. Разновидности атомов одного и того же химического элемента. (Изотопы)
19. Свойства элемента оттягивать на себя электроны других элементов. (Электроотрицательность)
20. Связь, образовавшаяся общими парами электронов. (Ковалентная)
21. Зараженные частицы, в которые превращаются атомы при отдаче электронов. (Ионы) 22. Химическая связь, возникшая между ионами. (Ионная)
23. Частицы, находящиеся в узлах атомных кристаллических решеток. (Атомы)
24. Формула фосфорной кислоты. (H3PO4)
25.Назовите вещество, формула которого Ba(OH)2. (Гидроксид бария)
26. Самый электроотрицательный элемент. (Фтор)
27. Процесс отдачи электронов. (Окисление)
28.Величина, показывающая, во сколько раз масса атома больше 1/12 массы атома углерода. (Относительная атомная масса)
29. Число атомов в молекуле обозначают с помощью… (Индекса)
30. Назовите вещество, формула которого Na2 S . (Сульфид натрия)
31. Число Авогадро. (6,03*1023)
32. Молярный объем газов. (22,4 л/моль)
33. Автор цитаты: «Широко распростирает химия руки свои в дела человеческие» (М. В. Ломоносов)
34.Автор теории электролитической диссоциации. (Сванте Аррениус)
35. Вещества, изменяющие свою окраску в зависимости от реакции среды. (Индикаторы)
36. Общее название элементов 8 группы главной подгруппы периодической системы Д. И. Менделеева. ( Инертные элементы, благородные газы)
37. Общее название солей азотной кислоты. (Нитраты)
38. Положительно заряженный ион. (Катион)
39. Вещества, замедляющие химическую реакцию. (Ингибиторы)
40. Уравнения, в которых указан тепловой эффект. (Термохимические)
41. Формула поваренной соли. (NaCl)
42. Нитрат аммония по-другому называется… (Аммиачная селитра)
43. Как называется реакция взаимодействия соли с водой? (Гидролиз)
44. Окраска лакмуса в нейтральной среде (Фиолетовый)
Самое сильное звено
1. Метод определения состава вещества путем его разложения. ( )
2. Вещества, ускоряющие химические реакции. ( )
3. Самый распространенный по массе элемент в природе. ( )
4. Химическая реакция, при которой выделение тепловой и световой энергии ( )
5. Ученый, экспериментально доказавший состав воздуха. ( )
6. Реакции, протекающие с выделением теплоты. ( )
7. Ученый, который впервые получил водород в чистом виде. ( )
8. Сложные вещества, образованные атомами металлов и кислотных остатков. ( )
9. Назовите вещество, формула которого Ca(NO3)2 ( )
10. Однородные системы, состоящие из молекул растворителя и растворенного вещества. ( )
11. Реакция между кислотой и основанием. ( )
12. Оксиды, которым соответствуют кислоты. ( )
13. Растворимые в воде основания. ( )
14. Соляная кислота. ( )
15. Оксид реагирующий с кислотами и щелочами. ( )
16. Автор периодического закона. ( )
17. С чем совпадает порядковый номер элемента? ( )
18. Разновидности атомов одного и того же химического элемента. ( )
19. Свойства элемента оттягивать на себя электроны других элементов. ( )
20. Связь, образовавшаяся общими парами электронов. ( )
21. Зараженные частицы, в которые превращаются атомы при отдаче электронов. ( ) 22. Химическая связь, возникшая между ионами. ( )
23. Частицы, находящиеся в узлах атомных кристаллических решеток. ( )
24. Формула фосфорной кислоты. ( )
25.Назовите вещество, формула которого Ba(OH)2. ( )
26. Самый электроотрицательный элемент. ( )
27. Процесс отдачи электронов. ( )
28.Величина, показывающая, во сколько раз масса атома больше 1/12 массы атома углерода. ( )
29. Число атомов в молекуле обозначают с помощью… ( )
30. Назовите вещество, формула которого Na2 S . ( )
31. Число Авогадро. ( )
32. Молярный объем газов. ( )
33. Автор цитаты: «Широко распростирает химия руки свои в дела человеческие» ( )
34.Автор теории электролитической диссоциации. ( )
35. Вещества, изменяющие свою окраску в зависимости от реакции среды. ( )
36. Общее название элементов 8 группы главной подгруппы периодической системы Д. И. Менделеева. ( )
37. Общее название солей азотной кислоты. ( )
38. Положительно заряженный ион. ( )
39. Вещества, замедляющие химическую реакцию. ( )
40. Уравнения, в которых указан тепловой эффект. ( )
41. Формула поваренной соли. ( )
42. Нитрат аммония по-другому называется… ( )
43. Как называется реакция взаимодействия соли с водой? ( )
44. Окраска лакмуса в нейтральной среде ( )