СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока

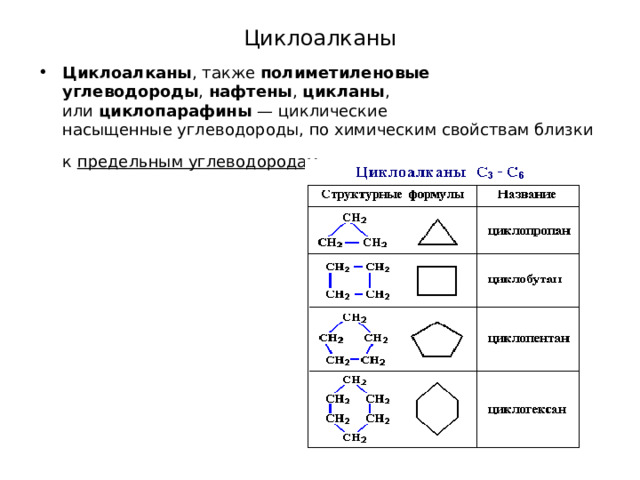
Химия. Строение органических веществ, классификация.Теория Бутлерова
Категория:
Химия
16.03.2024 11:43





![Термин «химическое строение» впервые ввёл А. М. Бутлеров 19 сентября в докладе «О 1861 года химическом строении веществ» на химической секции Съезда немецких естествоиспытателей и врачей в Шпейере (опубликованном в том же году на немецком и в следующем — на русском языках]). В том же докладе он заложил основы классической теории химического строения.](https://fsd.multiurok.ru/html/2024/03/16/s_65f55b85d0333/img1.jpg)


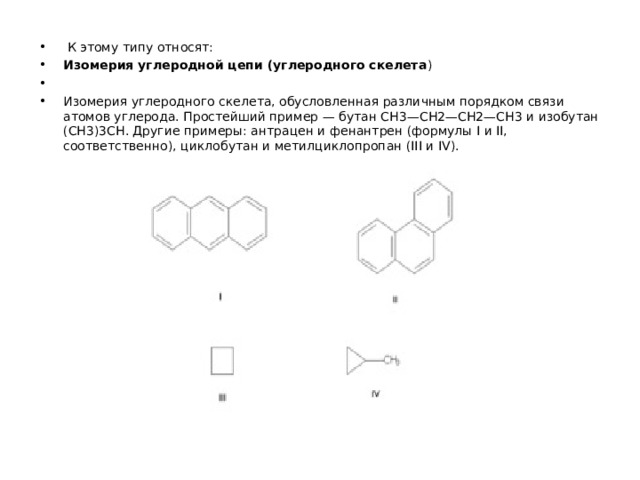
![Валентная изомерия. Валентная — особый вид структурной изомерии, при которой изомеры можно перевести друг в друга лишь за счёт перераспределения связей. Например, валентными изомерами бензола (V) являются бицикло [2.2.0]гекса-2,5-диен (VI, «бензол Дьюара»), призман (VII, «бензол Ладенбурга»), бензвален (VIII).](https://fsd.multiurok.ru/html/2024/03/16/s_65f55b85d0333/img5.jpg)