

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока


Химия в косметике
В данной работе собраны химические инградиенты, содержащиеся в косметических средствах. Особая роль отводится мыловарению.
Просмотр содержимого документа
«Химия в косметике»
Химия в косметике
ВСТУПЛЕНИЕ
ХИМИЯ (возможно, от греч. Chemia — Хемия, одно из древнейших названий Египта), наука, изучающая превращения веществ, сопровождающиеся изменением их состава и (или) строения. Химические процессы (получение металлов из руд, крашение тканей, выделка кожи и др.) использовались человечеством уже на заре его культурной жизни. В 3-4 вв. зародилась алхимия, задачей которой было превращение неблагородных металлов в благородные. С эпохи Возрождения химические исследования все в большей степени стали использовать для практических целей (металлургия, стеклоделие, производство керамики, красок); возникло также особое медицинское направление алхимии — ятрохимия. Во 2-й пол. 17 в. Р. Бойль дал первое научное определение понятия «химический элемент». Период превращения химии в подлинную науку завершился во 2-й пол. 18 в., когда был сформулирован сохранения массы закон при химических реакциях (см. также М. В. Ломоносов, А. Лавуазье) . В нач. 19 в. Дж. Дальтон заложил основы химической атомистики, А. Авогардо ввел понятие «молекула» . Эти атомно-молекулярные представления утвердились лишь в 60-х гг. 19 в. Тогда же А. М. Бутлеров создал теорию строения химических соединений, а Д. И. Менделеев открыл периодический закон . С кон. 19 — нач. 20 вв. важнейшим направлением химии стало изучение закономерностей химических процессов.
В современной химии отдельные ее области — неорганическая химия, органическая химия, физическая химия, аналитическая химия, химия полимеров стали в значительной степени самостоятельными науками. На стыке химии и других областей знания возникли, напр. биохимия, агрохимия, геохимия.
Косметическая химия — молодая наука, хотя многие её приёмы (приготовление косметических средств) вошли в практику еще в глубокой древности и описаны еще в IХ веке. до н. э.. Первые известные нам свидетельства настоящего расцвета косметики совпадают во времени с расцветом культуры Древнего Востока. В это время косметика развивается у египтян, персов, вавилонян, иудеев, ассирийцев, китайцев и индийцев. Как наука косметическая химия начала формироваться лишь в XIX веке.
Космети́ческая химия (от греч. κοσμητική – искусство украшать) - это наука о строении и свойствах веществ, используемых в косметических целях, о способах получения косметических средств и о влиянии этих средств на кожу, волосы, ногти человека. Современная косметическая химия применяет знания физики, химии природных и синтетических соединений, биохимии, медицины и других смежных наук. Она развивалась вместе с накоплением сведений о лекарствах и лекарственных растениях, вместе с развитием медицины, химии и физики.
КОСМЕТИКА (от греч. kosmetike — искусство украшать) ,
1) учение о средствах и методах улучшения внешности человека. Различают врачебную и декоративную косметику. Врачебная косметика использует для устранения внешних дефектов не только косметические средства, но и физиотерапевтические, хирургические и другие методы. С помощью декоративной косметики маскируются недостатки или подчеркиваются отдельные черты лица.
2) Средства для ухода за кожей, волосами, зубами и ногтями (крем, лосьон, пудра, помада и т. п.) .
ОСНОВНАЯ ЧАСТЬ
Искусство косметики
Наблюдения показывают, что если нужно, то женщины могут отказать себе во многом, только не в том, что сделает их хотя бы чуточку красивее. Искусство косметики уходит в далекое прошлое. Так, при раскопках найдены египетские мумии, ногти которых раскрашены. В усыпальницах египетских пирамид обнаружены натуральные краски и косметические инструменты, различные плитки для приготовления смеси красок и румян, сосуды для хранения мазей и масел. Найден письменный документ - папирус Эберса, в котором изложены косметические правила и рецепты. Его написание относят к пятому тысячелетию до новой эры. Древние рукописи свидетельствуют, что уже тысячи лет назад женщины Востока подкрашивали веки в голубой цвет тончайшей пыльцой из толченой бирюзы. Бирюза -- это природный минерал, имеющий состав СuА16(РО4)4(ОН)8•4Н2О. С незапамятных времен для подкрашивания бровей использовался мягкий природный минерал - сурьмяный блеск Sb2S3. В русском языке было выражение «сурьмить брови». Сурьмяный блеск поставлялся в различные страны арабами, которые называли его стиби. От этого названия и пошло латинское стибиум, означавшее в древности не химический элемент, а его сульфид Sb2S3. Природный сурьмяный блеск имеет цвет от серого до черного с синей или радужной побежалостью.
Достоверно известно, что в России косметические краски применялись в конце XVI и особенно широко в XVII веке. Ассортимент средств декоративной косметики, вырабатываемых промышленностью, разнообразен и включает следующие виды изделий: губные помады и блеск для губ, тени для век, тушь для ресниц, лаки для ногтей, маскирующие карандаши, румяна, макияжи и др. Промышленность выпускает перламутровые губные помады и кремы, а также шампуни с перламутровыми блесками. Перламутровый эффект в косметических средствах создается солями висмутила ВiOСl и BiO(NO3) или титанированной слюдой -- перламутровым порошком, содержащим около 40 % ТiO2. Давно известны жемчужные или испанские белила. Их основным компонентом является BiO(NO3)2, образующийся при растворении нитрата висмута Bi(NO3)з в воде. В косметике эти белила используют для приготовления белого грима. Для создания специальных косметических средств (гримов) применяют оксид цинка ZnO, получаемый прокаливанием основного карбоната (ZnOH)2CO3. В медицине его используют в присыпках (в качестве вяжущего, подсушивающего, дезинфицирующего средства) и для изготовления мазей. Средства для окраски волос в быту в качестве дезинфицирующего и отбеливающего средства широко используют растворы (3, 6, 10 %-ные) пероксида водорода. Более концентрированный -- 30%-ный раствор пероксида водорода - называют пергидролем, перекись водорода - неустойчивое (особенно на свету) химическое соединение. Оно разлагается на воду и кислород:2Н2О2 = 2Н2О + О2В момент образования кислород находится в атомарном состоянии и лишь, затем переходит в молекулярный:2О = О2Атомарный кислород обладает особенно сильным окислительным свойством. Благодаря ему растворы пероксида водорода разрушают красящие вещества и отбеливают ткани из хлопчатобумажных и шерстяных тканей, шелк, перья, волосы. Способность пероксида водорода обесцвечивать волосы используют в косметике. Она основана на взаимодействии атомарного кислорода с красящим веществом волос меланином - смесью сложных органических веществ. При окислении меланин переходит в бесцветное соединение. Следует помнить, что пергидроль вызывает ожоги кожи и слизистых оболочек. В настоящее время для окраски волос имеется большой ассортимент различных органических красителей. Иногда же для этой цели применяют соли серебра, меди, никеля, кобальта, железа. В таком случае крашение волос осуществляют при помощи двух растворов. Один из них содержит соли данных металлов: нитраты, цитраты, сульфаты или хлориды, а второй - восстановители: пирогаллол, таннин и др. При смешении этих растворов ионы металлов восстанавливаются до атомов, которые и осаждаются на поверхности волос.
Классификация продуктов косметической химии
Индустрия моды, огромный потенциал парфюмерно-косметической промышленности и идеология современного общества, требующая от человека молодого и здорового внешнего вида, побуждают людей применять большое количество разнообразных косметических средств. Поэтому сегодня перечень косметической продукции весьма обширен.
На сегодняшний день основными продуктами косметической химии являются:
Кремы, эмульсии, лосьоны, гели и масла для кожи (рук, лица, ног, и т. д.)
Маски для лица и составы для пилингов
Основы для окрашивания кожи (жидкости, пасты, порошки)
Присыпки, гигиенические присыпки, присыпки после ванн
Туалетное мыло, ароматическое мыло и т. д.
Духи, туалетная вода и одеколон
Продукты для ванны и душа (соли, пена, масла, гели и т. д.)
Средства для удаления волос
Дезодоранты и средства от пота
Средства по уходу за волосами
Краска для волос, а также для обесцвечивания волос
Продукция для завивки, выпрямления и фиксации волос
Фиксаторы и стабилизаторы
Очищающие продукты (лосьоны, порошки, шампуни)
Кондиционеры (лосьоны, кремы, масла)
Продукция для укладки волос (лосьоны, лаки, бриллиантины)
Продукция для бритья (кремы, пена, лосьоны и т. д.)
Продукция для макияжа (пудра, тональный крем, тушь для ресниц, румяна) и удаления макияжа с лица и глаз
Губные помады и продукция по уходу за губами
Зубные пасты и продукция по уходу за зубами
Продукция для ухода за ногтями, лаки для ногтей
Продукция личной гигиены
Продукция для загара
Продукция для загара без солнца
Продукция, отбеливающая кожу
Продукция против морщин и т. д.
Основные вещества
Исходя из состава эпидермальных тканей можно утверждать, что в косметические средства должны входить те вещества, из которых эти ткани состоят. Поэтому косметические препараты по уходу за ногтями, кожей, волосами и т.д. содержат аминокислоты и пептиды, жиры и масла, углеводы и витамины. Именно эти необходимые для живых клеток вещества составляют основу косметических средств. Но кроме этих основных видов сырья в косметике используются биологически активные вещества иного происхождения и их комплексы, имеющие определенное функциональное назначение и оказывающие на кожу то или иное положительное влияние.
В производстве косметических средств широко используют природные и синтетические виды сырья. Природные виды сырья могут быть животного, растительного и минерального происхождения. В настоящее время в косметике используется примерно 20000 природных компонентов. Синтетическое сырье получают химическим путем. Оно отличается высокой степенью чистоты. Для синтетического сырья характерно постоянство физико-химических свойств и параметров. Этот факт важную роль при составлении многокомпонентных косметических рецептур.
Основные виды ингредиентов для производства косметических средств:
Жиры животные — наибольшее применение находят куриный, норковый, говяжий и свиной жир, ланолин, спермацет и яичное масло;
Жиры растительные (масла) — в косметике в основном применяют хлопковое, льняное, касторовое, пальмовое, персиковое, соевое, абрикосовое, подсолнечное, миндальное, оливковое, кокосовое и кукурузное масло, масло какао, авокадо, каритэ, жожоба, виноградной косточки, зародышей пшеницы и др.;
Воски
Заменители жиров и масел (синтетические жиры, масла, воски)
Углеводороды
Высшие карбоновые кислоты
Эфирные масла
Поверхностно-активные вещества
Солюбилизаторы
Витамины
Парфюмерные композиции
Качество сырья имеет огромное значение для производства косметических препаратов. При оценке качества сырья пользуются органолептическими (определяю цвет, запах, вкус, прозрачность, внешний вид) и физико-химическими методами. Для характеристики косметических ингредиентов определяют относительную плотность; температуры плавления, кипения и помутнения; вязкость; показатель преломления; кислотное число; эфирное число; число омыления, йодное число и др.[1]
- Химические средства гигиены и косметики
Слово гигиена происходит от греч. гигиенос, что означает целебный, приносящий здоровье, а косметика – от греч., означающее искусство украшать. В настоящее время термин «косметика» употребляют прежде всего в связи с уходом за кожей лица и тела. Гигиена – это раздел профилактической медицины, изучающей влияние внешней среды на здоровье человека.
К важнейшим гигиеническим средствам следует прежде всего отнести мыла и моющие средства. О них была речь ранее. Конечно, охватить все химические средства гигиены и косметики невозможно в небольшой книжке. Поэтому здесь внимание читателей будет обращено лишь на некоторые.
А.Средства ухода за зубамиЗуб состоит из трех частей: коронки (часть, выступающая над десной), корня (часть, погруженная в альвеолу челюсти) и шейки – место перехода коронки в корень. Коронка покрыта эмалью, а под ней находится дентин. Корень покрыт слоем ткани, называемой цементом. Эмаль, дентин и цемент – это твердые ткани. Внутри зуба имеется полость, которая содержит пульпу, состоящую из рыхлой соединительной ткани, в которой проходят нервы и сосуды, питающие ткани зуба.
Зубы подвержены ряду заболеваний и одним из наиболее распространенных является кариес. К сожалению, никому не удается избежать этого заболевания, но ограничить его распространение на многие зубы можно, принимая профилактические меры. Сущность кариеса состоит в том, что под влиянием микроорганизмов и вырабатываемых ими кислот происходит разрушение тканей зуба. Самой прочной тканью является эмаль. Ее состав близок к минералу гидроксидапатиту Ca5OH(PO4)3. При разрушении эмали микроорганизмы попадают в дентин, а затем в пульпу и вызывают ее воспаление (пульпит).
Закреплению микроорганизмов на эмали способствует зубной камень – твердые пористые отложения на зубах. Микроорганизмы поселяются в порах этого камня. Первая стадия образования зубного камня связана с отложением на зубах мягкого налета из остатков пищи, отживших клеток, слизи. На второй стадии происходит минерализация мягкого налета, т.е. его пропитывание минеральными компонентами слюны. Слюна содержит ионы Ca2+ и HPO24–. Они препятствуют растворению эмали зуба, но, откладываясь в мягком налете в виде малорастворимой соли, приводят к его минерализации.
Слюна здорового человека имеет нейтральную реакцию (рН 7,0...7,5). В результате расщепления бактериями (Стрептококкус мутанис) остатков пищи, содержащей углеводы (в частности, сахар), образуются органические кислоты – в основном молочная. Эти кислоты снижают рН до 4,5...5,0. В данных условиях разрушение эмали ускоряется, что и приводит к весьма неприятным результатам. Давно замечено, что любители сладкого часто не могут похвастаться хорошим состоянием зубов.
Таким образом, одним из путей профилактики кариеса является очистка зубов и полоскание ротовой полости после приема пищи. Это приводит к предотвращению образования мягкого налета и зубного камня.
Трудно сказать, когда люди начали чистить зубы, но имеются сведения, что одним из древнейших препаратов для чистки зубов была табачная зола. Еще сравнительно недавно для чистки зубов широко применяли зубные порошки. Они состоят из абразивного материала: чаще всего это мел CaCO3, реже CaHPO4, а иногда их смеси Эти абразивы получают химическим осаждением, например, в соответствии с уравнением
Ca(NO3)2 + Na2CO3 = CaCO3↓ + 2NaNO3
Природный мел использовать нельзя, так как в нем содержатся твердые частицы от панцирей морских организмов, которые обладают высокой прочностью и могут привести к сильному истиранию и повреждению эмали зуба. К абразивным материалам добавляют MgO, полученный прокаливанием MgCO3. Оксид магния придает порошкам легкость и рыхлость. В некоторые сорта порошков вводят пероксид магния MgO2, который обладает отбеливающими свойствами. В небольших количествах в порошки включают поверхностно-активные вещества, например лаурилсульфат натрия C12H25OSO3Na, а также отдушки – чаще всего ментол или экстракт мяты. В настоящее время существенно сокращено производство зубных порошков, поскольку они стали менее популярными, чем пасты.
Важнейшим средством ухода за зубами являются зубные пасты. Они имеют меньшую истирающую способность по сравнению с порошками, более удобны в применении и характеризуются более высокой эффективностью. Зубные пасты – это многокомпонентные составы. Они подразделяются на гигиенические и лечебно-профилактические. Первые оказывают только очищающее и освежающее действие, а вторые, кроме того, служат для профилактики заболеваний и способствуют лечению зубов и полости рта.
Основные компоненты зубной пасты следующие: абразивные, связующие, загустители, пенообразующие. Абразивные вещества обеспечивают механическую очистку зуба от налетов и его полировку. В качестве абразивов чаще всего применяют химически осажденный мел CaCO3. Установлено, что компоненты зубной пасты способны влиять на минеральную составляющую зуба и, в частности, на эмаль. Поэтому в качестве абразивов стали применять фосфаты кальция: CaHPO4, Ca3(PO4)2, Ca2P2O7, а также малорастворимый полимерный мета-фосфат натрия (NaPO3)x. Кроме того, в качестве абразивов в различных сортах паст применяют оксид и гидроксид алюминия, диоксид кремния, силикат циркония, а также некоторые органические полимерные вещества, например метилметакрилат натрия. На практике часто используют не одно абразивное вещество, а их смесь. Для превращения смеси абразивных порошков в стойкую пасту применяют желатинирующие компоненты. Их часто получают в промышленном масштабе из растений; например, из морских водорослей извлекают природные полисахариды: натриевые соли альгиновых кислот и каррагинаты. Для этой цели реже применяют растительные камеди – трагакант и пектины. Из синтетических веществ широкое применение нашли производные клетчатки (хлопковой и древесной) – натрийкарбоксиметилцеллюлоза, оксиэтилированные этиловый и метиловый эфиры целлюлозы или просто этиловый и метиловый эфиры целлюлозы. Для получения пластичной, тиксотропной массы, легко выдавливающейся из тюбика, применяют полиатомные спирты: глицерин, сорбит, полиэтиленгликоль. Они способствуют сохранению в пасте влаги при хранении, повышают температуру замерзания и улучшают вкусовые свойства пасты. Растительные экстракты и камеди чувствительны к действию микробов. Поэтому для устранения их разрушительного действия в состав паст вводят антисептические вещества: формальдегид, хлорированные фенолы и алкильные эфиры оксибензойных кислот.
В качестве пенообразующих веществ в зубных пастах в прошлом использовали мыла. Однако их низкая пенообразующая способность в жесткой воде и неприятный мыльный привкус снижали качество паст. Вместо мыла стали использовать ализариновое масло (сульфированное касторовое масло)
Оно не связывается в малорастворимое вещество ионами кальция и магния и обладает смачивающими и бактерицидными свойствами. Кроме него в качестве пенообразователей используют натрийлаурилсульфат C12H25OSO3Na и натрийлаурилсаркозинат
Считают, что последний обладает антикариесным действием. Уже в концентрации 0,3% он подавляет действие бактерий, образующих в полости рта молочную кислоту, которая разрушает эмаль зуба. Действие лаурилсаркозината сохраняется в полости рта после чистки зубов в течение примерно 12 ч. Хорошими пенообразующими, очищающими и смачивающими свойствами обладает натриевая соль таурида жирной кислоты RCONHCH2SO3Na.
Борьбу с кариесом при помощи лечебно-профилактических зубных паст ведут по двум направлениям: 1) укрепление минеральной ткани зуба; 2) предупреждение образования зубного налета. Первое достигается введением в пасты соединений фтора: монофторфосфата натрия, формулу которого условно можно записать в виде двойной соли NaF·NaPO3, а также фторида натрия NaF и фторида олова (II) SnF2. Существуют две точки зрения на влияние фторидных ионов на укрепление эмали зуба. 1. Ионы F– переводят гидроксидапатит эмали CaOH(PO4)3 в менее растворимый в кислотах фторапатит Ca5F(PO4)3. 2. В результате обменной реакции в пасте образуется CaF2, который адсорбируется на гидроксидапатите и предохраняет его от воздействия кислот. Известно также, что фторидные соединения способствуют подавлению жизнедеятельности бактерий, вызывающих образование в полости рта органических кислот. В настоящее время в антикариесных пастах стали широко использовать ферменты, а иногда в них вводят антибиотики.
В зубные пасты обязательно вводят отдушки и вкусовые компоненты. Наиболее распространены отдушки мятного и коричного характера. Мятная отдушка обеспечивается применением ментола, мятных масел – перечной или кудрявой мяты, а также различных модификаторов. В отдушках применяют метилсалицилат, гвоздичное масло, эвкалиптол, коричный альдегид. В качестве подслащивающего компонента чаще всего используют сахарин и некоторые его производные. За рубежом для этой цели рекомендуют сахарат натрия и дульцин вместе с небольшим количеством хлорида натрия или лимонной кислоты. Недавно стали применять натриевую соль цикламеновой кислоты, которая по вкусу напоминает сахар.
Некоторые зарубежные фирмы приступили к производству безабразивных гелеобразных прозрачных зубных паст. В них используют гели SiO2, а также сополимеры акриловой кислоты и аллилового спирта. Эти пасты обладают высокой пенообразующей способностью, имеют приятный вкус и красивый внешний вид. Они легко окрашиваются в различные яркие цвета – красный, синий, зеленый, желтый. Однако их очищающая способность намного ниже, чем паст с использованием абразивов.
Хотя зубные протезы, естественно, не подвергаются кариесу и другим заболеваниям, но от них может зависеть состояние микрофлоры полости рта. Имеет существенное значение и их внешний вид. Поэтому зубные протезы требуют периодической чистки от остатков пищи, пятен и образующегося зубного камня. Для этой цели протезы погружают на ночь или на более короткий срок в растворы кислот: соляной, сульфаминовой или лимонной, а также в растворы, содержащие активный хлор, – гипохлориты или активный кислород – перборат натрия.
Б.Дезодоранты и озоновый «щит» планетыКаждый знает, что дезодоранты – это средства, устраняющие неприятный запах пота. На чем основано их действие? Пот выделяется особыми железами, расположенными в коже на глубине 1...3 мм. У здоровых людей на 98...99% он состоит из воды. С потом из организма выводятся продукты метаболизма: мочевина, мочевая кислота, аммиак, некоторые аминокислоты, жирные кислоты, холестерин, в следовых количествах белки, стероидные гормоны и др. Из минеральных компонентов в состав пота входят ионы натрия, кальция, магния, меди, марганца, железа, а также хлоридные и иодидные анионы. Неприятный запах пота связан с бактериальным расщеплением его составляющих или с окислением их кислородом воздуха. Дезодоранты (косметические средства от пота) бывают двух типов. Одни тормозят разложение выводимых с потом продуктов метаболизма путем инактивации микроорганизмов или предотвращением окисления продуктов потовыделения. Действие второй группы дезодорантов основано на частичном подавлении процессов потовыделения. Такие средства называют антиперспиранами. Этими свойствами обладают соли алюминия, цинка, циркония, свинца, хрома, железа, висмута, а также формальдегид, таннины, этиловый спирт. На практике из солей в качестве антиперспиранов чаще всего используют соединения алюминия. Перечисленные вещества взаимодействуют с компонентами пота, образуя нерастворимые соединения, которые закрывают каналы потовых желез и тем самым уменьшают потовыделение. В оба типа дезодорантов вводят отдушки.
Чем же создается давление в аэрозольных баллонах? Это не праздный вопрос, так как с ним, можно сказать, связана судьба человечества. Рабочее давление в баллонах создается парами сжиженного газа, либо за счет сжатого газа, например, N2, CO2 или N2O. До сих пор баллоны со сжатыми газами применялись редко, поскольку их рабочее давление падает по мере расходования содержимого баллона, т.е. по мере увеличения объема парового пространства. Давление над сжиженным газом постоянно, так как оно поддерживается испарением жидкости и заполнением увеличивающегося пространства. В качестве веществ, создающих давление в аэрозольных баллонах, оказались удобными фторхлоруглероды.
Так, при 21°C давление паров над жидким CF2Cl2 составляет 5 атм, а над смесью (50%:50%) CF2Cl2 и CF2Cl2 2,5 атм. Эти вещества, кроме того, обладают важным свойством – малой химической активностью по отношению ко многим веществам. Легкокипящие и химически инертные вещества, используемые для создания повышенного давления в аэрозольных баллонах, называют пропеллентами. Таким образом, в аэрозольных баллонах в жидком веществе (основе), ради которого и создается устройство, содержится жидкий пропеллент. Довольно часто растворы аэрозольного баллона (одеколоны, кремы для бритья и др.) содержат воду. Пропелленты CF2Cl2 и CFCl3 со временем частично гидролизуются (взаимодействуют с водой) и поэтому нежелательны. В таких случаях в качестве пропеллента используют CF2Cl – CF2Cl (1,2-дихлортетрафторэтан). В настоящее время принято международное соглашение по сокращению производства аэрозольных баллонов, содержащих в качестве пропеллентов фторхлоруглероды, поскольку установлено, что они плохо влияют на озоновый слой Земли.
В атмосфере на определенной высоте от Земли имеется повышенная концентрация озона. Он получается в результате фотодиссоциации молекулярного кислорода и взаимодействия атомарного кислорода
O2 ← [hν (свет)] → 2O
с молекулярным в соответствии с уравнением
O + O2 ↔ O3*
Образующиеся молекулы озона содержат избыточную энергию, т.е. они возбуждены. Если не отвести от молекулы озона эту избыточную энергию, то она долго не просуществует, а распадется на исходные атомарный и молекулярный кислород. Чтобы молекула озона стала стабильной, она должна отдать избыток энергии какой-то другой молекуле, например молекуле азота:
O3* + N2 → O3 + N2*
Концентрация озона в атмосфере зависит от двух причин. 1. Для диссоциации молекул O2 на атомы нужно интенсивное коротковолновое солнечное излучение, которое поглощается по мере приближения к Земле. Следовательно, диссоциация O2 на атомы преимущественно протекает в верхних слоях. 2. Для стабилизации образующихся молекул озона необходимо столкновение с другими частицами, т.е. разрежение воздуха не должно быть слишком большим, а следовательно, высота должна быть также не очень большая. В результате этих двух факторов, действующих в противоположных направлениях, озон накапливается в определенных слоях атмосферы. Опыт показывает, что наибольшая его концентрация наблюдается на высоте около 50 км. Этот слой атмосферы и называют озоновым «щитом» планеты. Он играет чрезвычайно важную роль в сохранении жизни на Земле. Оказалось, что молекулы озона, как никакие другие, находящиеся в атмосфере, сильно поглощают фотоны с длиной волны от 200 до 310 нм, т.е. ультрафиолетовое излучение Солнца. Известно, что растения и животные гибнут при интенсивном облучении этим светом. Таким образом, можно сказать, что от концентрации озона зависит судьба нашей планеты.
Концентрация озона в атмосфере зависит от содержания оксидов азота и фторхлорметанов. Оксиды азота постоянно присутствуют в низких концентрациях в результате фотохимического взаимодействия азота и кислорода. Оксид азота (II) разрушает озон, а оксид азота (IV) связывает атомарный кислород.
Таким образом, оксиды азота играют роль катализаторов в разложении озона.
За 4,6 млрд лет существования нашей планеты установилось равновесие, и жизнь на Земле возникла и развилась при определенном равновесном составе атмосферы. Однако интенсивное развитие сверхзвуковой авиации начинает оказывать влияние на создавшееся в атмосфере равновесие. Поскольку сверхзвуковые самолеты предназначены для полетов в стратосфере, верхний предел которой подходит к «озоновому» слою, то появляется опасность влияния сверхзвуковой техники на этот слой. При сгорании топлива в двигателях самолетов в довольно больших количествах образуются оксиды азота.
Другим источником опасности озоновому слою являются фторхлорметаны (главным образом CF2Cl2 и CFCl3). Эти вещества широко используют в баллонах в аэрозольной упаковке, а также в качестве хладоагентов в промышленных и бытовых холодильниках. Фторхлорметаны – чрезвычайно инертные химические вещества. В атмосфере они разрушаются лишь в верхних слоях под действием ультрафиолетового излучения в диапазоне длин волн 190...225 нм. Одним из продуктов разложения фторхлорметанов является атомарный хлор:
CCl4–xFx – [hν (свет)] → CCl3–xFx + Cl
Скорость разрушения фторхлорметанов максимальна на высоте около 30 км, т.е. в слое, примыкающем к озоновому. Атомарный хлор так же, как и оксиды азота, способен катализировать разложение озона.
Научная общественность высказывает озабоченность разрушением озонового слоя Земли и требует сокращения использования фторхлорметанов в качестве распылителей аэрозолей.
Необходимо отметить еще раз, что ожоги солнечным светом вызываются ультрафиолетовыми лучами в области длин волн 280...315 нм (эритемная область). Ультрафиолетовые лучи с длинами волн 315...400 нм способствуют образованию на коже человека пигмента меланина, который служит защитой от эритермы (от ожога). В некоторых странах налажен выпуск фотозащитных кремов, которые поглощают или отражают солнечные лучи эритемной области, но пропускают лучи, стимулирующие появление на коже загара. В качестве примеров фотозащитных соединений можно указать на этиловый эфир циннамилиденуксусной кислоты (I) и 2-фенилбен-зоксазол
В.Косметические средстваВ мире считается, что среди наиболее прибыльных отраслей промышленности на одном из первых мест стоит косметическая. Наблюдения показывают, что если нужно, то женщины могут отказать себе во многом, только не в том, что сделает их хотя бы чуточку красивее.
Искусство косметики уходит в далекое прошлое. Так, при раскопках найдены египетские мумии, ногти которых раскрашены. В усыпальницах египетских пирамид обнаружены натуральные краски и косметические инструменты, различные плитки для приготовления смеси красок и румян, сосуды для хранения мазей и масел. Найден письменный документ – папирус Эберса, в котором изложены косметические правила и рецепты. Его написание относят к пятому тысячелетию до новой эры.
Письменные источники далекого прошлого и наблюдения современных путешественников свидетельствуют о том, что на ранней стадии развития к раскрашиванию тела красками были неравнодушны и мужчины. Как атавизм этого можно рассматривать склонность некоторых мужчин к накожной татуировке. По мере развития культуры мужчины теряют этот интерес. Стремление женщин к подкрашиванию кожи (особенно лица) наоборот усиливается. Судя по всему, для женщин нет простой связи между культурой и количеством используемой косметики. Связь скорее можно уловить между количеством косметики и прирожденным вкусом.
Древние рукописи свидетельствуют, что уже тысячи лет назад женщины Востока подкрашивали веки в голубой цвет тончайшей пыльцой из толченой бирюзы. Бирюза – это природный минерал, имеющий состав СuАl6(PO4)4(OH)8·4H2О.
С незапамятных времен для подкрашивания бровей использовался мягкий природный минерал – сурьмяный блеск Sb2S3. В русском языке было выражение «сурьмить брови». Сурьмяный блеск поставлялся в различные страны арабами, которые называли его стиби. От этого названия и пошло латинское стибиум, означавшее в древности не химический элемент, а его сульфид Sb2S3. Природный сурьмяный блеск имеет цвет от серого до черного с синей или радужной побежалостью.
Достоверно известно, что в России косметические краски применялись в конце XVI и особенно широко в XVII в. Историк П.М. Лукьянов в одной из своих книг цитирует саксонского путешественника Олеария, который посетил Россию в первой половине XVII в. и позднее описал свои впечатления: «Женщины в России среднего роста, вообще стройны, нежны лицом и сложением, но в городах все румянятся и так грубо и заметно, что глядя на них подумаешь, будто кто вымазал их рукою полною муки и потом кисточкой намазывал им на щеки красной краской. Брови и ресницы они также подкрашивали черной, а иногда и коричневой краской». Впечатления того же времени другого путешественника по России голландца Стрюйса на этот счет записаны следующими словами: «Хотя женщины обыкновенно белы, и кожа на лице их очень гладкая, все-таки они почти все румянятся или вернее натираются аляповато белилами и приглашают для этого белильшиц». Румянами в то время красили не только щеки, но и губы.
Естественно, что в далеком прошлом в качестве косметических препаратов использовались лишь природные минеральные и органические вещества. С развитием химии для этой цели все чаще стали применять синтетические продукты. Так, например, в качестве пигмента для губных помад применяют малиново-красный бисди-метилглиоксимат никеля. Органический реагент диметилглиоксим химики-аналитики используют для качественного обнаружения и количественного определения ионов никеля (II), а реакция образования этого соединения носит имя нашего соотечественника Л.А. Чугаева.
Промышленность выпускает перламутровые губные помады и кремы, а также шампуни с перламутровыми блесками. Перламутровый эффект в косметических средствах создается солями висмутила BiOCl и ВiO(NO3) или титанированной слюдой – перламутровым порошком, содержащим около 40% TiO2. Давно известны жемчужные или испанские белила. Их основным компонентом является ВiO(NO3)2, образующийся при растворении нитрата висмута Вi(NO3)3 в воде. В косметике эти белила используют для приготовления белого грима.
Для создания специальных косметических средств (гримов) применяют оксид цинка ZnO, получаемый прокаливанием основного карбоната (ZnOH)2CO3. В медицине его используют в присыпках (в качестве вяжущего, подсушивающего, дезинфицирующего средства) и для изготовления мазей.
Косметические декоративные пудры – многокомпонентные смеси. В них входят: тальк, каолин, ZnO, TiO2, MgCO3, крахмал, цинковые и магниевые соли стеариновой кислоты, а также органические и неорганические пигменты, в частности Fe2O3. Тальк придает пудре сыпучесть и скользящий эффект. Его недостатком является способность впитываться в кожу и придавать жирный блеск. Тем не менее в состав пудр он входит в количестве до 50...80%. Каолин обладает высокой укрывистостью и способностью впитывать избыток жировых выделений кожи. Его повышенная гигроскопичность способствует слеживаемости и неравномерному распределению пудры на коже, поэтому каолин вводят не более 25%. Оксиды цинка и титана обладают хорошей укрывистостью. Кроме того, оксид цинка обладает антисептическими свойствами и потому одновременно выполняет роль дезинфицирующей добавки. Эти оксиды вводят в пудры до 15%. В больших количествах они приводят к сухости кожи. Крахмал придает коже бархатистость, а благодаря стеаратам цинка и магния пудра хорошо удерживается на коже и делает ее гладкой.
Компактная пудра в отличие от рассыпной содержит связующие добавки: натрийкарбоксиметилцеллюлозу, высшие жирные кислоты, воски, многоатомные спирты и их эфиры, минеральные и растительные масла. Они позволяют получать при прессовании брикеты определенной формы, которые сохраняют прочность при длительном употреблении.
В быту в качестве дезинфицирующего и отбеливающего средства широко используют растворы (3, 6, 10%-ные) пероксида водорода. Более концентрированный – 30%-ный раствор пероксида водорода – называют пергидролем. Пероксид водорода – неустойчивое (особенно на свету) химическое соединение. Оно разлагается на воду и кислород:
2H2O2 = 2H2О + O2
В момент образования кислород находится в атомарном состоянии и лишь затем переходит в молекулярный:
2О = O2
Атомарный кислород обладает особенно сильным окислительным свойством. Благодаря ему растворы пероксида водорода разрушают красящие вещества и отбеливают ткани из хлопчатобумажных и шерстяных тканей, шелк, перья, волосы. Способность пероксида водорода обесцвечивать волосы используют в косметике. Она основана на взаимодействии атомарного кислорода с красящим веществом волос меланином – смесью сложных органических веществ. При окислении меланин переходит в бесцветное соединение. Следует помнить, что пергидроль вызывает ожоги кожи и слизистых оболочек.
В настоящее время для окраски волос имеется большой ассортимент различных органических красителей.
Иногда же для этой цели применяют соли серебра, меди, никеля, кобальта, железа. В таком случае крашение волос осуществляют при помощи двух растворов. Один из них содержит соли данных металлов: нитраты, цитраты, сульфаты или хлориды, а второй – восстановители: пирогаллол, таннин и др. При смешении этих растворов ионы металлов восстанавливаются до атомов, которые и осаждаются на поверхности волос.
Наиболее распространенный лак для ногтей представляет раствор нитроцеллюлозы в органических растворителях. Нитроцеллюлозу получают нитрованием целлюлозы (хлопковой или древесной) смесью азотной и серной кислот. Она является сложным эфиром азотной кислоты и характеризуется общей формулой [C6H7O2(OH)3–x(ONO2)x]n. В качестве растворителей используют амиловый эфир уксусной кислоты, ацетон, различные спирты, этиловый эфир, а также их смеси. В лак добавляют пластификаторы – касторовое масло или другие экстракты, которые препятствуют обезжириванию ногтей и предотвращают их ломкость.
Следует отметить, что косметика тесно соприкасается с гигиеной, так как имеется много косметических средств (лосьоны, кремы, шампуни и др.), которые выполняют и гигиеническую функцию.
Все хотят быть молодыми и красивыми. И для достижения этой цели в ход идут всевозможные косметические средства. Но использовать их нужно с очень большой осторожностью, т.к. при неправильном применении результат может быть прямо противоположным.
Ассоциация Американских Потребителей подсчитала, что ежедневно мы используем в среднем около 10 косметических средств, которые содержат более 100 химических компонентов. Сейчас все больше потребителей задается вопросами: какой процент химии находится в моей косметике и безопасна ли та или иная косметика для моего организма? Не наносит ли ее использование вред не только мне, а и окружающей среде?
Химия в косметике опасна для окружающей среды и здоровья человека
Исследования, проводимые в США и Канаде, выявили множество гормональных нарушений в организме человека в связи с общим загрязнением воды. Каково же было удивление санитарных врачей, когда выяснилось что причина заболеваний - смыв отходов косметических фабрик в реки и водоемы. Что касается собственного здоровья, то многие "эксперты" говорят, что химия, которая содержатся в косметике, не способна вызвать серьезные нарушения в организме после однократного применения. Исключение составляют только особо чувствительные люди. Именно этот аргумент ученых очень часто используется производителями косметики для оправдания наличия химии в их продукции. Но ведь мы используем данные косметические продукты не единожды, а ежедневно. И это наталкивает на очень неприятные выводы.
Так, например, многие «завсегдатаи» нашей косметики – фталаты, акриламиды, формальдегиды и оксиды этилена – включены Управлением по охране окружающей среды Калифорнии в список канцерогенов или репродуктивных токсинов.
Экологической рабочей группой (EWG) в течении пяти лет проводились исследования косметической продукции. В результате была составлена электронная база ингредиентов, включившая в свой состав 14100 брендовых продуктов. Эта база данных имеет перекрестные ссылки на базу данных токсических компонентов. В результате было выявлено, что:
более одной трети всех косметических средств содержат хотя бы один компонент, способный вызвать рак;
57% всей продукции содержит «усилитель проникновения», который помогает химическим веществам быстрее и глубже проникать в кожу и кровеносные сосуды;
79% всей косметики содержит примеси, которые известны как канцерогены.
Все эти примеси не запрещены законом и могут использоваться в косметических средствах без всяких ограничений. Также EWG в своих исследованиях выяснила, что производители на своих этикетках показывают только 11% от действительного количества ингредиентов в косметике.
- Ядовитая десятка. Список самых вредных и опасных веществ в косметике
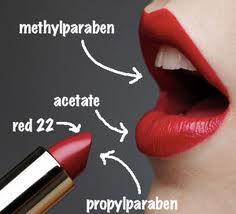
Диоксан - по праву занимают первое место в рейтинге опасных соединений. Это химическое вещество, которое используется в качестве растворителя. Его наличие в косметике очень трудно отследить. Он может образовываться в продукции во время хранения. И если производитель четко не придерживается сроков эксплуатации косметики, то страдают потребители. В 2011 году диоксан был официально запрещен в Калифорнии, США. Остальные штаты никак не прореагировали на данную инициативу. Диоксан является канцерогенным веществом и вызывает рак.
Нитрозамины одни из самых агрессивных канцерогенов. Они могут образовываться при взаимодействие двух абсолютно безвредных веществ. Нитрозамины появляются в любой косметике, которая содержит нитриты. Их использование официально запрещено в Европейском Союзе. При регулярном попадании в кровь человека, нитрозамины многократно увеличивают риск возникновения рака.
Фталаты — это группа промышленных химических пластификаторов, которые используются во многих косметических средствах - от лаков для ногтей до дезодорантов. Именно они вызывают особую озабоченность EWG. Прошлым летом ученные проводили исследования, которые помогли выявить взаимосвязь между фталатами и развитием женских половых признаков у новорожденных младенцев мужского пола. Наличие фталатов в парфюмерии названо главной причиной этого явления. Фталаты, как правило, не указываются на этикетке в качестве ингредиентов. Обнаружить их можно только в лабораторных условиях. Данные исследования привели к тому, что в последнее время в Европейском Союзе был введен запрет на продажу косметических средств, содержащих два наиболее активных фталата - DBP и DEHP. Имейте ввиду, что на продукцию, реализуемую в США и другие страны вне ЕС, этот запрет не распространяется!
Парабены ( парагидробензонат) к сожалению, сейчас присутствуют практически во всех косметических средствах, особенно в лаках для ногтей. Косметика, не содержащая парабенов, встречается редко, стоит существенно дороже и быстрее приходит в негодность. Ведь парабены – это консерванты, сдерживающие рост и размножение микроорганизмов. Неприятная новость – парабены не только могут вызвать симптомы аллергии на косметику, но и имеют способность накапливаться в организме, что иногда приводит к злокачественным образованиям Парабены идентифицированы как разрушители гормональных функций организма. Согласно недавним исследованиям, одним из факторов возникновения рака груди может быть использование дезодорантов, в состав которых входят парабены. Подробнее о том что такое парабены в статье Парабены в косметике
Пропиленгликоль. Это вещество, помогающее сохранять гигроскопичность косметических средств, а по совместительству – продукт нефтепереработки и наиболее частый компонент автомобильных антифризов. Его присутствие в составе косметики - может стать причиной различных кожных заболеваний и аллергических реакций. Споры о безопасности гликолей ведутся до сих пор. О видах гликолей в косметике и безопасных альтернативах в статье Вреден ли пропиленгликоль в косметике?
Вазелин. Вещество, еще более «родное», чем предыдущее. Распространившееся еще во времена наших бабушек из-за неприлично низкой цены и рекламирующееся как увлажняющее средство, вазелин на самом деле нарушает процессы естественного увлажнения кожи и вызывает то, что должен устранять: сухость кожи, возникновение микротрещинок.
Формальдегид. Не смотря на клеймо «канцероген», активно используется в косметологии как консервант. А определение «канцероген» говорит само за себя: формальдегид токсичен, отрицательно влияет не только на кожу, органы дыхания и зрения, но и вредит нервной системе и генетическому составу организма в целом. Опасны и те вещества в составе косметических средств, которые выделяют формальдегид: диазолидинил-мочевина, имидазо-лидинил-мочевина.
Триклозан или триклозан хлорфенол. Помните рекламу антибактериального мыла? Так вот, вещество уничтожает не только вредные, но и полезные бактерии, таким образом разрушая естественный щит организма.
Сополимеры винил пирролидина и винил ацетата. Вещества, которые можно найти в лаках для укладки волос и других фиксирующих средствах. Как бы мы ни старались, при фиксации прически лаком, мы вдыхаем его небольшое количество. И тем самым наносим вред нашим легким.
Ароматизаторы - еще одна серьезная угроза для здоровья. Исследования показали, что 50% всех косметических средств включают в себя дополнительные ароматизаторы — смесь стойких и не стойких химических веществ, наносящих вред организму и живой природе. В 2004 году учеными Стенфордского университета был опубликован доклад, в котором в частности было показано, что мидии мгновенно теряют способность к очищению своих раковин в результате воздействия крошечной частички мускуса.
Одним из первых известных косметических средств можно назвать мыло.
Утро французского короля Людовика XIV начиналось с многочасового ритуала одевания и очень короткого умывания. Ему подносили большую великолепную чашу, на дне которой плескалась вода. Король смачивал кончики пальцев и слегка дотрагивался ими до век. На этом процедура заканчивалась - мыться целиком в те времена было не принято, зато душиться различными духами было насущной необходимостью.
Век гигиены настал только в конце XVIII столетия. Однако мыло было известно задолго до этого. Археологи установили, что уже 6 тысяч лет назад существовало довольно налаженное производство мыла из щелочной соли, растений, золы, животных жиров. В античном мире мыло из козьего или бычьего жира с примесью золы бука было трех сортов: твердое, мягкое и жидкое. Им можно было не только умываться, но и красить волосы в желтый, розовый или красный цвета. А галлы, населявшие территорию современной Франции, использовали для создания причесок из своих длинных волос особую смесь растительного масла и красной земляной краски. Стоило на смесь попасть воде, как образовывалась густая пена. Ее оставалось смыть - и вот они, чистые, блестящие, пушистые волосы!
Скифские женщины делали моющий порошок из древесины кипариса и кедра, затем смешивали его с водой и ладаном. Полученной нежной мазью, имевшей тонкий аромат, они натирали все тело. Затем удаляли раствор скребками, и кожа становилась чистой и гладкой. Хотя мыло уже было изобретено, многие народы еще долго продолжали пользоваться щелоком, бобовой мукой, клеем, пемзой, ячменной закваской и глиной. Даже знаменитый арабский врач Ибн Сина, живший в XI веке, советовал пользоваться мылом только для обмывания прокаженных. Здоровым же он предлагал глину. Кстати, подручные средства, заменяющие мыло, люди используют до сих пор. Земля одного из островов в Эгейском море содержит моющее вещество, с помощью которого жители борются с грязью. Когда идет дождь, весь остров покрывается мыльной пеной.
Но вернемся к истории мыла. В средние века основными его поставщиками в Европе были города Неаполь и Марсель. Постепенно ремеслу варки мыла научились и в других местах. Отношение к этому ремеслу было самое серьезное. В 1399 году в Англии король Генрих IV основал орден, особой привилегией членов которого считалось… мытье в бане с мылом. В этой стране долгое время под страхом смерти члену гильдии мыловаров запрещалось ночевать под одной крышей с мастерами других ремесел - дабы не выдать тайну. Во второй половине XVII века во Франции был издан королевский указ, разрешающий варку мыла только в летнее время и только из золы и оливкового масла. В России мыло начали делать во времена Петра I, но вплоть до середины XIX века им пользовалась только знать. Крестьяне стирали и мылись щелоком - древесную золу заливали кипятком и распаривали в печке. Главным центром мыловарения был город Шуя, на его гербе даже изображен кусок мыла. Широко известны были и московские фирмы - фабрика Ладыгина, фабрика Альфонса Ралле "Ралле и К" и парфюмерная фабрика Брокара, Оборудование фабрики Брокара поначалу состояло из трех котлов, дровяной печи и каменной ступки. Но он сумел стать признанным "королем парфюмерии", выпустив дешевое, копеечное мыло для всех слоев населения. Брокар старался придать недорогой продукции привлекательный вид. Например, его мыло "огурец" так походило на настоящий овощ, что покупалось даже из одного любопытства.
По имеющимся данным, мыло изготовляли ещё в древних Шумере и Вавилоне (около 2800 г. до н. э.). Описание технологии изготовления мыла найдено в Месопотамии на глиняных табличках, относящихся примерно к 2200 г. до н. э. Египетский папирус середины второго тысячелетия до нашей эры свидетельствует, что египтяне регулярно употребляли мыло в омовениях. Широко применяли подобные моющие средства и в Древнем Риме.
Практика показывает, что масла биологического происхождения хорошо снимают загрязнения с поверхности кожи. Это легко заметить при употреблении жирной пищи руками, например жареного на костре мяса. Также примем во внимание тот факт, что в то время, как в южных широтах для мытья проще было использовать растительное масло, в северных это могло быть затруднительным ввиду дороговизны сырья. А топлёный животный жир получать в условиях севера ощутимо легче. Учитывая, что для топления зачастую использовали открытый огонь, смешение топлёного жира с золой или песком — вопрос времени. В дальнейшем необходимо лишь подобрать оптимальный состав жиров для получения однородной эргономичной и приятной смеси.
В 1808 году французский химик Мишель Эжен Шеврёль (1786−1889) по просьбе владельцев текстильной фабрики установил состав мыла. В результате анализа оказалось, что мыло — это натриевая соль высшей жирной (карбоновой) кислоты.
В Европе и США непрерывный процесс мыловарения был отработан в конце 1930-х годов вместе с непрерывным процессом гидролиза (расщепления) жиров водой и паром высокого давления в мыловаренных башнях.
Мыла
А. История мыловарения
Первым моющим средством, разумеется, была обыкновенная вода. Правда, в безводных местностях использовали просто-напросто песок: оттирали им пятна. Но когда одна вода не помогала, в ход шли другие средства: бычья желчь и мозговые кости, разложившаяся моча и свежий помет, яичные желтки и кипящее молоко, мед и пивные дрожжи, теплые отруби и бобовая мука, селитра и гуммиарабик, опилки, зола и прочее, прочее... Неправда ли, похоже на колдовской рецепт? Итак, императорскую тогу топтали ногами в чане с водой и желчью. Однако, чаще использовали разложившуюся мочу животных, содержащую уреаты и аммиак, в присутствии которой вода пенилась. Во многих странах для стирки применяли корни, кору или плоды растений типа мыльнянки. Они содержат жидкость, которая пенится в воде благодаря наличию в ней до 10% сапонинов - моющих веществ природного происхождения. В отварах мыльнянки стирали шелка. При этом ткань не разрушалась и не линяла. На Антильских островах и в наше время используют для стирки кору белого орехового дерева. Почти по всей Европе вдоль ручьев и рек, в низинах и канавах растет дикая разновидность обыкновенной мыльнянки. Этой травой стирали и в бедных хижинах, и в богатых усадьбах. Уличную грязь (в которой недостатка не было) смывали так: сначала одежду опускали в горячий раствор бычьей желчи, а затем полоскали в ключевой воде. Высохший костюм посыпали мелким чистым песком, били палками, терли щетками. Еще одно признанное средство - смесь древесных опилок, воды и гуммиарабика. И, конечно же, многие столетия стирали с помощью поташа, соды или древесной золы. Для этого в бочку с нагретой до кипения водой клали белье, а затем насыпали соду или опускали мешочек с золой и все тщательно перемешивали.
Самое раннее описание мыловарения было обнаружено учеными на шумерских табличках, датируемых 2500 годом до н.э. Судя по этим записям, мыло изготавливалось путем смеси воды и древесной золы, которую кипятили и в последствии растапливали в ней жир, получая тем самым мыльный раствор. Но, к сожалению, свидетельств применения данного раствора в шумерские времена не сохранилось.
Легенда гласит, что само слово soap (мыло) произошло от названия горы Сапо в древнем Риме, где совершались жертвоприношения богам. (У римлян мыло называлось sapo. Из этого слова позднее у англичан образовалось soap, у французов - savon, у итальянцев - sapone.) Животный жир, выделяющийся при сжигании жертвы, скапливался и смешивался с древесной золой костра. Поученная масса смывалась дождем в глинистый грунт берега реки Тибр, где жители стирали белье и, естественно, наблюдательность человека не упустила того факта, что благодаря этой смеси одежда отстирывалась гораздо легче. Поэтому долгое время изобретение мыла приписывалось именно римлянам. Именно в Риме мыловарение приобрело широкое распространение и выделилось в отдельную ремесленную отрасль. Так при раскопках Помпеи археологами была раскопана мыловарня, где найдены готовые куски мыла.
О мыловарении упоминает также римский писатель и ученый Плиний Старший в своем основном трактате «Естественная история» в тридцати семи томах. Данный источник представляет собой энциклопедию естественных знаний античности, и упоминание в нем мыловарения однозначно говорит о том, что к тому времени его продукт стал неотъемлемой частью жизни римского населения. Плиний писал о способах приготовления мыла путем омыления жиров. При этом изготавливалось как твердое, так и мягкое мыло, получаемое с использованием соды и древесной золы (поташа). Твердое мыло отличалось своей жесткостью и использовалось исключительно для стирки, в то время как мягкое мыло использовалось в косметических целях, в том числе и для укладки волос.
После падения Римской империи и с началом так называемого темного времени в Европе, чистота и личная гигиена отошли на второй план, поэтому производство мыла пошло на спад, но рецепты не были утеряны и небольшие кустарные мастерские продолжали дело мастеров древности.
В Западной Европе ремесло мыловарения окончательно сформировалось только к концу XVII века. Немаловажную роль в развитии мыловарения сыграл географический фактор. Ингредиенты для приготовления мыла варьировались в зависимости от региона. На севере при варке мыла применялся животный жир, а на юге использовалось оливковое масло, благодаря которому мыло получалось превосходного качества.
Об изготовлении мыла в средние века имеются лишь скудные сведения. Вероятно, арабы в VII веке н. э. узнали способ обработки мыльного раствора гашеной известью и таким образом стали изготавливать твердое мыло. От арабов искусство мыловарения проникло в Испанию. Здесь научились делать твердое красивое мыло из оливкового масла и золы морских растений. Повсюду на Средиземноморье, где выращивали масличные растения, стало процветать мыловарение. Центрами были Аликанте, Карфаген, Севилья, Савона, Венеция, Генуя, а с XVI века также Марсель и Неаполь, благодаря наличию на близлежащей территории сырьевых источников, то есть оливкового масла и соды. Масло, получаемое после первых двух прессовок, употреблялось в пищу, а после третьей использовалось для приготовления мыла. С этого времени мыло начало все более широко применяться в качестве моющего средства.
Во дворцах знати эпохи Ренессанса стали уделять большое внимание чистоте, но еще большее - приятному запаху. Существовала мода на запахи, поэтому изготовление душистых веществ и мыла в те времена находилось под влиянием модных веяний из Парижа. Еще бы! Где же найти ароматические вещества, как не на юге Франции с его обилием цветов, которые издавна здесь выращивали. Иногда мыло служило подарком. Крестоносцы в XII веке привозили знаменитые мыльные шарики из Дамаска и приносили в дар своим возлюбленным. В XV и XVI веках рыцари и купцы привозили пахнущие шарики из Венеции. На них были вытиснены лилии, еловые шишки, полумесяцы - первые, если можно так сказать, торговые знаки.
Во времена Каролингов искусство мыловарения было широко распространено. Управляющим и арендаторам в Аквитании (Юго-Западная Франция) было указано при наборе батраков следить за тем, чтобы среди них были люди, умеющие варить мыло. Любящий роскошь французский король Людовик XIV лично интересовался производством туалетного мыла. Гольберт, его министр финансов, "выписал" из Генуи специалистов по мыловарению. Возникла новая промышленность, оказавшаяся вскоре под защитой французского государства, которой предписывалось использовать только душистые масла из Прованса. Марсель стал метрополией производства такого ценного мыла. Развитию мыловарения способствовало наличие сырьевых источников. Например, марсельская мыловаренная промышленность, известная с эпохи раннего средневековья, располагала оливковым маслом и содой. Оливковое масло получают простым холодным прессованием плодов масличных деревьев. Масло, получаемое после первых двух прессовок, употребляли для пищевых целей, а после третьей – использовали для переработки на мыло. Марсельское мыло было важным товаром торговли уже в IX в. Оно уступило свое место международной торговле венецианскому мылу лишь с конца средних веков (XIV в.) Кроме Франции, мыловарение в Европе развивалось в Италии, Греции, Испании, на Кипре, т.е. в районах, культивирующих оливковые деревья. Первые германские мыловарни были основаны в XIV столетии.
Лишь с конца XIV века марсельское мыло уступило свое место в международной торговле венецианскому. Так же мыловарение активно развивалось в Италии, Греции и Испании. В XV веке в Италии, в Севоне, начали впервые выпускать твердое мыло промышленным путем. При этом жиры соединялись не с золой, а с природной кальцинированной содой. Это значительно снижало себестоимость мыла, а, следовательно, перевело мыловарение его из разряда ремесленного производства в мануфактурное. Начиная с XIV века, мыловарни стали появляться и в Германии. Для варки мыла использовали говяжье, баранье, свиное, лошадиное сало, костяной, китовый и рыбий жир, отходы жиров различных производств. Добавляли и растительные масла - льняное, хлопковое, оливковое.
С мылом связаны разнообразные перлы истории, основанные на серьезности отношения к ремеслу мыловарения. В 1399 году в Англии король Генрих IV основал орден, особой привилегией членов которого считалось… мытье в бане с мылом. В этой стране долгое время под страхом смерти члену гильдии мыловаров запрещалось ночевать под одной крышей с мастерами других ремесел - дабы не выдать тайну. Во второй половине XVII века во Франции был издан королевский указ, разрешающий варку мыла только в летнее время и только из золы и оливкового масла.
История мыловарения в России уходит своими корнями в допетровскую эпоху. В античные времена использовали специальные глины, способные сорбировать грязь и пыль с одежды. Кстати, название Сапун-горы под Севастополем означает "мыльная гора". Глину, добываемую на этой горе, использовали для мытья тела и стирки одежды. Главным центром мыловарения был город Шуя, на его гербе даже изображен кусок мыла. Но русские умельцы быстро научились изготавливать мыло из поташа и животных жиров. Таким образом, в каждом доме было налажено производства этого столь необходимого в быту продукта. Ширилось число мелких мыловаренных мастерских, тем более что Россия располагала всеми необходимыми для этого ресурсами, и в первую очередь древесиной, так как в основе поташа лежала именно зола.
Поташ стал одним из основных продуктов экспорта, что привело к массовой вырубке лесов. К началу царствования Петра I остро встал вопрос о поиске более дешевого заменителя поташа. Проблема была решена в 1685 году, когда французский химик Николас Лебман смог получить из поваренной соли соду. Этот отличный щелочной материал вытеснил поташ.
В связи с особыми экономическими условиями, первые мыловаренные фабрики стали появляться в России лишь в XVIII веке. В Москве на тот момент было известно две: в Новинской и Пресненской частях. К 1853 году в Московской губернии их число выросло до восьми. Потребителями мыловаренных заводов стали многочисленные суконные, ситценабивные и красильные фабрики.
Б. Процесс приготовления мыла на Востоке (традиционное алеппское мыло)
Технология производства традиционного алеппского мыла включает в себя 3 этапа: подготовка первичных продуктов, омыление и обработка готового продукта
1. Подготовка первичных продуктов:Натуральная сода не совсем подходит для прямого использования, поскольку её реакция с маслами очень слабая. Её следует обработать известью, чтобы получить каустическую соду. Процесс каустификации соды был изобретён в Алеппо в VIII веке нашей эры, и с того момента начинается история твердого мыла.
2. Омыление в чанах (традиционный способ)Цель этого этапа – спровоцировать химическую реакцию между маслом и щелочью, и в результате получается вязкая мыльная масса. Традиционный способ занимает более недели и включает в себя четыре подэтапа: подготовка, снижение растворимости, варка и выщелачивание
2.1. Подготовка.
В каменный чан на 5 тонн заливается масло и добавляется каустическая сода, в определенной пропорции (кол-во соды должно быть достаточным для полного омыления масла), масса интенсивно перемешивается вручную и нагревается до температуры кипения (при этом в чане обязательно присутствует вода). Процесс омыления масла длится 8 часов и это очень деликатная операция, поскольку даже незначительная ошибка мыловара может привести к неудаче.
Мыльная масса, полученная в результате этой операция, оставляется «отдыхать» на 12 часов.
2.2. Снижение растворимости.
Реакция омыления приводит к возникновению мыла и глицерина. Продукты отделяются друг от друга путем добавления солёной воды. Масса разделяется на два слоя; нижняя часть, смешанная с водой, извлекается через трубу в низу чана, через 6 часов «отдыха». Тем не менее, часть воды оставляют в чане, для того, чтобы содействовать дальнейшему кипению.
2.3. Варка.
Мыльная масса, полученная путем снижения растворимости и остающаяся в чане, нагревается и кипит «на медленном огне» на протяжении многих часов; также добавляется дополнительное количество соды, чтобы гарантировать полное превращение масла в мыло. Потом масса 12 часов «отдыхает», потом через нижнюю трубу сливают воду, которая осталась в нижней части чана.
2.4. Выщелачивание.
Это процесс удаляет излишки соды в мыле. Массу кипятят с соленой водой 2-3 раза, до тех пор, пока мыло не будет содержать ровно изначально заданную пропорцию соды. Выщелачивание длится 4 часа. После 12-тичасового перерыва, вода, отделившаяся от мыльной массы – щелок – удаляется.
Наконец, теплая мыльная масса извлекается из чана, разливается на пол, на заранее расстеленную на нем бумагу, в результате чего она охлаждается и теряет излишки воды.
Стадии конечной обработки: нарезка, затвердение, формовка. Все эти фазы, как и остальные, делаются полностью вручную.
3.1. Нарезка.
После дневного перерыва, мыльная масса переходит из жидкого состояния в более твердое. После разметки горизонтальных и вертикальных линий на поверхности мыла, нарезка производится при помощи длинного ножа, зафиксированного на грифе, который тянут помощники мыловара, одетые в специальную обувь – обычные плоские дощечки, привязанные к ногам (чтобы не оставлять на мыле следов). После нарезки все мыло маркируется печатью фабрики.
3.2. Затвердение.
Мыло, нарезанное на бруски, переносят в наиболее проветриваемую часть фабрики, чтобы оно сушилось на открытом воздухе, где бруски в шахматном порядке раскладываются (либо складываются в башенки). На протяжении долгого времени мыло постепенно затвердевает, теряя при этом излишки воды. Мыло сушится не менее 9 месяцев.
3.3. Формовка.
Приготовленное таким образом традиционное алеппское мыло нарезается – из него делают мыльную стружку. И уже из этой стружки делают любое формовое мыло, либо используют стружку для изготовления прессованного мыла.
В. Химические процессы при мыловарении
Несмотря на то, что в конце эпохи средневековья в разных странах существовала довольно развитая мыловаренная промышленность, химическая сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления. В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового масла с оксидом свинца и водой образуется сладкое и растворимое в воде вещество. Решающий шаг на пути изучения химической природы жиров был сделан французским химиком Шеврелем. Он открыл стеариновую, пальмитиновую и олеиновую кислоты, как продукты разложения жиров при их омылении водой и щелочами. Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет спустя Бертло установил природу глицерина и объяснил химическое строение жиров. Глицерин – трехатомный спирт. Жиры – сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой CH3(CH2)14COOH, стеариновой CH3(CH2)16COOH и олеиновой CH3(CH2)7CH = CH(CH2)7COOH. Их формулу и реакцию гидролиза можно описать следующим образом:
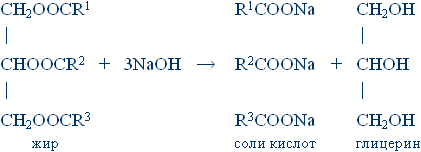
В состав различных жиров входят в различных соотношениях пальмитиновая, стеариновая, олеиновая и другие кислоты. В растительных (жидких) жирах преобладают непредельные кислоты (содержащие этиленовые связи), а в животных (твердых) – предельные кислоты, т.е. не содержащие двойных связей. Потребности в твердых животных жирах большие, чем в растительных. Поэтому жидкие растительные жиры переводят в твердые каталитической гидрогенизацией. В этом процессе остатки непредельных кислот в глицеридах превращаются (присоединением водорода) в остатки предельных кислот. Например:
CH3(CH2)7CH = CH(CH2)7COOH
|
[катализатор 190...240°C]
↓
CH3(CH2)7CH2 – CH2(CH2)7COOH
Именно так получают кулинарные жиры, масло для обжаривания, салатное масло, а также жиры, идущие на производство маргарина. Гидрированные жиры называют саломаслами (сало из масла).
Важно то, что среди остатков различных кислот в глицеридах (жирах) присутствует остаток линолевой кислоты CH3(CH2)4CH = CHCH2CH2CH = CH(CH2)7COOH. В отличие от других эта кислота не синтезируется в организме человека, а вводится только с пищей. В настоящее время существует утвердившееся мнение, что линолевая кислота необходима для предотвращения атеросклероза – распространенной болезни, служащей одной из главных причин потери трудоспособности и преждевременной смерти. Необходимо отметить, что линолевая кислота непредельная, а значит, она входит в состав главным образом растительных жиров.
В быту, не говоря о промышленности, мойке подвергают разные предметы и объекты. Загрязняющие вещества бывают самые разнообразные, но чаще всего они малорастворимы или нерастворимы в воде. Такие вещества, как правило, являются гидрофобными, поскольку водой не смачиваются и с водой не взаимодействуют. Поэтому нужны и различные моющие средства.
Если попытаться дать определение, то мытьем можно назвать очистку загрязненной поверхности жидкостью, содержащей моющее вещество или систему моющих веществ. В качестве жидкости в быту используют главным образом воду. Хорошая моющая система должна выполнять двойную функцию: удалять загрязнение с очищаемой поверхности и переводить его в водный раствор. Значит, моющее средство также должно обладать двойной функцией: способностью взаимодействовать с загрязняющим веществом и переводить его в воду или водный раствор. Следовательно, молекула моющего вещества должна иметь гидрофобную и гидрофильную части. Фобос – по-гречески означает страх, боязнь. Значит, гидрофобность означает боящийся, избегающий воду. Филео – по-гречески – люблю, а гидрофильность – любящий, удерживающий воду. Гидрофобная часть молекулы моющего вещества обладает способностью взаимодействовать с поверхностью гидрофобного загрязняющего вещества. Гидрофильная часть моющего вещества взаимодействует с водой, проникает в воду и увлекает с собой частицу загрязняющего вещества, присоединенную к гидрофобному концу.
Таким образом, моющие вещества должны обладать способностью адсорбироваться на пограничной поверхности, т.е. обладать поверхностной активностью. Их называют поверхностно-активными веществами (ПАВ).
Соли тяжелых карбоновых кислот, например CH3(CH2)14COONa, являются типичными поверхностно-активными веществами. Они содержат гидрофильную часть (в данном случае – карбоксильную группу) и гидрофобную часть (углеводородный радикал).
Животные жиры – древнее и весьма ценное сырье мыловаренной промышленности. Они содержат до 40% (насыщенных) жирных кислот. Искусственные, т.е. синтетические, жирные кислоты получают из парафина нефти каталитическим окислением кислородом воздуха. В упрощенном виде реакцию можно описать следующим уравнением:
CH3(CH2)mCH2 – CH2(CH2)nCH3 + 2,5O2
↓
CH3(CH2)mCOOH + CH3(CH2)nCOOH + H2О
Молекула парафина при окислении разрывается в разных местах и потому получается смесь кислот, которые разделяются на фракции. При производстве мыла используют две фракции: C10–C16 и C17–C20. В хозяйственное мыло синтетические кислоты вводят в количестве 35...40%. Для производства мыла также применяют нафтеновые кислоты, выделяемые при очистке нефтепродуктов (бензина, керосина и др.). С этой целью нефтепродукты обрабатывают раствором гидроксида натрия и получают водный раствор натриевых солей нафтеновых кислот (монокарбоновые кислоты ряда циклопентана и циклогексана). Этот раствор упаривают и обрабатывают поваренной солью, в результате чего на поверхность раствора всплывает мазеобразная масса темного цвета – мылонафт. Для очистки мылонафт обрабатывают серной кислотой, т.е. вытесняют из солей сами нафтеновые кислоты. Этот нерастворимый в воде продукт называют асидолом или асидол-мылонафтом. Непосредственно из асидола можно изготавливать только жидкое или, в крайнем случае, мягкое мыло. Оно имеет нефтяной запах, но зато обладает бактерицидными свойствами.
В производстве мыла давно используют канифоль, которую получают при переработке живицы хвойных деревьев. Канифоль состоит из смеси смоляных кислот, содержащих в цепи около 20 углеродных атомов. В рецептуру хозяйственного мыла обычно вводят 12...15% канифоли от массы жирных кислот, а в рецептуру туалетных мыл – не более 10%. Введение канифоли в больших количествах делает мыло мягким и липким.
Процесс производства мыла состоит из химической и механической стадий. На первой стадии (варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот или их заменителей (нафтеновых, смоляных). На второй стадии проводят механическую обработку этих солей – охлаждение, сушку, смешивание с различными добавками, отделку и упаковку.
Варку мыла заканчивают обработкой мыльного раствора (мыльного клея) избытком щелочи (NaOH) или раствором NaCl. В результате этого на поверхность раствора всплывает концентрированный слой мыла, называемый ядром. Полученное таким образом мыло называют ядровым, а процесс его выделения из раствора – отсолкой или высаливанием. При высаливании происходит повышение концентрации мыла и его очистка от белковых, красящих и механических примесей – так получают хозяйственное мыло.
Если мыло варилось из животных или растительных жиров, то из раствора после отделения ядра выделяют образующийся в результате омыления глицерин. Он находит широкое и разнообразное применение: в производстве взрывчатых веществ (тринитроглицерина) и полимерных смол; в качестве умягчителя тканей и кожи; для парфюмерных, косметических и медицинских препаратов; при производстве кондитерских изделий и ликеров. Последним он придает вязкую консистенцию.
Для получения особо чистого и светлого мыла его очищают (шлифуют) переведением снова в раствор кипячением с горячей водой и повторным высаливанием. В результате шлифования мыло приобретает большую однородность, низкую вязкость и надлежащую пластичность. Для изготовления туалетного мыла в очищенном ядровом мыле снижают содержание воды от 30 до 12%. Затем в него вводят парфюмерные отдушки, отбеливатели типа TiO2, красители и др. Хорошие сорта туалетного мыла содержат до 50% мыла, полученного из импортного кокосового или пальмового масла. Кокосовое масло хорошо растворяется в холодной воде и характеризуется высоким пенообразованием. Иногда туалетное мыло содержит до 10% свободных жирных кислот. Самое дорогое туалетное мыло целиком изготавливают из кокосового масла.
Для улучшения некоторых характеристик хозяйственного мыла (иногда и туалетного), а также для удешевления в него вводят наполнители. К ним относятся некоторые натриевые соли (Na2CO3, Na2B4O7, Na5P3O10, жидкое стекло), которые при растворении в воде приводят к подщелачиванию, клеи (казеин, казеиновый студень), углеводы (крахмал). Клеи и крахмал способствуют пенообразованию мыльного раствора и стойкости пены, однако моющей способностью не обладают. Для получения паст в жидкое хозяйственное мыло вводят тонкоизмельченный песок, толченый кирпич, жирные глины. Они способствуют механической очистке. Такие мыла применяют для чистки кухонной посуды, некрашеной мебели, полов и т.д.
Особое место среди наполнителей занимает сапонин, получаемый выщелачиванием некоторых растений и прежде всего мыльного корня. Он хорошо растворяется в воде и его растворы сильно пенятся. Поэтому сапонин используют для улучшения пенообразования и применяют для дорогих сортов мыл.
Следует отметить, что замена натрия на калий приводит к изменению консистенции мыла. Из твердого оно становится мягким или мазеобразным.
Ионы кальция и магния образуют с анионами тяжелых карбоновых кислот малорастворимые соли. Этот процесс можно выразить уравнениями:
2RCOONa + Ca(HCO3)2 = Ca(RCOO)2 + 2NaHCO3
2RCOONa + MgCl2 = Mg(RCOO)2 + 2NaCl
Поэтому при стирке белья в жесткой воде, содержащей эти ионы, расход мыла повышается на 25...30%. Малорастворимые соли кальция и магния оседают на ткани, забивают поры и потому делают ткань грубой, менее эластичной, с плохой воздухо- и влагопроницаемостью. Такие ткани приобретают сероватый оттенок, а окраска становится блеклой. Кроме того, осевшие на ткани известковые мыла приводят к снижению ее прочности. Это происходит потому, что анионы ненасыщенных карбоновых кислот при сушке тканей окисляются кислородом воздуха с образованием веществ пероксидного характера. Они же окисляют целлюлозу, из которой состоят ткани. Для устранения вредных последствий жесткой воды в мыла вводят натрий трифосфат Na5P3O10. Анион P3O510– связывает ионы Ca2+ и Mg2+ в прочные, но растворимые в воде соединения. По существу они играют роль умягчителя воды. С этой же целью натрий трифосфат и другие полифосфатные анионы добавляют и в стиральные порошки.
Г. Ингредиенты для мыла
Гидроксид натрия (лат. Natrii hydroxidum; другие названия — каустическая сода, каустик, едкий натр, едкая щёлочь) — самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется более 57 миллионов тонн едкого натра.
Интересна история тривиальных названий как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разъедать кожу, бумагу, и другие органические вещества, вызывая сильные ожоги. До XVII века щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой (по растению Salsola Soda, из золы которого её добывали), а карбонат калия — поташем. В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.
Термодинамика растворов
ΔH0 растворения для бесконечно разбавленного водного раствора -44,45 кДж/моль.
Из водных растворов при 12,3—61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH0обр −425,6 кДж/моль), в интервале от -28 до -24 °C — гептагидрат, от -24 до -17,7 °C — пентагидрат, от -17,7 до -5,4 °C — тетрагидрат (α-модификация), от -5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t = 28 °C), в этаноле 14,7 г/л (t = 28 °C). NaOH·3,5Н2О (температура плавления 15,5 °C);
с жирами (омыление), такая реакция необратима, так как получающаяся кислота со щёлочью образует мыло и глицерин. Глицерин впоследствии извлекается из подмыльных щёлоков путём вакуум-выпарки и дополнительной дистилляционной очистки полученных продуктов. Этот способ получения мыла был известен на Ближнем Востоке с VII века:
(C17H35COO)3C3H5 + 3NaOH → C3H5(OH)3 + 3C17H35COONa
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
Несмотря на то что в конце эпохи средневековья в разных странах существовала довольно развитая мыловаренная промышленность, химическая сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления. В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового масла с оксидом свинца и водой образуется сладкое и растворимое в воде вещество. Решающий шаг на пути изучения химической природы жиров был сделан французским химиком Шеврелем. Он открыл стеариновую, пальмитиновую и олеиновую кислоты, как продукты разложения жиров при их омылении водой и щелочами. Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет спустя Бертло установил природу глицерина и объяснил химическое строение жиров. Глицерин – трехатомный спирт. Жиры – сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой CH3(CH2)14COOH, стеариновой CH3(CH2)16COOH и олеиновой CH3(CH2)7CH = CH(CH2)7COOH.
В состав различных жиров входят в различных соотношениях пальмитиновая, стеариновая, олеиновая и другие кислоты. В растительных (жидких) жирах преобладают непредельные кислоты (содержащие этиленовые связи), а в животных (твердых) – предельные кислоты, т.е. не содержащие двойных связей. Потребности в твердых животных жирах большие, чем в растительных. Поэтому жидкие растительные жиры переводят в твердые каталитической гидрогенизацией. В этом процессе остатки непредельных кислот в глицеридах превращаются (присоединением водорода) в остатки предельных кислот.
Именно так получают кулинарные жиры, масло для обжаривания, салатное масло, а также жиры, идущие на производство маргарина. Гидрированные жиры называют саломаслами (сало из масла).
Важно то, что среди остатков различных кислот в глицеридах (жирах) присутствует остаток линолевой кислоты CH3(CH2)4CH = CHCH2CH2CH = CH(CH2)7COOH. В отличие от других эта кислота не синтезируется в организме человека, а вводится только с пищей. В настоящее время существует утвердившееся мнение, что линолевая кислота необходима для предотвращения атеросклероза – распространенной болезни, служащей одной из главных причин потери трудоспособности и преждевременной смерти. Необходимо отметить, что линолевая кислота непредельная, а значит, она входит в состав главным образом растительных жиров.
В быту, не говоря о промышленности, мойке подвергают разные предметы и объекты. Загрязняющие вещества бывают самые разнообразные, но чаще всего они малорастворимы или нерастворимы в воде. Такие вещества, как правило, являются гидрофобными, поскольку водой не смачиваются и с водой не взаимодействуют. Поэтому нужны и различные моющие средства.
Если попытаться дать определение, то мытьем можно назвать очистку загрязненной поверхности жидкостью, содержащей моющее вещество или систему моющих веществ. В качестве жидкости в быту используют главным образом воду. Хорошая моющая система должна выполнять двойную функцию: удалять загрязнение с очищаемой поверхности и переводить его в водный раствор. Значит, моющее средство также должно обладать двойной функцией: способностью взаимодействовать с загрязняющим веществом и переводить его в воду или водный раствор. Следовательно, молекула моющего вещества должна иметь гидрофобную и гидрофильную части. Фобос – по-гречески означает страх, боязнь. Значит, гидрофобность означает боящийся, избегающий воду. Филео – по-гречески – люблю, а гидрофильность – любящий, удерживающий воду. Гидрофобная часть молекулы моющего вещества обладает способностью взаимодействовать с поверхностью гидрофобного загрязняющего вещества. Гидрофильная часть моющего вещества взаимодействует с водой, проникает в воду и увлекает с собой частицу загрязняющего вещества, присоединенную к гидрофобному концу.
Таким образом, моющие вещества должны обладать способностью адсорбироваться на пограничной поверхности, т.е. обладать поверхностной активностью. Их называют поверхностно-активными веществами (ПАВ).
Соли тяжелых карбоновых кислот, например CH3(CH2)14COONa, являются типичными поверхностно-активными веществами. Они содержат гидрофильную часть (в данном случае – карбоксильную группу) и гидрофобную часть (углеводородный радикал).
Животные жиры – древнее и весьма ценное сырье мыловаренной промышленности. Они содержат до 40% (насыщенных) жирных кислот. Искусственные, т.е. синтетические, жирные кислоты получают из парафина нефти каталитическим окислением кислородом воздуха.
Молекула парафина при окислении разрывается в разных местах и потому получается смесь кислот, которые разделяются на фракции. При производстве мыла используют две фракции: C10–C16 и C17–C20. В хозяйственное мыло синтетические кислоты вводят в количестве 35...40%. Для производства мыла также применяют нафтеновые кислоты, выделяемые при очистке нефтепродуктов (бензина, керосина и др.). С этой целью нефтепродукты обрабатывают раствором гидроксида натрия и получают водный раствор натриевых солей нафтеновых кислот (монокарбоновые кислоты ряда циклопентана и циклогексана). Этот раствор упаривают и обрабатывают поваренной солью, в результате чего на поверхность раствора всплывает мазеобразная масса темного цвета – мылонафт. Для очистки мылонафт обрабатывают серной кислотой, т.е. вытесняют из солей сами нафтеновые кислоты. Этот нерастворимый в воде продукт называют асидолом или асидол-мылонафтом. Непосредственно из асидола можно изготавливать только жидкое или, в крайнем случае, мягкое мыло. Оно имеет нефтяной запах, но зато обладает бактерицидными свойствами.
В производстве мыла давно используют канифоль, которую получают при переработке живицы хвойных деревьев. Канифоль состоит из смеси смоляных кислот, содержащих в цепи около 20 углеродных атомов. В рецептуру хозяйственного мыла обычно вводят 12...15% канифоли от массы жирных кислот, а в рецептуру туалетных мыл – не более 10%. Введение канифоли в больших количествах делает мыло мягким и липким. [5]
Д. Компоненты мыла
Компоненты и Ингредиенты используемые в мыловарении
При производстве мыла одним из главных компонентов являются натуральные растительные масла
РАСТИТЕЛЬНЫЕ МАСЛА жирные (жиры растительные), продукты, извлекаемые из растит. сырья и состоящие в основном из триглицеридов высших жирных кислот. Основные источники растительных масел - масличные растения (масличные культуры). Растительные масла содержатся также в косточках некоторых плодовых деревьев (абрикос, персик, вишня, черешня, миндаль), семенах винограда, арбуза, томатов, табака, чая, а также в различных маслосодержащих отходах пищевых производств перерабатывающих сельско-хозяйственное сырье. К последним относят главным образом отруби и зародыши семян зерновых культур. В оболочке зерна пшеницы и ржи содержится 5-6% масла, в зародыше-11-13 и 10-17% соотв.; в зародыше кукурузы 30-48% масла, проса-около 27%, риса-24-25%. Содержание масла в растениях и его качество зависят от сорта растения, условий произрастания (удобрения, обработка почвы), степени зрелости плодов и семян.
Состав и свойства. Растительные масла на 94-96% состоят из смесей триглицеридов высших жирных кислот (табл. 1). Оставшуюся часть составляют вещества, близкие к жирам (например, фосфолипиды, стерины, витамины), свободные жирные кислоты и др. компоненты.
Плотность растительных масел 0,87-0,98 г/см3 (табл. 2); большинство из них растворяются в бензине, бензоле, дихлорэтане, сероуглероде, ацетоне, диэтиловом эфире, СС14; ограниченно растворяется в этаноле и метаноле, не растворяется в воде.
Свойства растительных масел определяются главным образом составом и содержанием жирных кислот, образующих триглицериды. Обычно это насыщенные и ненасыщенные одноосновные жирные кислоты с неразветвленной углеродной цепью и четным числом атомов углерода (преим. С16 и С18). В подавляющем большинстве растительные масла содержат смеси глицеридов различных кислот, в некоторых присутствуют и глицериды одной кислоты. Кроме того, в растительных маслах, обнаружены в небольших количествах глицериды жирных кислот с нечетным числом атомов углерода.
В зависимости от состава триглицеридов растительные масла могут быть жидкими (подсолнечное, хлопковое, соевое, рапсовое, кукурузное, льняное и др.) и твердыми (кокосовое, пальмовое, пальмоядровое и др.). У жидких масел, содержащих главным образом непредельные кислоты, температура застывания ниже 0°С, у твердых - достигает 40 °С. При контакте с О2 воздуха или при нагревании до 250-300°С многие растительные масла подвергаются окислительной полимеризации ("высыхают"), образуя пленки. По способности к высыханию растительные масла условно подразделяют на высыхающие, полувысыхающие и невысыхающие. Первые, например льняное масло, конопляное и тунговое масла, содержат главным образом триглицериды кислот с двумя или тремя двойными связями (линолевой, линоленовой, элеостеариновой); вторые, например подсолнечное масло, соевое и маковое масла,-триглицериды кислот с одной или двумя двойными связями (олеиновой, линолевой); третьи, например кокосовое и пальмовое масла,-преим. триглицериды насыщенные кислотами (лауриновой, пальмитиновой, стеариновой) и небольшое количествово монрненасыщенной олеиновой. Невысыхающее касторовое масло содержит тригли-церидрицинолевой кислоты.
При анализе состава растительных масел кол-во высших жирных кислот, образующихся при омылении, характеризуют числом омыления, степень ненасыщенности - йодным и родановым числами.
Компоненты растительных масел, отличные от триглицеридов, подразделяют на омыляемые и неомыляемые. К первым относят свободные жирные кислоты (содержание 1-2%), фосфолипиды (0,5-4%), стерины (0,3-1,3%), воски и воскообразные вещества (0,002-0,4%), пигменты (не более 0,16%), ко вторым - белки (0,1-1,5%), витамины (до 0,5%), углеводороды и другие.
Свободные жирные кислоты могут содержаться в растительном сырье (семенах недозревших растений или семенах, самосозревающих при хранении во влажном состоянии) или образовываться в процессе выделения масла в результате частичного гидролиза триглицеридов (высшие жирные кислоты) и их окисления под действием света и при длительном хранении (низкомолекулярные жирные кислоты - масляная, каприновая, капроновая, каприловая, ацетоуксусная, уксусная). Суммарное содержание свободных кислот в % по массе в растительных маслах определяет их кислотность и характеризуется кислотным числом. Наличие свободных низкомолекулярных жирных кислот, растворимых в воде и испаряющихся при нагревании, характеризуется числом Рейхарта-Мейсля; наличие кислот, не растворяющихся в воде, но способных испаряться при нагревании, числом Поленске. Оба этих числа определяются количеством мл 0,1 н. раствора КОН, расходуемого на нейтрализацию 5 г растительного масла в определенных условиях. Содержание нерастворимых кислот и неомыляемых компонентов характеризуется числом Генера (содержание их в % в 100 г растительного масла).
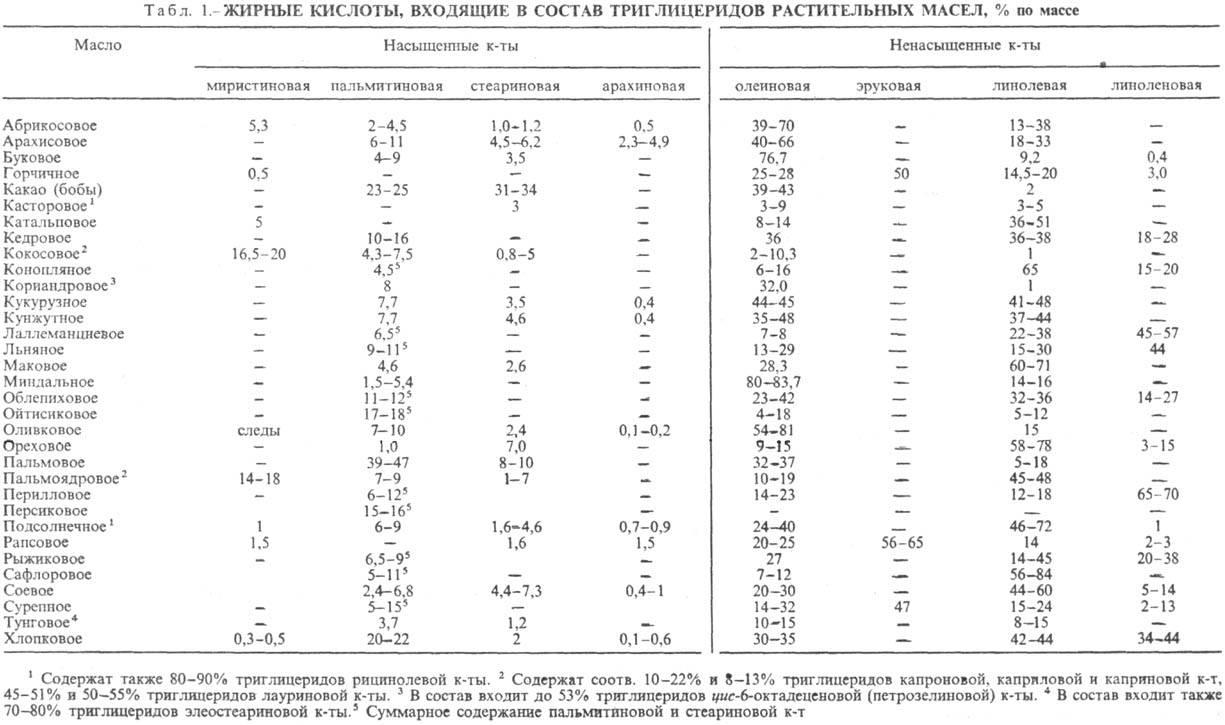
Фосфолипиды в растительных маслах представлены главным образом глицеро-фосфатидами (лецитины), в меньшем количестве -инозитфосфалидами и сфингомиелинами. Фосфолипиды растительных масел участвуют в биологическом окислении масел в организме и сами по себе представляют большую ценность. Однако в растительных маслах они образуют коллоидные растворы, из которых при поглощении воды коагулируют с образованием осадков, называемых фузами. В таких осадках могут происходить гидролитические процессы, приводящие к потере масел и затруднениям при переработке. Под действием О2 воздуха фосфолипиды легко окисляются с образованием темноокрашенных соединений, ухудшающих качество масел. Поэтому растительные масла, не идущие непосредственно в пищу или подвергающиеся дальнейшей переработке (например, рафинированию), очищают-вт фосфолипидов, подвергая масло гидратации, или связывая с помощью различных химических агентов, например диметилдиаллиламмоний-хлорида. Выделенные фосфолипиды, учитывая их биологическую и пищевую ценность, используют для производства фосфолипидных концентратов, которые добавляют во многие пищевые продукты (напр., маргарин) и корма для животных.
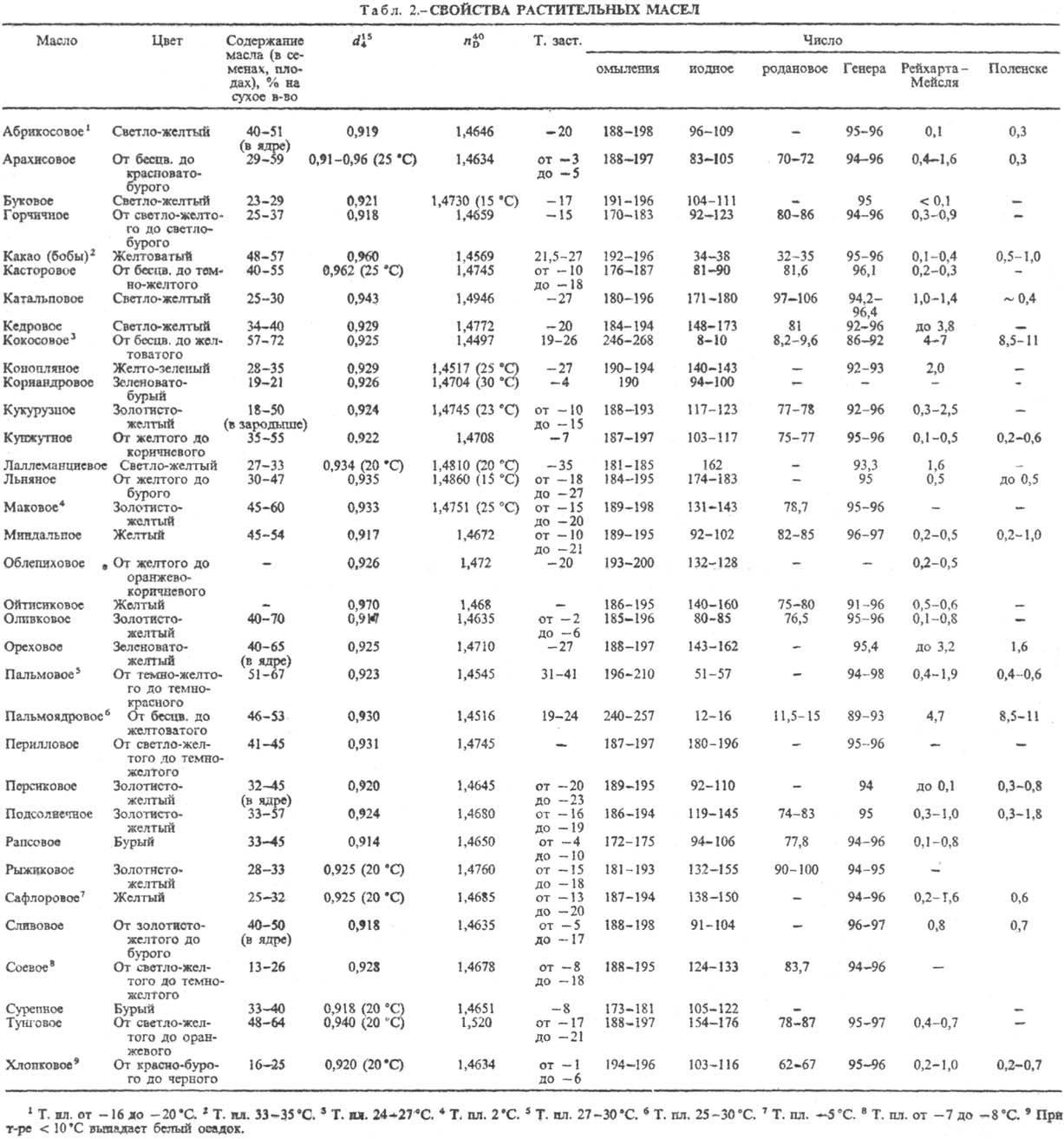
Из стеринов растительного происхождения (фитостеринов) в растительных маслах наиболее часто содержатся ситостерин и стигмастерин, являющиеся предшественниками витамина D. Холестерин в растительных маслах практически не содержится. Наибольшее количество стеринов содержится в кукурузном масле-0,42-1,38%, в подсолнечном их 0,25-0,53%, в хлопковом 0,26-0,57%, в соевом 0,35-0,40%. При переработке и очистке растительных масел потери стеринов стараются свести к минимуму. При необходимости стерины из растительных масел могут быть извлечены с помощью алкалоида дигитонина, с которым они дают нерастворимые в этаноле соединения.
Воски и воскообразные вещества в растительных маслах образуют эмульсии и вызывают помутнение масла. Для их удаления масло обычно охлаждают до 8-12°С и осадок отфильтровывают (способ "вымораживания").
Пигменты, содержащиеся в семенах и плодах масличных растений, придают растительным маслам разл. окраску. Красные и желтые оттенки в цвете растительных масел определяются присутствием в них каротиноидов (красный оттенок-каротин, желтый-ксантофилл), наибольшее их кол-во содержится в кукурузном масле (0,058-0,15%). Зеленый оттенок, характерный для соевого, кукурузного, рапсового, горчичного и других масел, определяется присутствием в них смеси хлорофиллов А и В. В хлопковом масле содержится токсичный пигмент госсипол (0,14-2,5% по массе), наибольшее содержание которого отмечается в масле, подученном из низкосортных и незрелых хлопковых семян. При переработке масла госсипол дает различные темно-окрашенные продукты. Удаляют госсипол из масла с помощью антраниловой кислоты, с которой он образует нерастворимое соединение. При очистке растительных масел с помощью адсорбентов происходит удаление пигментов и осветление масла.
Основную массу белковых веществ, переходящих в растительные масла из семян, составляют альбумины и глобулины. Поскольку наличие белков ухудшает товарный вид масел и увеличивает его потери при очистке и хранении, белковые примеси (вместе с фосфолипидами) удаляют при гидратации масла, а также под действием щелочей или минеральных кислот. Углеводы, моно-, ди- и олигосахариды, декстрины, крахмал, клетчатка и гемицеллюлоза, содержащиеся в растительных маслах в кол-ве 0,02-0,5%, образуют стабильные эмульсии, способствуют потемнению масла при термической обработке, придают маслам неприятный вкус и запах.
Часть неомыляемых веществв, входящих в растительные масла, составляют витамины Е, A, D и К. Витамин Е содержится в растительных маслах в виде a-, b-, g-, и d-токоферолов. Кол-во D-a-токоферола в подсолнечном масле составляет около 0,05%. Высоким содержанием токоферолов характеризуются также масла пшеничных отрубей (100-400 мг в 100 г масла), соевое (74-160 мг в 100 г масла) и кукурузное (87-200 мг) масла; до 100 мг токоферолов в 100 г подсолнечного, хлопкового, рапсового и некоторых других маслах, до 60 мг-в арахисовом, до 30 мг-в оливковом и кокосовом.
Витамин А встречается в растительных маслах в виде провитаминов; содержится преимущественно в облепиховом, абрикосовом, персиковом и других маслах. Витамин D содержится главным образом в соевом и кунжутном маслах, витамин К (К1, К2, К3)-в конопляном, подсолнечном, льняном и сурепном маслах.
В растительных маслах присутствуют также незначительное кол-ва насыщенных и не-насыщенных углеводородов с разветвленной цепью. В частности, в состав подсолнечного, хлопкового и соевого масел входит сквален (0,008-0,012%). Углеводороды, совместно с белками, в значительной степени определяют вкус и запах масла.
В результате длительного хранения на свету, при повышенной температуре или под действием микроорганизмов растительные масла портятся-прогоркают. Неприятный запах и вкус растительным маслам сообщают продукты окисления жирных кислот (альдегиды, кетоны, гидроксикислоты), низкомолекулярные жирные кислоты и их глицериды, продукты распада каротиноидов, стеринов, витаминов, фосфолипидов.
Иногда в растительных маслах могут находиться пестициды, используемые в сельском хозяйстве. Их обычно удаляют из масла вместе с одорирующими веществами в процессе перегонки с паром при 200-250 °С в вакууме.
Жиры, способствующие образованию пены: кокосовый жир и жир пальмовых косточек. Их оптимальный объем в мыле: 10% - 25 %. Кроме них пенообразующее, правда в немного ослабленной форме, действуют пальмовое и оливковое масло. Последнее создает чрезвычайно мелкопористую пену, которая становится тем лучше, чем дольше мыло зреет.
Особенно хорошо увлажняют кожу и ухаживают за ней – рапсовое и подсолнечное масло.
Глицерин – это природный спирт. Он применяется в косметической промышленности уже несколько столетий. В отличие от своих собратьев глицерин не сушит, а наоборот увлажняет кожу. Кроме того, глицерин прекрасно защищает кожу от неблагоприятных воздействий окружающей среды. Он представляет собой густую бесцветную жидкость. Несмотря на то, что это жидкость, глицерин продается на развес. Температура кипения + 290С.
Кокосовое масло – вещество растительного происхождения, добывается путем прессования кокосовой стружки. Кокосовое масло применяется для мыловаренной и кондитерской промышленности. Оно обладает противовоспалительными, увлажняющими, питательными и защитными свойствами. Кокосовое масло подходит для изготовления массажных плиток, мыла, блесков для губ и масок для волос. Температура плавления кокосового масла составляет 22-27 градусов. В комнатной температуре выглядит как белый мягкий маргарин. При контакте с кожей кокосовое масло мгновенно тает.
Касторовое масло – вещество растительного происхождения. Его получают из плодов клещевины, родиной которой является Восточная Африка. Касторовое масло для лечебного и косметологического применения получают с помощью холодного отжима. Касторовое масло прекрасно смягчает и отбеливает кожу, устраняет пигментные пятна. Идеально подходит для возрастной и чувствительной кожи. Касторовое масло прекрасно борется с мимическими морщинами и возвращает коже упругость. Представляет собой вязкую маслянистую жидкость желтого цвета. Сильно увлажняющее жирное масло, оно не высыхает и не образует пленку. Для того чтобы приготовить хорошо смягчающее твердое мыло с сильной пеной используйте касторку в своих рецептах до 20%.
Какао-масло - золотистого цвета и приятного вкуса и запаха (если не деодорированное). Его получают на стадии технологической обработки какао-бобов. Именно вкус и консистенцию какао-масла вы чувствуете, когда шоколад тает во рту.
Оливковое масло
В оливковом масле содержится большое количество ненасыщенных жирных монокислот, минеральных веществ и жирорастворимых витаминов (A, D, К).
Оливковое масло необходимо для того чтобы не нарушать естественный защитный барьер, не пересушивать кожу и вернуть ей данные от природы красоту и сияние. Чем еще полезно оливковое масло? Во-первых в нем содержатся различные соединения которые задерживают рост и размножение микробов, во-вторых оно прекрасно защищает кожу от воспаления, от солнечных ожогов, от шелушения и ороговения, обладает антиоксидантными свойствами благодаря большому содержанию витамина Е.
Миндаль
Масло сладкого миндаля очень многокомпонентно по своему составу: содержит витамины ( А, В1, В2, В6, Е), провитамины, полиненасыщенные жирные кислоты (витамин F), белковые вещества, минеральные вещества (цинк, железо, натрий, магний), глюкозу, лецитин, растительные стеарины, дубильные вещества. За счет такого структурного и органического разнообразия, масло сладкого миндаля регулирует белковое равновесие клеток кожи, помогая становиться ей более ровной, прозрачной, эластичной. Восстанавливает водно-липидный баланс, регенерирует, снимает раздражение. Масло обладает омолаживающим эффектом, разглаживает мелкие морщинки, придает бархатистый оттенок коже и красивый ровный цвет
Кофейные зерна
Самый ценный ингредиент, содержащийся в кофейных зернах – кофеин. Он стимулирует биохимические процессы в клетках, активизирует липолиз - основной механизм расщепления и выведения жиров, обладает выраженным антицеллюлитным эффектом. Зерна кофе богаты витаминами группы В, органическими кислотами, маслами, белками, жирами и углеводами, которые способствуют восстановлению эластичности кожи, препятствуют преждевременному старению, обладают противовоспалительными и солнцезащитными свойствами, оказывают смягчающее и увлажняющее воздействие на кожу. Не обжаренные кофейные зерна проявляют антиоксидантные свойства. Аромат кофе улучшает дыхательную функцию легких, оказывает стимулирующее действие на мозговую деятельность.
Лимон
Основными составляющими лимона являются конечно же вода и лимонная кислота. Но кроме того, в нем еще присутствуют важнейшие для организма витамины. Больше всего в лимоне витамина С, который незаменим для правильного обмена веществ в организме и участвует в питании тканей. Наряду с ним лимон содержит витамины А, В1, В2, и D, а также витамин, характерный исключительно для цитрусовых: цитрин (витамин Р). Лимон обладает антиоксидантным, антицеллюлитным и отбеливающим свойствами. Лимонный сок стягивает поры, тонизирует и оздоровляет кожу, делает жирную, блестящую кожу матовой, более сухой.
Апельсин
В апельсинах содержатся витамины группы В, С, Е, К, Р, каротин, соли железа, кальция, калия, кремния, марганца, магния, меди, фосфора, фтора, хлора, цинка, различные органические кислоты, в том числе и лимонная (около 2%).
По содержанию кальция апельсины превосходят другие цитрусовые фрукты. Как и лимон апельсин обладает антицеллюлитным свойством.
Отруби
В отрубях много клетчатки, а так же витамины группы В, витамины А и Е. Кроме того в отрубях содержатся микроэлементы, необходимые для нормального протекания обменных процессов в организме: калий, кальций, фтор, медь, цинк, магний, хром, селен и другие. Отруби являются основой многих масок для лица. Они успокаивают, умеряют раздражение кожи и смягчают ее. Применяются при нормальной и сухой коже.
Мед
Мед содержит фруктозу и глюкозу, а также ряд минералов (калий, магний, кальций, серу, хлор, натрий, фосфат и железо). Кроме того, мед богат витаминами B1, B2, B6, B3, B5 и C. Концентрация этих полезных веществ в меде зависит от качества нектара и пыльцы. Кроме незначительного количества меди, йода и цинка, мед также содержит некоторые натуральные гормоны. Мед славится своими антибактериальными, антивирусными и противогрибковыми свойствами.
То есть, используя те или иные ингредиенты для приготовления мыла в домашних условиях можно добиться того результата который вы хотите получить ( антицеллюлитного, отбеливающего и т. д.).
Кофе. Мелко размолотый натуральный кофе сделает мыло пятнистым, придаст ему аромат роскоши. Кроме того кофе обладает антиоксидантными свойствами, делает кожу эластичной и предупреждает её старение. Лучше всего использовать натуральный кофе для приготовления скрабов.
Лепестки календулы - обладают ранозаживляющим, противовоспалительным, бактерицидным свойствами (т. е. убивают болезнетворные микроорганизмы), кроме того придают мылу красивый золотистый цвет.
Листья грецкого ореха. Берутся сухие листья грецкого ореха, толкутся в ступке; они придают мылу зеленовато-коричневый цвет.
Листья крапивы добавляют для того чтобы придать мылу красивый зеленый цвет.
Масло сладкого миндаля не имеет запаха, отлично растворяет в себе эфирные масла, не мешает коже свободно дышать и поэтому используется в качестве масла-основы в ароматерапии для приготовления разных композиций для массажных смесей. Отлично увлажняет кожу. Из масла миндаля получается очень приятное мыло с хорошей мягкой пеной, но лучше всего использовать миндальное масло в сочетании с другими маслами, например с оливковым.
Мёд - В мёде содержится около 300 разных полезных веществ. Врачи говорят, что в крови человека содержится 24 микроэлемента, так вот в мёде из них присутствует 22! Мёд способен не только задерживать рост болезнетворных микроорганизмов, но и совсем убивать их. Он помогает сделать кожу мягкой и эластичной. Если у вас сухая кожа используйте для приготовления мыла 1 ч. ложку мёда на рецепт.
Оливковое масло - это растительное масло, которое делают из плодов оливы европейской. Оливковое масло традиционно используется в мыловарении. Больше года хранить его нельзя, потому что постепенно теряются его полезные свойства. Если у вас чувствительная кожа используйте это масло. Мыло получится приятным и хорошо смягчит вашу кожу.
Подсолнечное масло — очень лёгкое масло, его получают из семян подсолнечника. Если у вас сухая тонкая кожа, то берите подсолнечное масло, но не более 15%, потому что если взять больше, мыло получится не очень качественным: оно тогда плохо мылится и пузырьки больших размеров получаются.
Ростки пшеницы содержат большое количество витамина Е и А, поэтому скраб с ростками пшеницы очень полезен, он прекрасно успокаивает кожу, отшелушивает омертвевшие клетки и омолаживает кожу.
Сухое молоко - это порошок белого цвета, его получают из сгущённого молока. Если добавить сухое молоко в ваш рецепт, то вы получите прекрасное мыло, которое отлично смягчит и успокоит вашу кожу.
Шоколад придает мылу роскошный тёмный цвет, но если взять больше 10% в рецепте, то мыльная пена получится неприятного грязно-коричневого цвета. Шоколад надо выбирать с большим содержанием какао (80%) и с небольшим количеством сахара.
Цитрусовая кожура. Берутся любые шкурочки: из-под лимона, апельсина, грейпфрута...— не важно, трутся на тёрке и добавляются в мыло. Сначала кладем кожурки на дно формочки, а только потом заливаем мыло, когда смесь высохнет и затвердеет, переворачиваем мыло, тогда получаются красивые желто-оранжевые крапинки. Если положить много кожуры, мыло будет плохо пениться.
Натуральные красители для мыла
Красный цвет мыла получится при добавлении:
- Свекла (от приглушенно-розового до красного)
- Кошенили порошок (насыщенный красный)
- Марроканская красная глина (красно-коричневый цвет)
- Розовая глина (красно-коричневый цвет)
Персиковый:
- Кайеннский перец (порошок перца чили, применять с осторожностью - очень жгучее вещество!)
- Паприка (от легкого персикового до лососевого – может раздражать кожу. Пропорция: 2.5-5 мл на 500 гр мыла.)
Оранжевый:
- Аннато семена (первоначально растворяется в масле – желто-оранжевый)
- Морковь (от желтого до оранжевого)
- Тыква (насыщенный оранжевый цвет)
- Облепиховое масло
- куркума
Желтый:
- Цветки календулы
- Цветы ромашки (бежево-желтый)
- Карри порошок (от золотого до янтарного, применять осторожно - может раздражать кожу)
- Куркума (от персикового и оранжевого, примерно 5 мл на 1.2 кг мыла)
- Шафран
Зеленый:
- Люцерна (легкий зеленый)
- Огурец (ярко-зеленый цвет)
- Хна порошок (от оливкового до насыщенного серо-зеленого и коричневого цвета, 15 мл на 2.3 кг мыла)
- Водоросли
- Спирулина (от зеленого до изумрудного)
- Шалфей
- Шпинат (светло-зеленый)
- Петрушка или укроп сухие (светло-зеленый цвет)
Голубой:
- Эфирное масло ромашки (от голубого до синего)
Синий:
- Индиго корень (насыщенный синий – может окрашивать кожу)
Фиолетовый:
- Алкана красильная (первоначально растворяется в масле – от насыщенного фиолетового до приглушенно синего)
Коричневый:
- Корица (от бежевого до коричневого – может быть раздражителем кожи)
- Гвоздика измельченная
- Какао порошок
- Зерна кофе измельченные, кофейная гуща (от коричневого до черного цвета)
- Корень окопника (легкий, молочно-коричневый цвет)
- Ягоды бузины (первоначально добавляют в раствор щелочи – светло-коричневый)
- Шиповник измельченный (от светло-коричневого до насыщенного коричневого)
- Кусочки шоколада (коричневый)
- Каркадэ (красные цветы гибискуса - фиолетовый, лиловый)
- Жженый сахар
Белый:
- Каолин
- Диоксид титана (яркий белый)
Бежевый:
- Молоко (от светло-бежевого до коричневого цвета, в зависимости от жирности и содержания сахара)
Серый:
- Семена мака (от серо-синих до светло-черных вкраплений)
- Измельченная пемза
- Уголь (в белой основе даёт серовато-лиловый оттенок и черные точки)
ЗАКЛЮЧЕНИЕ.
Мировое производство хозяйственных мыл постепенно сокращается в связи с увеличением выпуска синтетических моющих средств и растущим дефицитом жирового сырья. Однако с распространением разнообразных синтетических мылоподобных веществ мыла не потеряли своего значения важнейшего средства личной гигиены. Они по-прежнему широко применяются в быту и во многих отраслях промышленности (особенно в текстильной). Мыло наряду с другими типами поверхностно-активных веществ используются как смачиватели, эмульгаторы, стабилизаторы коллоидно-дисперсных систем. Мыло применяют в составе смазочно-охлаждающих жидкостей для металлообрабатывающих станков; при обогащении полезных ископаемых флотацией. Их используют в химической технологии: при синтезе полимеров эмульсионным способом, в производстве лакокрасочной продукции и др. «Металлические» Мыла как загустители входят в состав пластичных смазок, как сиккативы (ускорители «высыхания») — в состав масляных лаков, олиф и др.
ПРИЛОЖЕНИЕ
Способы приготовления
Оборудование:
Для того, чтобы изготовить мыло понадобиться некоторое количество необходимого оборудования, которое должно использоваться только для приготовления мыла:
1. Старые газеты или клеенка, чтобы застелить место работы
2. Бумажным скотчем можно обклеить места стыков, но это не обязательно.
3. Кухонные весы, электронные +- 1 грамм для отмеривания ингредиентов.
4. Стеклянная емкость, выдерживающая довольно большие температуры, например из лабораторного стекла.
5. Кастрюля из металла или стекла для замешивания мыльной массы.
6. Кастрюля большего размера для водяной бани.
7. Два лабораторных термометра.
8. Блендер, правда мыло можно смешать и ложкой, но блендером все же быстрее.
9. Перчатки, например хозяйственные резиновые.
10. Ступка и пестик или кофемолка для смешивания и размалывания ингредиентов для мыла.
11. Маска или марлевая повязка на лицо, чтобы не вдыхать пары щелочного раствора.
12. Емкости и плошки для трав, отмеривания масел, и прочих потребностей.
13. Уксус, который нейтрализует щелочь, пригодится на всякий случай и в дальнейшем при уборке помещения.
14. Пара ложек или удобных шпателей для перемешивания и укладки мыльной массы в формы.
15. Текстильные полотенца.
16. Формы для мыла.
В общем-то, это все приспособления. Список может показаться очень обширным, но на самом деле, многие из вещей, от которых давно пора было избавиться на кухне, пригодятся для дальнейшего использования в мыловарении. Что ж теперь можно перейти к тому, из чего же состоит мыло.
Мыло - это натриевые соли жирных кислот растительных и животных жиров. В древние времена мыло изготавливалось с использованием жира животных и золы. Теперь же, когда есть способ получить щелочь химическим путем процесс изготовления мыла стал доступен в домашних условиях. Итак, для приготовления мыла понадобятся следующие ингредиенты:
1. Щелочь - едкий натр, каустическая сода, гидроксид натрия, все это одно и то же едкое вещество. Приобрести ее можно в Москве в магазине Лабтех, или в интернете. Щелочь должна быть марки ЧДА. Ее необходимо хранить вдалеке от влаги, в закупоренном контейнере, потому что щелочь впитывает влагу из воздуха и теряет свои свойства. А так же это ОЧЕНЬ ОПАСНОЕ вещество, поэтому стоит изолировать детей, мужей и домашних животных от даже самых мелких частичек этого вещества, а после приготовления мыла нужно сделать влажную уборку с уксусной водой.
2. Растительные и животные жиры. Разнообразные масла оливковое, подсолнечное, ореховые масла, растительные воски, пчелиный воск (до 15% для твердости) и прочие Животные жиры, говяжий, свиной, гусиный, куриный жир, норочий и барсучий жиры. Некоторые специалисты считают, что животные жиры способствуют аномальному развитию клеток организма.
3. Вода, питьевая, дистиллированная, отвары, молоко, пиво, вино, коньяк, соки - все это может быть использовано в приготовлении мыла.
Для приготовления простейшего куска мыла трех вышеуказанных составляющих будет вполне достаточно. Но если, мы хотим украсить мыло необычным цветом, понадобятся следующие ингредиенты:
4. Натуральные красители - глины, хна, травы, кофе, какао, индиго и прочие.
Так же можно добавить мылу свойства скраба, в чем тоже помогут и травы и глины и соль мелкого помола и прочие натуральные ингредиенты.
Еще мы часто любим, когда мыло пахнет, например:
5. Любимые эфирные масла помогут ароматизировать ваше мыло.
Техника безопасности
Для начала нужно подготовить щелочной раствор. В охлажденную воду, отмеренную на весах, аккуратно и медленно всыпать необходимое количество щелочи и аккуратно размешать. ВНИМАНИЕ! Не вдыхать пары, и открыть окно! Щелочь в воду, а не наоборот! Если готовить мыло на молоке, его необходимо предварительно заморозить, потому что раствор на молоке нагревается очень сильно, чего не стоит допускать.
Когда раствор щелочи готов, нужно оставить его остывать. Лучше делать все манипуляции с щелочью в раковине, чтобы в случае пролития раствора не бегать с уксусом по всей кухне, а просто смыть его водой, заодно и трубы почистить.
Далее необходимо отмерить нужное количество масел и поставить их на водяную баню. Сначала растопить твердые масла, если они есть в рецепте. Согласно рецепту, необходимо подогреть оливковое масло и касторку, а 10% масла авокадо или виноградные косточки оставить для пережиривания, используем его позже.
Когда масла нагреются, а раствор остынет до температуры в диапазоне 35-55 градусов, можно снять масла с бани и аккуратно влить щелочной раствор в масла. Температура масел и раствора должны быть приблизительно одинаковой. Когда данная манипуляция произведена, можно переходить к замешиванию мыльной массы.
Ложкой или блендером смешать массу до появления следа или трассы. Интенсивное замешивание производится для запуска реакции омыления, которая содержит несколько стадий, и первая из них "трасса" или "стадия следа".
Стадия следа - это консистенция плотного пудинга. Довести массу до стадии следа занимает от 5 до 25 минут, зависит от состава масел в рецепте и температуры замешивания.
На данном этапе необходимо решить, каким способом готовить мыло: холодным или горячим.
Если выбрать холодный способ, то уже на стадии следа нужно вмешать в мыльную массу масло, оставленное в качестве пережиривания, травы, эфирные масла и красители, уложить массу в формы и изолировать в теплом месте, например в подогретой заранее духовке, чтобы мыло уже в формах прошло следующую стадию "стадию геля", которая занимает несколько часов. Проще оставить мыло на ночь, а через сутки или двое его можно будет достать из форм, оно уже затвердеет, и если нужно порезать и оставить вызревать в течение 4-6 недель в проветриваемом помещении, завернутым в пергаментную или вощеную бумагу, оливковое мыло вызревает на пару недель подольше. Важное замечание: мыло на молоке не стоит изолировать, оно само по себе войдет в гель, это повлияет на цвет мыла, чтобы сделать белоснежное молочное мыло надо избежать стадии геля, например, поставив формы с мылом в как можно более прохладное место. Вот и все стадии холодного способа изготовления мыла. Смысл холодного процесса, его плюсы или минусы.
Достоинства:
1.Мыло, изготовленное холодным способом, лучше сформовано, соответственно легче укладывается в формы и лучше выглядит в готовом виде.
2.В него можно добавить активы, которые не терпят высоких температур, например витамины, экстракты растений, отвары.
Недостатки:
1.Нужно долго ждать пока оно, наконец, созреет, потому что реакция омыления при таком способе происходит медленно для этого оно и вызревает, чтобы реакция прошла до конца.
2.Так же мы не может точно знать какие из масел останутся неомыленными, и какой именно компонент будет ухаживать за нашей кожей.
Если же выбрать горячий способ приготовления мыла, то на стадии следа нужно взять массу и поставить обратно на водяную баню. Где при температуре около 60-65 градусов можно будет наблюдать реакцию омыления масел до конца. Весь процесс занимает где-то 2-3 часа. Массу нужно время от времени помешивать, чтобы не было комочков.
Здесь показана мыльная масса с замешанными в нее травами.
Сначала мыльная масса начнет затвердевать как на следующей фотографии, может даже подниматься, это в порядке вещей. Просто перемешайте ее тщательно.
Через некоторое время мыльная масса войдет в "стадию геля", станет жидкой и как бы створожиться.
А после прохождения данной стадии наступит "восковая стадия" масса снова станет густой, но все еще створоженной и не будет налипать на ложку или к пальцам.
Вскоре масса начнет набирать нужную консистенцию, плотнеть, станет густой, блестящей и будто с мраморным или перламутровым рисунком. После того, как вы увидите такую консистенцию можно произвести пробу на язык, если она не щиплет, а ощущается просто мыльный вкус, значит ваше мыло почти готово. Необходимо быстренько подготовить добавки, эфиры и масло для пережиривания, и вмешать в массу, в кратчайшие сроки, масса при снятии с бани начнет быстро густеть. И, наконец, выложить в формы. Укладывать стоит поплотнее, чтобы мыло было ровненькое, хорошей формы и без пузырьков воздуха внутри. На следующий день мыло можно достать из формы и порезать на куски.
О плюсах и минусах процесса.
Достоинства:
1.Мылом можно пользоваться уже на следующий день, потому что реакция омыления прошла полностью и щелочи в мыле не осталось.
2.Масла добавленные в мыло обладают своими свойствами в полной мере, а так же мы точно знаем, какое масло будет ухаживать за нашей кожей.
3. Оно приятнее и на ощупь и в использовании.
Недостатки:
1.Горячее мыло хуже формуется, отчего иногда не получается нужной формы, но можно снять с мыла фаску и получить замечательные аккуратные кусочки мыла.
Литература:
[1] Википедия http://ru.wikipedia.org/wiki/%C3%E8%E4%F0%EE%EA%F1%E8%E4_%ED%E0%F2%F0%E8%FF
[2] Кукушкин Юрий. Химия вокруг нас. http://n-t.ru/ri/kk/hm10.htm
[3]Процесс изготовления традиционного алеппского мыла http://www.arabsoap.ru/about/z_story/process.html
4.http://www.soapmaker.ru
http://www.xumuk.ru/encyklopedia/2335.html
5 http://www.magicaltouch.ru/index.php?aux_page=aux41.php ИСТОРИЯ МЫЛОВАРЕНИЯ
6 http://izbushka.mybb.ru/viewtopic.php?id=108
7 Паронян В.Х. Растительные масла http://www.ximuk.ru/encyklopedia/2/3827.html
8 Тютюнников Б.Н., Химия жиров, М., 1974; Беззубов Л. П., Химия жиров, 3 изд., М., 1975; Щербаков В. Г., Биохимия и товароведение масличного сырья, 3 изд., М., 1979; Технология жиров и жирозаменителей, М., 1982; Технология переработки жиров, М., 1985; Паронян В.Х., Новокшо-нов Ю. И., Моделирование и оптимизация процессов рафинации жиров, М., 1985
9 http://lovekasoap.ru/article_info.php?articles_id=4
СОДЕРЖАНИЕ
I ВСТУПЛЕНИЕ
II ОСНОВНАЯ ЧАСТЬ
Искусство косметики
Классификация продуктов косметической химии
3. Химические средства гигиены и косметики
А. Средства ухода за зубами
Б. Дезодоранты и озоновый «щит» планеты
В. Косметические средства
4. Ядовитая десятка
5. Мыла
А. История мыловарения
Б. Процесс приготовления мыла на Востоке
В. Химические процессы при мыловарении
Г.Ингредиенты для мыла
Д.Компоненты мыла
III ЗАКЛЮЧЕНИЕ
ПРИЛОЖЕНИЕ
ЛИТЕРАТУРА












