| 1 слайд |
ЧТО ТАКОЕ ЭЛЕКТРОН? |
|
2 слайд
|
• é – это частица!
m0 = 0,9109534*10 – 27 г
Z = 1,6021892*10 – 19 Кл |
|
3 слайд
|
é – волна!
Электрон обладает большой СКОРОСТЬЮ и ЭНЕРГИЕЙ!
За долю секунды электрон способен «обежать» целую область пространства, называемую
Электронное облако
или атомная орбиталь |
|
4 слайд
|
Местоположение электронов в пространстве в данный момент времени определить невозможно.
Они ведут себя примерно так, как описал Льюис Кэрролл Чеширского Кота в сказке «Алиса в стране чудес»:
Вроде бы он здесь, но в тоже время его нет, осталась лишь улыбка… |
|
5 слайд
|
Виды электронных облаков: s-, p-, d-, f- |
|
6 слайд
|
Все электроны атома образуют его ЭЛЕКТРОННУЮ ОБОЛОЧКУ |
|
7 слайд
|
ЭЛЕКТРОННАЯ ОБОЛОЧКА ДЕЛИТСЯ НА УРОВНИ.
ИЗВЕСТНО 7 ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ,
РАСПОЛОЖЕННЫХ НА РАЗНЫХ РАССТОЯНИЯХ ОТ ЯДРА
|
|
8 слайд
ПРОБЛЕМНЫЙ
ВОПРОС
|
(пример атома кремния)
Атом какого химического элемента изображен на рисунке? |
|
9 слайд
|
УРОВНИ состоят из ПОДУРОВНЕЙ, на которых располагаются атомные орбитали s-, p-, d- и f-типа |
|
10 слайд
ПРОБЛЕМНЫЙ
ВОПРОС
|
1 уровень – s- подуровень,
2 уровень – s- и p- подуровни,
3 уровень – s-, p- и d- подуровни,
4 уровень – s-, p-, d- и f- подуровни.
Чему равно число подуровней на уровне?
|
|
11 слайд
|
s-подуровень 1 АО
р-подуровень 3 АО
d-подуровень 5 АО
f-подуровень 7 АО
ИТАК, имеем:
1s2s2p3s3p3d4s4p4d4f5s5p5d5f…
6s6p6d6f…7s7p7d7f…
|
|
12 слайд
|
ПРАВИЛА ЗАПОЛНЕНИЯ ЭЛЕКТРОНАМИ АО, ПОДУРОВНЕЙ, УРОВНЕЙ
1) На одной АО могут находиться только ДВА электрона, которые вращаются вокруг своей оси в противоположных направлениях (условно: по часовой стрелке и против часовой стрелке) – электроны с противоположными спинами.
|
|
13 слайд
|
2) В пределах подуровня атомные орбитали заполняются одиночными электронами с параллельными спинами, и когда все орбитали данного подуровня будут заняты, происходит спаривание последних |
|
14 слайд
|
3) Электроны стремятся занять энергетически выгодное положение в электронной оболочке, руководствуясь правилом наименьшей энергии. Расположим АО в порядке возрастания значений их энергии, которая определяется суммой: (№ УРОВНЯ + число, которое соответствует подуровню):
s (0), p (2), d (3), f (4) |
|
15 слайд
|
 1 2 3 3 4 5 4 5 6 7 5 6 7 8 1 2 3 3 4 5 4 5 6 7 5 6 7 8
1s 2s2p3s3p3d4s4p4d4f5s5p5d5f…
 6 7 8 9 7 8 9 10 6 7 8 9 7 8 9 10
6s6p6d6f… 7s7p7d7f…
РЯД НАИМЕНЬШЕЙ ЭНЕРГИИ:
1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p7s5f6d7p…
|
|
16 слайд
|
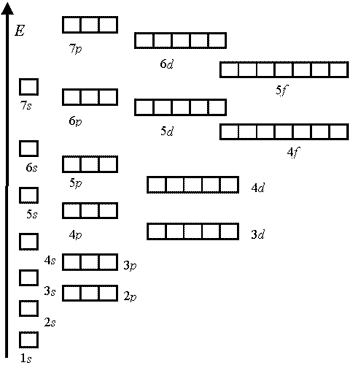
ЭНЕРГЕТИЧЕСКАЯ ДИАГРАММА РАСПОЛОЖЕНИЯ АО В ЭЛЕКТРОННОЙ ОБОЛОЧКЕ

|
|
17 слайд
|
СХЕМА СТРОЕНИЯ АТОМА
Показывает распределение электронов по уровням |
|
18 слайд
|
ЭЛЕКТРОННАЯ ФОРМУЛА (КОНФИГУРАЦИЯ) АТОМА
1s1
Показывает распределение электронов по подуровням |
|
19 слайд
|
ЭЛЕКТРОННО-ГРАФИЧЕСКАЯ ФОРМУЛА АТОМА
Показывает распределение электронов по АО |





 1 2 3 3 4 5 4 5 6 7 5 6 7 8
1 2 3 3 4 5 4 5 6 7 5 6 7 8