Урок № 66
класс 8
дата 12.05.2025
Тема урока: Обобщение и систематизация знаний по теме «Классы неорганических соединений»
Тип урока: урок-игра
Цель урока: в занимательной форме обобщить и закрепить знания о химических свойствах основных классов неорганических соединений и их взаимопревращениях.
Задачи урока:
Образовательная: обобщить и углубить знания обучающихся о классах неорганических веществ, особенностях каждого класса, способах распознавания веществ.
Развивающая: развивать аналитическое мышление, способность анализировать, сравнивать, синтезировать материал, формулировать выводы.
Воспитательная: воспитывать интерес к химии, ответственность за качество своей учебной деятельности, самостоятельность и инициативу.
Предметные цели:
Обобщить и систематизировать знания обучающихся о классах неорганических соединений (кислоты, основания, соли, оксиды);
Закрепить умения определять принадлежность веществ к различным классам соединений, устанавливать взаимосвязи между ними, составлять уравнения химических реакций;
Развить практические навыки распознавания признаков принадлежности веществ к определённым классам, установления формул веществ и написания уравнений реакций.
Метапредметные цели:
Способствовать развитию критического мышления и способности анализировать, сравнивать, классифицировать химические объекты;
Создавать условия для формирования коммуникативных компетенций через активное участие в коллективной игре, обсуждениях и работе в группах;
Совершенствовать регулятивные учебные действия: целеполагание, самоконтроль, самооценка результатов собственной деятельности.
Личностные цели:
Воспитание ответственности и инициативности, желания совершенствоваться и развивать собственные знания и умения;
Формирование научного мировоззрения и понимания важности химии в жизни человека и общества;
Поддержание положительного отношения к учёбе, развитие познавательной активности и самостоятельности.
Оборудование и реактивы. Игровое поле, таблицы растворимости, карточки с заданиями, пробирки с растворами гидроксида натрия, соляной кислоты, хлорида калия, растворы индикаторов.
Ход урока
Организационный этап.
Приветствие обучающихся, подготовка к уроку.
2. Актуализация знаний.
Учитель предлагает учащимся быстро назвать известные классы неорганических веществ и перечислить характерные признаки каждого класса (кислоты, основания, соли, оксиды). Учитель фиксирует правильные ответы на интерактивной доске или листе бумаги.
Предварительно ребятам раздаются фишки с разными цветами: Класс делится на группы, каждая группа получает карточку с названием одного класса неорганических веществ. Нужно записать три главных признака, характеризующих этот класс. Время ограничено — две минуты.
Пример карточек:
Группа №1: Кислоты
Группа №2: Основания
Группа №3: Оксиды
Группа №4: Соли
3. Постановка формируемых результатов и задач урока. Мотивация учебной деятельности.
Представьте себе мир, где каждая молекула — это маленький кирпичик большого здания науки, а химия — та волшебница, которая строит этот дом из атомов и молекул. Вы стоите перед огромной стройплощадкой неорганического мира, полной удивительных открытий и невероятных возможностей.
Изучая классы неорганических соединений, вы открываете дверь в царство загадочных превращений и скрытых связей. Каждый урок — это приключение, наполненное увлекательными опытами, неожиданными реакциями и глубокими размышлениями о природе вещей. Каждая формула, каждый закон становится частью вашей личной коллекции научных сокровищ, которыми можно гордиться!
4. Обобщение и систематизация знаний.
Объяснение правил игры.
Основа игры – классическое детское поле из 9 клеток, в каждой из которых написано название конкурса.
Учитель объясняет правила игры
Начинает представитель команды « Крестики », выбирая на поле конкурс. Следующий конкурс выбирает команда « Нолики ».
Выбор конкурсов командами осуществляется поочередно, независимо от итогов сыгранного конкурса.
В каждом конкурсе ответы должны давать разные игроки команды.
Задания, имеющие варианты, представители команд выполняют у доски. Команды одновременно с игроками получают задания конкурса, чтобы оценить правильность ответа их представителя.
Победившая команда ставит свой знак на игровом поле, на клетке сыгранного конкурса. Если обе команды правильно выполнили задание конкурса, победителя определяют путем дополнительного задания.
Выигрывает команда, которой удалось поставить на поле три своих знака в один ряд в любом направлении или пять знаков в любом порядке.
Игра проводится в форме путешествия по станциям. Каждая станция представляет собой серию небольших заданий, связанных с данным классом веществ.
Станция 1. Разгадайте ребусы:
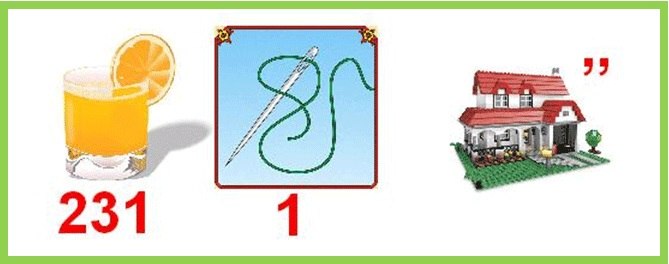 оксиды
оксиды соль
соль
 кислоты
кислоты
 основание
основание
Учащиеся дают определение понятиям (оксиды, кислоты, основания, соли).
Станция 2. Разгадайте сказку (на мультимедийном экране).
Жила была на берегу моря добрая принцесса, звали её Оксигеница. Ее имя означало «рожденная кислородом», и она олицетворяла собой чистоту воздуха и ясность ума. Окружающие любили Оксигеницу, потому что она заботилась обо всех живых существах, снабжая их чистым воздухом.
Но однажды пришел коварный чародей по имени Феруларт, властелин тьмы и разрушений. Используя свое черное искусство, он превратил сердце Оксигеницы в черный камень — феррумоксид. Теперь без сердца, Оксигеница стала слабеть, деревья пожелтели, птицы перестали петь, а небо покрылось мрачностью.
Однако один смелый герой, кузнец по имени Карбонилус, вознамерился спасти Оксигеницу. Дух предков открыл ему секрет: чтобы разрушить проклятие Феруларта, нужен особый сплав. Но чтобы создать его, нужны были три ингредиента: чистая вода, самый твердый минерал и святая искорка света.
Отправившись в путешествие, Карбонилус встретил первую героиню — прекрасную фею Гидрагению, повелительницу чистых вод. Именно её прозрачная жидкость — вода — была первой составляющей сплава.
Затем он нашел второе средство помощи в подземельях, где жил могучий великан Базилиянт, обладатель священного минерала. Базилиянт вручил Карбонилусу крупинку белого кристалла — сильнейший защитник от тёмных чар, называемый гидроксидом натрия.
Последним элементом стал пламенный страж крепости Огня, отважный рыцарь Аксифлюс, хранящий животворящую искорку света. Аксифлюс передал герою кусочек яркого желтого кристалла — серной кислоты (H2SO4)
Объединив вместе компоненты, Карбонилус получил новый состав — мощный защитный элемент, похожий на белый блестящий песок. Этот новый союзник оказался сульфатом натрия (Na2SO4), силой которого удалось победить Феруларта и восстановить равновесие.
Освобожденная Оксигеница вдохнула глубокий глоток свежего воздуха, солнце засияло ярко, реки вновь заблестели чистотой, цветы расцвели пышнее прежнего.
История эта напоминает нам простую истину: справедливость восстанавливается, когда объединяют усилия самые различные сущности — вода, основа и кислота создают новую гармонию, проявляя свою истинную мощь именно тогда, когда действуют сообща.
Имена героев и предметы символизируют следующие химические вещества:
Оксигеница — кислород.
Феруларт — символ железа.
Феррумоксид — оксид железа.
Гидрагения — вода.
Базилиянт — гидроксид натри.
Аксифлюс — серная кислота.
Новый союзник — сульфат натрия.
Реакции, иллюстрирующие восстановление:
Образование основания и воды:
NaOH+H2SO4→Na2SO4+H2O
Освобождение железа от оксида: Fe2O3+3 C→2 Fe+3 CO
Физкультминутка гимнастика для глаз
Начало формы
Станция 3. “Химический детектив”
Задание: Узнайте соль по подсказкам и напишите её формулу. Подсказки: «Это растворимая соль натрия, применяется в пищевой промышленности». Правильный ответ: NaCl — поваренная соль.
Станция 4. Получи хлорид натрия используя данные вещества: хлорид кальция, натрий, соляная кислота, гидроксид натрия, сульфат натрия, хлорид алюминия, хлорид калия
Станция 5. Конкурс « Рассыпанные уравнения»
Из цифр и химических знаков, находящихся в конверте, сложить два уравнения реакций:
3Ba, 2, O, Al 2, P, H, PO4, +, =, O3, +, 3, H2, O4, S, Ba, Al, 3, 2, S, =, O4, 2, +, 3, H2, O, O4, 3, 2, 3, H, +, O, (…), (…).
Ответ
3BaO + 2H3PO4 = Ba3(PO4)2 + 3H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
6. Закрепление материала.
Каждая команда подготовила задание сопернику и объясняет его публично всей группе.
Затем учитель подводит итоги выполненного задания каждой командой, отмечая успехи и исправляя возможные ошибки.
7. Рефлексия.
Учащимся предлагается устно высказаться о том, чему научились на уроке, какие трудности возникли, и что понравилось больше всего.
Например:
Что нового узнали?
Какие задания были самыми интересными/самыми сложными?
Как бы хотели продолжить изучение данной темы?
8. Домашнее задание.
Подготовить мини-проект или презентацию на тему «Применение солей в повседневной жизни», выбрать один конкретный пример и рассказать о нём классу.
Итоги урока.
Учитель благодарит всех участников за активное участие, подводит общие итоги урока, оценивает работу команд и объявляет победителей игры.
мышление и создать условия для успешного усвоения материала.
Начало формы






 оксиды
оксиды соль
соль кислоты
кислоты основание
основание









