9класс
Контрольная работа № 3 по теме «Металлы».
Вариант 1.
Часть А.
При выполнении заданий выберите номер одного правильного ответа.
1.Наиболее сильные восстановительные свойства проявляет
а) K б) Mg в) Li г) Na
2.Ряд, в котором элементы расположены в порядке возрастания их атомного радиуса:
а) B→Be→Li в) K→Na→Li
б) Mg→Ca→Be г) Na→Mg→Al
3.Электронная конфигурация внешнего электронного слоя….2s22p1 соответствует атому
а) алюминия б) бора в) скандия г) калия
4.Реактивом на катион Al3+ является
а) Сl- б) Na+ в) OH- г) CO32-
5.Наиболее активно с водой при комнатной температуре будут взаимодействовать оба металла из пары
а) Na и Cu б) Li и Na в) K и Mg г) Cu и Hg
6.С растворами кислот будут взаимодействовать оба металла
а) Li и Ag б) Na и Hg в) K и Mg г) Cu и Hg
7. При взаимодействии железа с водой при нагревании образуется
а) соль и вода в) оксид металла и водород
б) основание и водород г) реакция не протекает
8. С водой с образованием основания и водорода будет взаимодействовать
а) Са б) Сu в) Zn г) Ag
9. Амфотерный оксид образуется при взаимодействии кислорода и
а) натрия б) меди в) магния г) цинка
10. Для вытеснения меди из раствора ее соли можно использовать
а) натрий б) серебро в) кальций г) железо
Часть В.
В1.Установите соответствие между правой и левой частями уравнений
| 1) Сu+HNO3конц.→ | А) FeCl3+H2↑ |
| 2) Fe+HСl→ | Б) FeCl2+H2↑ |
| 3) Fe+Cl2→ | B) FeCl2 |
| 4) Cu+HNO3разб.→ | Г) FeCl3 |
|
| Д) Cu(NO3)2 +NO↑+H2O Е) Cu(NO3)2 +NO2↑+H2O |
В2. Напишите уравнения реакций, соответствующих превращениям, укажите типы реакций и условия их протекания:
А) Fe → FeCl3 → Fe(OH)3 → Fe2O3 → Fe2(SO4)3
Б)Al→Al2O3→AlCl3→Al(OH)3→Al2(SO4)3→Al(NO3)3
↓
NaAlO2
В3. Рассчитайте массу оксида магния, который образуется при обжиге карбоната магния массой 200 г, содержащего 10 % примесей.
9класс
Контрольная работа №3 по теме «Металлы».
Вариант 2.
Часть А.
При выполнении заданий выберите номер одного правильного ответа.
1. Наиболее сильные восстановительные свойства проявляет
а) К б) Al в) Na г) Zn
2.Ряд, в котором элементы расположены в порядке уменьшения их атомного радиуса:
а) Al→Mg→Na в) Li→Na→K
б) Ca→Ba→Be г) Ca→ Mg→Be
3.Электронная конфигурация внешнего электронного слоя….3s23p1 соответствует атому
а) алюминия б) бора в) скандия г) калия
4.Реактивом на ион Ca2+ является ион
а) Сl- б) Na+ в) OH- г) CO32-
5. Наиболее активно с водой при комнатной температуре будут взаимодействовать оба металла из пары
а) K и Cu б) Na и K в) Na и Zn г) Cu и Hg
6.С растворами кислот будут взаимодействовать оба металла
а) K и Cu б) Na и Hg в) K и Zn г) Cu и Hg
7. При взаимодействии цинка с водой при нагревании образуется
а) соль и вода в) оксид металла и водород
б) основание и водород г) реакция не протекает
8. С водой с образованием оксида металла и водорода при нагревании будет взаимодействовать
а) Na б) Fe в) Cu г) Ag
9. Амфотерный оксид образуется при взаимодействии кислорода и
а) натрия б) алюминия в) магния г) бария
10. Для вытеснения меди из раствора её соли можно использовать
а) калий б) литий в) цинк г) натрий
Часть В.
В1. Установите соответствие между правой и левой частями уравнений
| 1) Сu +H2SO4разб.→ | А) Al(OH)3+H2↑ |
| 2) Сu +H2SO4конц.→ | Б) не взаимодействует |
| 3)Al+H2O→ | B) СuSO 4 + SO2↑ + H2O |
| 4)Al2O3+HCl→ | Г) AlCl3+H2O |
|
| Д) AlCl3+H2↑ Е) СuSO4 + H 2S↑ + H2O |
В2. Напишите уравнения реакций, соответствующих превращениям, укажите типы реакций и условия их протекания:
Fe → FeCl2 → Fe(OH)2 → FeO → FeSO4
Na→Na2O2 →Na2O→NaOH→Na3PO4→NaNO3.

Na2CO3
В3. Вычислите, какой объём углекислого газа (н.у.) выделится при обжиге 500 г карбоната магния с массовой долей примесей 8 %?
9класс.
Контрольная работа №3 по теме: «Металлы».
Вариант 3
Часть А.
При выполнении заданий выберите номер одного правильного ответа.
1.Наиболее ярко металлические свойства проявляет
1)K 2)Be 3)Al 4)Na
2.Ряд, в котором элементы расположены в порядке возрастания их атомного радиуса:
1) Na →Mg→ Al 3)K→Na→Li
2)Ca→Ba→Be 4)K→Ca→Al
3.Электронная конфигурация внешнего электронного слоя….3s2 соответствует атому
1)алюминия 2)бора 3)кальция 4)калия
4.Реактивом на ион  является ион
является ион
1) 2)
2) 3)
3)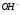 4)
4)
5.Наиболее активно с водой при комнатной температуре будут взаимодействовать оба металла из пары
1)Na и Cu 2) Na и K 3)K и Zn 4)Cu и Hg
6.С растворами кислот будут взаимодействовать оба металла
1)Na и Cu 2) K и Hg 3) Na и Fe 4)Cu и Hg
7.При взаимодействии цинка с водой при нагревании образуется
1)Соль и вода 3)оксид металла и водород
2)основание и водород 4)реакция не протекает
8.С водой с образованием основания и водорода будет взаимодействовать
1) K 2)Zn 3)Cu 4)Нg
9.Амфотерный оксид образуется при взаимодействии кислорода и
1)натрия 3)алюминия
2)магния 4)бария
10.Для вытеснения меди из раствора её соли можно использовать
1)натрий 3)железо
2)калий 4) серебро
Часть В.
В1.Установите соответствие между правой и левой частями уравнений
| 1) NaCl+AgNO3→ | А)Fe(OH)3↓+3NaCl |
| 2)CuSO4+BaCl2→ | Б)Cu↓+FeCl2 |
| 3)Fe+CuCl2→ | B)Fe(OH)2+2NaCl |
| 4)2NaOH+FeCl2→ | Г)NaNO3+AgCl |
|
| Д)CuCl2+BaSO4↓ |
В2.Напишите уравнения реакций, соответствующих превращениям, укажите типы реакций и условия их протекания:
А)Zn → ZnSO4 → Zn(OH)2→ ZnO→Zn
Б)Fe→ FeCl2→Fe(OH)2→ Fe(OH)3→ Fe2O3→ Fe2(SO4)3
↓
FeCl3
В3. Определите объём оксида углерода (ΙV), выделившегося при обжиге 120 г известняка, содержащего 10 % примесей.
9класс.
Контрольная работа №3 по теме: «Металлы».
Вариант 4
Часть А.
При выполнении заданий выберите номер одного правильного ответа.
1.Наиболее ярко металлические свойства проявляет
1)Ca 2)Be 3)Mg 4)K
2.Ряд, в котором элементы расположены в порядке уменьшения их атомного радиуса:
1)Al→Mg→Na 3)K→Na→Li
2) Li → Na → K 4)Ca→ K→Al
3.Электронная конфигурация внешнего электронного слоя….2s22p1 соответствует атому
1)алюминия 2)бора 3)скандия 4)калия
4.Реактивом на ион  является ион
является ион
1) 2)
2) 3)
3)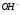 4)
4)
5.Наиболее активно с водой при комнатной температуре будут взаимодействовать оба металла из пары
1)K и Cu 2) Li и K 3)Na и Zn 4)Cu и Hg
6.С растворами кислот будут взаимодействовать оба металла
1)K и Cu 2) Na и Hg 3)K и Mn 4)Cu и Hg
7.При взаимодействии кальция с водой образуется
1)Соль и вода 3)оксид металла и водород
2)основание и водород 4)реакция не протекает
8.С водой с образованием оксида металла и водорода при нагревании будет взаимодействовать
1)Na 2)Zn 3)Cu 4)Ag
9.Амфотерный оксид образуется при взаимодействии кислорода и
1)натрия 3)алюминия
2)магния 4)бария
10.Для вытеснения меди из раствора её соли можно использовать
1)калий 3)никель
2)золото 4) натрий
Часть В.
В1.Установите соответствие между правой и левой частями уравнений
| 1) CaCl2+2NaOH→ | А)FeCl2+H2↑ |
| 2)2K+2H2O→ | Б) FeCl3+H2↑ |
| 3)3NaOH+FeCl3→ | B)Ca(OH)2↓+2NaCl |
| 4)2HCl+Fe→ | Г)3NaCl+Fe(OH)3↓ |
|
| Д)2KOH+H2↑ |
В2.Напишите уравнения реакций, соответствующих превращениям, укажите типы реакций и условия их протекания:
А)Li → Li2O →LiOH→ Li2SO4→BaSO4
Б)Al→Al2O3→AlCl3→Al(OH)3→ Al2O3→ Al2(SO4)3
↓
NaAlO2
В3. Рассчитайте объём водорода (при н.у.), если он выделился при взаимодействии 240 г магния, содержащего 12 % примесей, с соляной кислотой.







 является ион
является ион  2)
2) 3)
3)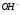 4)
4)
 является ион
является ион 

















