ВАРИАНТ 4.
1. Какой процесс называют окислением, восстановлением?
Окисление -процесс отдачи электронов, с увеличением степени окисления.
Восстановление - процесс присоединение электронов атомом вещества при этом его степень окисления понижается
2. Какие органические соединения обладают основными свойствам
ОснОвными свойствами обладают амины и аминокислоты, в которых амино-групп больше, чем карбоксильных.
3. Как определяется степень гидролиза?
Степень гидролиза— это соотношение количества подвергающейся гидролизу соли nгидр и общего количества растворенной соли nобщ. Обычно, ее обозначают через hгидр (или α ):
hгидр = (nидр/nобщ)·100 %
Величина hгидр увеличивается с уменьшением силы образующих соль кислоты или основания.
4. Ионная сила раствора определяется формулой:
I = ½ ∑ Сi · zi2 , где
Сi – концентрация ионов, присутствующих растворе,
zi – заряд ионов, присутствующих растворе.
Рассчитайте ионную силу раствора: 0,2М Н2SО4.
Решение.
Молярность 0.2 М означает концентрацию 0.2 моль/л.
Кислота в растворе диссоциирует на 2H+ и (SO4)2- ионы.
Концентрация ионов H+ = 2 * 0.2 = 0.4 моль/л
Концентрация ионов (SO4)2- = 1 * 0.2 = 0.2 моль/л
I = 1/2 * (0.4 * 1 + 0.2 * 22) = 1/2 * (0.4 + 0.8) = 0.6
5. Какую величину называют произведением растворимости?
Произведение концентраций ионов малорастворимого электролита в его насыщенном растворе называют произведением растворимости и обозначают знаком ПР.
ПР(AgCl) = [Ag+][Cl-]
ПР(PbI2) = [Pb2+][I-]2
ПР(Ag2S) = [Ag+]2[S2-]
ПР(Ba3(AsO4)2) = [Ba2+]3[AsO43-]2.
6. Как можно обнаружить при совместном присутствии Fe2+, Mg2+, Mn2+, Bi3+.
а)Гексацианоферрат (III) калия K3[Fe(CN)6] с катионом Fe2+ образует синий осадок «турнбулевой сини»:
3FeSO4 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2↓ + 2K2SO4,
Б)Гидрофосфат натрия Na2HPO4 образует с катионами Mg2+ в присутствии NH4OH и соли аммония при рН ≈ 9 белый кристаллический осадок MgNH4PO4· 6H2O:
MgCl2 + Na2HPO4 + NH4OH = MgNH4PO4↓ + 2NaCl + H2O.
Осадок магний-аммоний фосфата растворяется в минеральных кислотах и CH3COOH:
MgNH4PO4 + 3HCl = MgCl2 + NH4Cl + H3PO4.
При постепенном прибавлении раствора аммиака к кислому раствору соли магния происходит медленное выделение крупных кристаллов MgNH4PO4. При избытке NH4OH может образоваться аморфный осадок Mg(OH)2. Осадок MgNH4PO4 склонен к образованию устойчивых пересыщенных растворов, поэтому при его получении необходимо энергичное перемешивание реакционной смеси.
В)Сильные окислители окисляют в кислой среде ион Mn2+ до MnO4- малинового цвета.
2Mn(NO3)2 + 5NaBiO3 + 16HNO3 = 2HMnO4 + 5Bi(NO3)3 + 5NaNO3 + 7Н2O.
Диоксид свинца PbO2 окисляет Mn2+ в азотнокислой среде при нагревании:
2Mn(NO3)2 + 5PbO2 + 6HNO3 = 2HMnO4 + 5Pb(NO3)2 + 2Н2О.
При наличии в растворе ионов Cl- в больших концентрациях и при высокой концентрации ионов Mn2+ образовавшиеся ионы MnO4- восстанавливаются до темно-бурого осадка MnO(OH)2.
Г)Гидролиз – одна из характерных реакций катиона Bi3+. При разбавлении растворов солей висмута Bi(NO3)3 и особенно BiCl3 – выпадает белый осадок оксосоли (хлорид оксовисмута):
BiCl3 + H2O = BiOCl↓ + 2HCl.
7. Назовите катионы, относящиеся к III аналитической группы.
Катионы третьей группы – осаждаются серной кислотой и ее солями, которые являются групповыми реагентами. При взаимодействии с сульфатом катионы дают нерастворимые в воде сульфаты бария и стронция и плохо растворимый сульфат кальция. Они образуют также нерастворимые в воде фосфаты, сульфиты, карбонаты. Нитраты, бромиды, хлориды, гидрокарбонаты хорошо растворимы в воде.
Гидроксиды кальция, бария, стронция обладают слабощелочными свойствами и в воде растворимы плохо. Катионы бесцветны, окраска их солей зависит от аниона. Соединения кальция, бария и стронция широко применяют как реактивы, минеральные краски, строительные материалы.
8. Напишите уравнения качественных реакций на аммоний-ион и укажите специфические реакции.
NH4Cl + NaOH = NaCl + H2O + NH3
Если к отверстию нагреваемой пробирки поднести увлажнённую фенолфталеиновую бумажку, она приобретёт малиновую окраску.
9. Что происходит с осадком гидроксида марганца (II)на воздухе?
Гидроксид марганца (II) легко окисляется на воздухе до бурого оксогидроксида марганца, который далее разлагается на оксид марганца (IV):
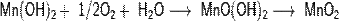
10. Как отличить качественными реакциями Fe2+и Fe3+.
1. Качественная реакция на ион железа (II) – реакция с красной кровяной солью.
Добавим красную кровяную соль ‑ гексацианоферрат калия K3[Fe(CN)6]. (Для определения железа (III) используют желтую кровяную соль K4[Fe(CN)6]). В присутствии ионов железа (II) образуется темно-синий осадок. Это - турнбуллева синь ‑ комплексная соль железа KFe[Fe(CN)6]).
Появление турнбуллевой сини доказывает присутствие в растворе ионов железа (II).
2 К3[Fe(CN)6 ] +3 Fe SO4 = KFe[Fe(CN)6])↓ + 3K2SO4
Турнбуллева синь очень похожа по свойствам на берлинскую лазурь и тоже служила красителем. Названа по имени одного из основателей шотландской фирмы по производству красителей «Артур и Турнбуль».
2. Качественная реакция на ион железа (II) – реакция со щелочью.
Реакция со щелочью – еще один способ обнаружения ионов железа (II). Гидроксид железа (II) Fe(OH)2 - серо-зеленого цвета, гидроксид железа (III) Fe(OH)3 - бурый. Добавим щелочь (NaOH) в колбу с солью железа - образуется серо-зеленый осадок. Значит, в растворе присутствуют ионы железа (II). Образовавшийся осадок – гидроксид железа (II) Fe(OH)2.
Fe SO4 +2 NaOH = Fe(OH)2 ↓ + Na2 SO4
По каким причинам в ходе анализа могут возникать ошибки взвешивания и отмеривания
ри выполнении количественного определения любым химическим или физико-химическим методом могут быть допущены три группы ошибок: грубые (промахи), систематические (определенные) и случайные (неопределенные).
Грубые ошибки являются результатом просчета наблюдателя при выполнении какой-либо из операций определения или неправильно выполненных расчетов. Результаты с грубыми ошибками отбрасываются как недоброкачественные.
Систематические ошибки отражают правильность результатов анализа. Они искажают результаты измерений обычно в одну сторону (положительную или отрицательную) на некоторое постоянное значение. Причиной систематических ошибок в анализе могут быть, например, гигроскопичность препарата при отвешивании его навески; несовершенство измерительных и физико-химических приборов; опытность аналитика и т.д. Систематические ошибки можно частично устранить внесением поправок, калибровкой прибора и т.д. Однако всегда необходимо добиваться того, чтобы систематическая ошибка была соизмерима с ошибкой прибора и не превышала случайной ошибки.
Случайные ошибки отражают воспроизводимость результатов анализа. Они вызываются неконтролируемыми переменными. Среднее арифметическое случайных ошибок стремится к нулю при постановке большого числа опытов в одних и тех же условиях. Поэтому для расчетов необходимо использовать не результаты единичных измерений, а среднее из нескольких параллельных определений.
12. Какие реакции используют для гравиметрического анализа Fe3+?
13. Определите титр 0.11 н. раствора НCl.
Т= m вещества / V раствора, г/мл
Т=(mэ*СН)/1000=(36,5*0,11)/1000= 0.004015 г/мл
14. Рассчитайте нормальность раствора NaOH. если навеска титруемой щавелевой кислоты 0,6112 г (Э=63.04) и на титрование израсходовано 52 см3 раствора NaOH.
Решение
Рассчитаем количество эквивалентов щавелевой кислоты H2C2O4 6
m/Э= 0.6112/63.04 = 0.0096954 моль
Рассчитаем нормальность раствора щелочи
Cн. р-ра NaOH = 0.0096954/0.052 =0.18645 моль/л.
15. Вычислить рН буферной смеси, содержащей 0,5 М уксусной кислоты и 0,01 М ацетата калия.
Решение.
pH=pKa+lg([CH3COONa]/[CH3COOH])
pH=-lg(1,75*10-5)+ lg(0,01/0,5)=3,06
16. Каков механизм действия металлохромных индикаторов?
Принцип действия металлохромных индикаторов:
1 До начала титрования в анализируемый раствор вводят буферную систему и небольшое количество индикатора. В результате реакции между индикатором и определяемым катионом образуется окрашенный комплекс.
М + Ind = MInd М – катион определяемого металла, Ind – ион индикатора (заряды отпущены), MInd – окрашенный комплекс катиона с индикатором. Раствор окрашен в цвет комплекса MInd. Например, при определении жесткости воды до начала титрования раствор имеет винно-красную (пурпурную) окраску – цвет комплекса MInd.
2 В процессе титрования к исследуемому раствору постепенно добавляют ЭДТА, протекает реакция: М + Y = MY М – катион определяемого металла, Y – дианион ЭДТА (заряды отпущены), MY – бесцветный комплекс катиона с ЭДТА. С комплексом MInd изменений не происходит, окраска раствора сохраняется.
3. В конце титрования, когда в растворе почти не остается свободных ионов М, происходит реакция MInd + Y = MY + Ind MInd – окрашенный комплекс катиона с индикатором, Y – дианион ЭДТА (заряды отпущены), MY – бесцветный комплекс катиона с титрантом ЭДТА, Ind – свободный ион индикатора. Комплекс металл-индикатор MInd менее прочный, чем комплекс металл-ЭДТА MY:βMY βMInd Комплекс MInd разрушается, от одной лишней капли индикатора раствор приобретает окраску свободного индикатора Ind.
17. Рассчитайте навеску для -определения гравиметрическим методом СаС12, осадитель раствор (NH4)2 С2О4 (для расчетов используйте формулу аналитического фактора).
Гравиметрический фактор (F) – отношение молекулярной массы определяемого вещества к молярной массе гравиметрической формы с коэффициентами a и b, на которые нужно умножить это отношение, чтобы молекулярные массы были эквивалентны друг другу.
F = а М(опр.в-ва) / bМ(г.ф.).СаС12-определяемое вещество=111г/моль, х=1
(NH4)2 С2О4 -гравиметрическая форма=124г/моль,х=1
СаС12+(NH4)2 С2О4 = Са С2О4+2(NH4) С1
для кристаллических осадков:
g = х ×М (опр.в-ва)×0,5/ у× М(г.ф.)=(1*111*0,5)/1*124=0,45г
18 На чем основан метод турбидиметрии?
Турбидиметрическим методом анализа (турбидиметрией) называют метод, основанный на измерении интенсивности потока света, прошедшего через раствор, содержащий взвешенные частицы. Интенсивность уменьшается вследствие поглощения и рассеяния светового потока.
При турбидиметрических измерениях величина, называемая мутностью, соответствует оптической плотности.
Для турбидиметрических измерений можно использовать любой фотометр или спектрофотометр. Если растворитель и рассеивающие частицы бесцветны, максимальная чувствительность достигается при использовании излучения голубой или ближней ультрафиолетовой области. Для окрашенных систем оптимальную длину волны необходимо подбирать экспериментально.
При этих методах анализа получаемые осадки, вернее, взвеси, должны иметь ничтожную растворимость и быть стойкими во времени, а получение правильных результатов при анализе суспензий зависит от методики получения суспензий и воспроизводимости их оптических свойств. На размеры частиц и оптические свойства суспензий влияют концентрация ионов, образующих осадок, отношение между концентрациями смешиваемых растворов, порядок смешивания растворов, скорость смешивания, время, требуемое для получения максимальной мутности, стабильность дисперсии, присутствие посторонних электролитов, присутствие неэлектролитов, температура, наличие защитных коллоидов.
19. Какие реакции лежат, в основе йодометрического титрования?
Иодометрией называют титриметрнческнй метод в основе которого лежат реакции:
I2 + 2ē →2I-
2I- -2ē → I2
Методов иодометрии можно определять как окислители (они окисляют I- до I°), так и восстановители (они восстанавливают йод до I-).
Исходным веществом для установки титра Na2S2O3 служит дихромат калия К2Сг2О7.
Большинство окислителей нельзя титровать непосредственно тиосульфатом натрия, так как невозможно фиксировать точку эквивалентности. Поэтому для определения окислителей методом иодометрии применяют косвенный метод — титрование заместителя. Вначале проводят реакцию между окислителем и иодидом калия в кислой среде. Для подкисления применяют серную кислоту или хлороводородную. Реакция протекает по уравнению:
К2Сг2О7 + 6KI + 7H2SO4 = Cr2(SO4)3 + 7Н2О + 4K2SO4 + 3I2
Сг2О72-+ 14Н+ + 6е →2Сг3+- + 7Н2О
2I- -2е- → I2
Выделившийся свободный иод титруют раствором тиосульфата натрия:
Na2S2O3 + I2 = 2NaI + Na2S4O6
2S2O32- -2е- → S4O62-
I2 + 2ē →2I-
20. К раствору нитрита свинца массой 250г прилили избыток раствора сульфида калия. Образовался осадок массой 47,8г.Определите массовую долю нитрата свинца в исходном растворе?
Решение.
Pb(No2)2+K2S=PbS+2KNO2
n(PbS)=47.8/239=0.2
n(PbS)=n(Pb(No2)2)=0.2моль
m(Pb(No2)2)=0.2x331=66.2
w(Pb(No2)2)=47.8/66.2=0.72=72%