Рассмотрены Утверждены
на педагогическом Совете Директор школы_____________
Протокол № 4 от 26.03.2018 г Л. П. Терехова
Приказ №____ от _______
Контрольно-измерительные материалы
по предмету химия
для проведения промежуточной аттестации
обучающихся 8 класса за 2017-2018 учебный год
Пояснительная записка
Диагностическая работа проводится в конце учебного года с целью определения достижения учащимися 8-го класса уровня обязательной
подготовки по химии, а также сформированности некоторых учебных умений -правильного восприятия учебной задачи, умения работать самостоятельно, контролировать свои действия, находить несколько правильных ответов.
Документы, определяющие содержание и параметры диагностической
работы
Содержание и основные характеристики проверочных материалов определяются на основе следующих документов:
– Федеральный государственный образовательный стандарт основного общего образования (приказ Министерства образования и науки Российской Федерации от 17.12.2010 № 1897).
–Примерные программы основного общего образования. М.: Просвещение.
Структура диагностической работы
Работа состоит из трех частей, количество заданий 14. Часть А содержит 9 тестовых вопросов с выбором одного правильного ответа. В части В даны два задания: на соответствие и множественный выбор. Часть С содержит три задания, на которые учащиеся должны дать развернутый ответ.
Распределение заданий по содержанию
| Раздел программы | Количество заданий | Максимальный первичный балл |
| Строение атома | А1 | 1 |
| Периодическая система | А2 | 1 |
| Химическая связь | А3 | 1 |
| Степень окисления | А4 | 1 |
| Строение веществ | А5 | 1 |
| Типы химических реакций | А6 | 1 |
| Техника безопасности | А7 | 1 |
| Вычисление количества вещества | А8 | 1 |
| Вычисление массовой доли химического элемента в веществе | А9 | 1 |
| Классы веществ | В1 | 2 |
| Изменение свойств в Периодической системе | В2 | 2 |
| Характеристика химического элемента | С1 | 7 |
| Уравнивание реакций, определение типа реакции, умение называть сложные вещества | С2 | 6 |
| Решение задач по уравнению реакции | С3 | 3 |
| Итого | 14 | 29 |
Условия проведения: работа выполняется обучающимися в классе в течение 40 минут. Обучающиеся могут пользоваться калькулятором, Периодической системой химических элементов Д.И. Менделеева, таблицей растворимости.
Критерии оценивания выполненных работ.
| № задания | Оценочный балл |
| А 1-9 | 1 балл – вариант ответа выбран верно. |
| В1 | 2 балла - правильно определены соответствия 1 балл допущена 1 ошибка. |
| В2 | 2 балла - правильно выбраны утверждения 1 балл - допущена 1 ошибка. |
| С 1 | 7 баллов: 1 балл за каждый правильный ответ по плану. |
| С 2 | 1 балл – расстановка коэффициентов; 1 балл – определение типа химической реакции; 1 балл – название сложных веществ. Максимальное количество баллов 6. |
| С 3 | 1 балл – составлено уравнение реакции 1 балл – вычислена масса или количество исходного вещества 1 балл – найдено количество вещества по уравнению реакции и вычислена масса или объем по условию задачи |
| Итого | 29 балла |
Выставление итоговых оценок
Итоговая оценка за работу выставляется в соответствии со следующей шкалой перевода с сайта http://5-ege.ru/shkala-perevoda-ballov-gia-v-ocenki/
| Суммарный балл за работу | % выполнения | Отметка по 5-балльной шкале |
| 0 – 8 | 0-29 | «2» |
| 9-15 | 30-54 | «3» |
| 16-23 | 55-79 | «4» |
| 24-29 | 80-100 | «5» |
КОНТРОЛЬНАЯ РАБОТА ПО ХИМИИ 8 КЛАСС
БЛАНК ОТВЕТОВ
Фамилия, имя____________________________________________
Класс _________ Дата ___________ Вариант ________________
ЧАСТЬ А
| А1 | А2 | А3 | А4 | А5 | А6 | А7 | А8 | А9 |
|
|
|
|
|
|
|
|
|
|
ЧАСТЬ В
В 1
В 2
ЧАСТЬ С
Контрольная работа по химии 8 класс
Вариант 1
При выполнении контрольной работы все ответы заносятся в отдельный бланк ответов.
Часть А.
К каждому заданию части А дано несколько ответов, из которых только один верный. Выберите правильный ответ и занесите его в бланк ответов.
А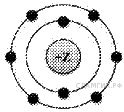 1. На приведённом рисунке изображена модель атома химического элемента
1. На приведённом рисунке изображена модель атома химического элемента
1) 2-го периода VIIIA группы
2) 2-го периода VIA группы
3) 3-го периода VIA группы
4) 3-го периода VIIIA группы
А 2. В каком ряду химических элементов усиливаются металлические свойства соответствующих им простых веществ?
1) калий → натрий → литий 3) углерод → кремний → германий
2) сурьма → мышьяк → фосфор 4) алюминий → кремний → углерод
А 3. Ковалентная неполярная связь образуется между атомом хлора и атомом
1) углерода 2) калия 3) водорода 4) хлора
А 4. Степень окисления кислорода в гидроксиде натрия равна:
- 2 2) + 1 3) + 2 4) 0
А5. В каком ряду расположены сложные вещества?
1) S, Al, N2 3) HNO3, CaO, PH3
2) CO2, Fe, H2O 4) Si, P4, Fe2O3
А 6. Какое уравнение соответствует реакции обмена?
1)CuCl2+Fe=Cu+FeCl2 3)2KOH+H2SO4=K2SO4+2H2O
2)2Al+Fe2O3=2Fe+Al2O3 4)2Na+O2=Na2O2
А 7. Верны ли суждения о правилах применения и опасности для здоровья препаратов бытовой химии?
А. Стиральные порошки нельзя использовать для мытья посуды.
Б. Работать с хлорсодержащими дезинфицирующими средствами следует при плотно закрытой двери в помещении.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
А 8. Газообразный водород объемом 224 л при н.у. составляет
1) 5 моль 2) 10 моль 3) 20 моль 4) 2 моль
А 9. На какой диаграмме распределение массовых долей элементов соответствует количественному составу сульфата железа(II)?

Часть В
В1. К каждой формуле соединения из первого столбца подберите соответствующий класс вещества из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы в бланке ответов.
| Формула соединения | Название вещества |
| А. ZnO Б. Al (NO3)3 В.H2SiO3 Г Mn(OH)2 | 1) Основание 2) Оксид 3) Кислота 4) Соль |
В 2. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры под которыми они указаны
В группе (главной подгруппе) при увеличении порядкового номера элемента возрастает
1) высшая степень окисления
2) радиус атома
3) валентность элемента в водородном соединении
4) число заполненных электронами энергетических уровней
5) электроотрицательность элемента
Часть С
Ответом части С служит развернутый ответ на вопрос. Запишите сначала номер задания (С1, С2, С3), а затем его полное решение. Ответы записывайте чётко и разборчиво бланк ответов.
С 1: Дайте характеристику химическому элементу фосфору по плану:
Положение в периодической системе:
1)порядковый номер
2)период
3)группа; подгруппа
Строение атома:
4)заряд ядра
5)число нейтронов, протонов, электронов в атоме
6)число электронов на внешнем электронном слое
7)принадлежность к металлам или неметаллам
С2: Расставьте коэффициенты в уравнениях, укажите тип реакции, назовите сложные вещества:
А) K+O2=K2O
Б) NaОН+AlCl3=Al(OH)3+NaCl
C3: Решите задачу: Вычислите объём газа (н. у.), который выделится при действии избытка сульфида железа(II) на 490 г 10%-ного раствора серной кислоты.
Контрольная работа по химии 8 класс
Вариант 2
При выполнении контрольной работы все ответы заносятся в отдельный бланк ответов.
Часть А.
К каждому заданию части А дано несколько ответов, из которых только один верный. Выберите правильный ответ и занесите его в бланк ответов.
А1. На приведенном рисунке изображена модель атома
1 ) магния
) магния
2) кальция
3) лития
4) калия
А 2. В каком ряду химических элементов усиливаются металлические свойства соответствующих им простых веществ?
1) кислород → фтор → неон 3) селен → сера → кислород
2) кремний → сера → хлор 4) алюминий → магний → натрий
А 3. Какой вид химической связи в оксиде хлора(VII)?
1) ковалентная полярная 3) ковалентная неполярная
2) ионная 4) металлическая
А 4. Степень окисления азота в азотной кислоте равна:
1) + 6 2) + 5 3) - 5 4) + 1
А 5. В каком ряду расположены простые вещества?
1) S, Al, N2 3) HNO3, CaO, PH3
2) CO2, Fe, H2O 4) Si, P4, Fe2O3
А 6. Какое уравнение соответствует реакции разложения?
1)Na2S+Br2=2NaBr+S 3) 2AgI=2Ag+I2
2)2HCl+Ba(OH)2=BaCl2+2H2O 4) Ca(OH)2+CO2=CaCO3+H2O
А 7. Верны ли суждения о назначении лабораторной посуды и оборудования?
А. Для измерения объёма жидкости используют мерный цилиндр.
Б. Ступка с пестиком предназначены для измельчения твёрдых веществ.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
А 8. В воде массой 360 г содержится количество воды:
10 моль 2) 20 моль 3) 4 моль 4) 2 моль
А 9 На какой диаграмме распределение массовых долей элементов соответствует количественному составу нитрата калия?

Часть В
В1. К каждой формуле соединения из первого столбца подберите соответствующий класс вещества из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы в бланке ответов
| Формула соединения | Название вещества |
| А. CaO Б. Ca (NO3)2 В.H2SO3 Г. NaOH | 1) Соль 2) Оксид 3) Кислота 4) Основание |
В 2. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры под которыми они указаны
В ряду химических элементов Be → B → C происходит увеличение (усиление)
1) числа протонов в ядрах атомов
2) числа электронных слоев в атомах
3) радиуса атомов
4) неметаллических свойств
5) основного характера свойств высших оксидов
Часть С
Ответом части С служит развернутый ответ на вопрос. Запишите сначала номер задания (С1, С2, С3), а затем его полное решение. Ответы записывайте чётко и разборчиво бланк ответов.
С 1: Дайте характеристику химическому элементу сере по плану:
Положение в периодической системе:
1)порядковый номер
2)период
3)группа; подгруппа
Строение атома:
4)заряд ядра
5)число нейтронов, протонов, электронов в атоме
6)число электронов на внешнем электронном слое
7)принадлежность к металлам или неметаллам
С2: Расставьте коэффициенты в уравнениях, укажите тип реакции, назовите сложные вещества:
А) Al+O2=Al2O3
Б) Ca(ОН)2+HNO3= Ca(NO3)2+H2O
C3: Решите задачу: Раствор соляной кислоты массой 116, 8 г и массовой долей 10% добавили к избытку сульфида магния. Вычислите объём (н. у.) выделившегося газа.
Контрольная работа по химии 8 класс
Вариант 3
При выполнении контрольной работы все ответы заносятся в отдельный бланк ответов.
Часть А.
К каждому заданию части А дано несколько ответов, из которых только один верный. Выберите правильный ответ и занесите его в бланк ответов.
А 1. На приведённом рисунке изображена модель атома
1. На приведённом рисунке изображена модель атома
1) хлора
2) азота
3) магния
4) фтора
А 2. Неметаллические свойства простых веществ усиливаются в ряду
1) фосфор → кремний → алюминий 3) селен → сера → кислород
2) фтор → хлор → бром 4) азот → фосфор → мышьяк
А 3. Группа формул веществ с ковалентным типом связи:
1) H2S, P4, CO2 3) H2, Na, CuO
2) HCl, NaCl, H2O 4) CaO, SO2, CH4
А 4. Степень окисления углерода в молекуле углекислого газа:
1) + 2 2) + 4 3) – 4 4) + 6
А 5. Формула сложного вещества
1) Na 2) HCl 3) O2 4) I2
А 6. Какое уравнение соответствует реакции замещения?
1)AlCl3+3KOH=3KCl+Al(OH)3 3)2Al+3CuSO4=3Cu+Al2(SO4)3
2)4Al+3O2=2Al2O3 4)2Al(OH)3=Al2O3+H2O
А 7. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории и с препаратами бытовой химии?
А. В лаборатории наличие кислоты в растворе определяют на вкус
Б. При работе с препаратами бытовой химии, содержащими щелочь, необходимо использовать резиновые перчатки.
1) верно только А 2) верно только Б
3) верны оба суждения 4) оба суждения неверны
А 8. Оксид кальция массой 560 г составляет:
10 моль 2) 20 моль 3) 4 моль 4) 2 моль
А 9. На какой диаграмме распределение массовых долей элементов соответствует количественному составу карбоната лития?

Часть В
В1. К каждой формуле соединения из первого столбца подберите соответствующий класс вещества из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы в бланке ответов
| Формула вещества | Класс соединения |
| А) BaO Б) H3PO4 В) Ca(OH)2 Г) Ba(NO3)2 | 1) Соль 2) Оксид 3) Кислота 4) Основание
|
В 2. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры под которыми они указаны
Общим для натрия и алюминия является
Наличие 12 протонов в ядрах их атомов
Находятся в третьей группе
Образование простых веществ металлов
Не существуют в природе в виде двухатомных молекул
Образование ими высших оксидов с общей формулой Э2О
Часть С
Ответом части С служит развернутый ответ на вопрос. Запишите сначала номер задания (С1, С2, С3), а затем его полное решение. Ответы записывайте чётко и разборчиво бланк ответов.
С 1: Дайте характеристику химическому элементу литию по плану:
Положение в периодической системе:
1)порядковый номер
2)период
3)группа; подгруппа
Строение атома:
4)заряд ядра
5)число нейтронов, протонов, электронов в атоме
6)число электронов на внешнем электронном слое
7)принадлежность к металлам или неметаллам
С2: Расставьте коэффициенты в уравнениях, укажите тип реакции, назовите сложные вещества:
А) Al+S=Al2S3
Б) Ba(ОН)2+H2SO4= BaSO4+H2O
C3: Решите задачу: К раствору сульфата алюминия массой 68, 4 г и массовой долей 8% прилили избыток раствора хлорида бария. Вычислите массу образовавшегося осадка.
Контрольная работа по химии 8 класс
Вариант 4
При выполнении контрольной работы все ответы заносятся в бланк ответов.
Часть А.
К каждому заданию части А дано несколько ответов, из которых только один верный. Выберите правильный ответ и занесите его в бланк ответов.
А 1. На рисунке изображена модель атома. Какому химическому элементу она соответствует?
1. На рисунке изображена модель атома. Какому химическому элементу она соответствует?
1) алюминию
2) бору
3) азоту
4) фосфору
А
 2. Металлические свойства в ряду Na Mg Al
2. Металлические свойства в ряду Na Mg Al
Увеличиваются 3) не изменяются
Уменьшаются 4) сначала увеличиваются, затем уменьшаются
А3. Какой вид химической связи в оксиде бария?
1) ковалентная неполярная 3) ковалентная полярная
2) металлическая 4) ионная
А4. Степени окисления атома азота в соединениях NH3 и NO соответственно равны
1) -3 и +3 2) -3 и +2 3) -1 и +1 4) +5 и +2
А 5. Только элементы неметаллы расположены в ряду:
P, Cu, K 3) H, S, Hg
K, Fe, C 4) Si, H, O
А6. Какое уравнение соответствует реакции соединения?
1) 2KOH+H2SO4=K2SO4+2H2O 3)2Al+3CuSO4=3Cu+Al2(SO4)3
2)4Al+3O2=2Al2O3 4) 2AgI=2Ag+I2
А7. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории и хранения веществ в быту?
А. При попадании раствора кислоты на кожу, её следует промыть водой и обработать раствором питьевой соды.
Б. Легковоспламеняющиеся жидкости, например ацетон, разрешается хранить только в холодильнике.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
А8. Газообразный кислород объемом 224 л при н.у. составляет
1) 5 моль 2) 20 моль 3) 10 моль 4) 2 моль
А9. На какой диаграмме распределение массовых долей элементов соответствует количественному составу карбоната кальция?

Часть В
В1. К каждой формуле соединения из первого столбца подберите соответствующий класс вещества из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы в бланке ответов.
| Формула вещества | Класс соединения |
| А) MgO Б) Н2SO4 В) КOH Г) ВaCO3 | 1) Соль 2) Оксид 3) Основание 4) Кислота |
В 2. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры под которыми они указаны
В ряду химических элементов Al → Na → Mg происходит уменьшение (ослабление)
1) числа электронов на внешнем энергетическом уровне
2) числа электронных слоев в атомах
3) металлических свойств
4) степени окисления в высших оксидах
5) основного характера свойств высших гидроксидов
Часть С
Ответом части С служит развернутый ответ на вопрос. Запишите сначала номер задания (С1, С2, С3), а затем его полное решение. Ответы записывайте чётко и разборчиво бланк ответов.
С 1: Дайте характеристику химическому элементу натрию по плану:
Положение в периодической системе:
1)порядковый номер
2)период
3)группа; подгруппа
Строение атома:
4)заряд ядра
5)число нейтронов, протонов, электронов в атоме
6)число электронов на внешнем электронном слое
7)принадлежность к металлам или неметаллам
С2: Расставьте коэффициенты в уравнениях, укажите тип реакции, назовите сложные вещества:
А) Ca+O2=CaO
Б) КОН+FeCl2=Fe(OH)2+KCl
C3: Решите задачу: К раствору карбоната калия массой 110, 4 г и массовой долей 5% прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.






 1. На приведённом рисунке изображена модель атома химического элемента
1. На приведённом рисунке изображена модель атома химического элемента
 ) магния
) магния
 1. На приведённом рисунке изображена модель атома
1. На приведённом рисунке изображена модель атома
 1. На рисунке изображена модель атома. Какому химическому элементу она соответствует?
1. На рисунке изображена модель атома. Какому химическому элементу она соответствует?
 2. Металлические свойства в ряду Na Mg Al
2. Металлические свойства в ряду Na Mg Al










