Просмотр содержимого документа
«Коррозия металлов»

Коррозия металлов
Учитель: Дегтярёва Марина Вениаминовна
МБОУ”Первомайская средняя общеобразовательная школа”
Первомайского района Тамбовской области

Гипотеза
- Если железный гвоздь поместить в разные среды, то скорость коррозии будет различна.

Цель
- Изучить коррозию металлов

Задачи:
- Изучить виды коррозийных разрушений
- Определить от чего зависит скорость коррозии
- Узнать способы защиты от коррозии

ХОД ИССЛЕДОВАНИЯ
Общие сведения:
- Коррозия металлов –разрушение металлов в следствии химического или электрохимического воздействия их с внешней средой(коррозионной).
- Причина коррозии- термоденамическая неустойчивость системы ,состоящей из металла и компонентов окружающей (коррозионной) среды.

Ход исследования:
Классификация коррозионных процессов:
- По виду коррозионных разрушений на поверхности или в объёме металла
- По механизму реакций взаимодействия металлов со средой
- По характеру дополнительных воздействий,которым подвергается металл одновременно с действием коррозионной среды
- По типу коррозионной среды

ХОД ИССЛЕДОВАНИЯ :
Виды коррозионных разрушений:
- По характеру коррозионного разрушения
1. Общая
2. Сплошная
а. равномерная
б. не равномерная
в. избирательная
3. Местная
а. коррозия язвами в.межкристалитная
б.межкристами г. транскристалитная
- По условиям протекания процесса
1. Атмосферная 6..коррозия внешним током
2. Жидкостная 7.блуждающими токами
3. Подземная 8.. контактная коррозия
4.Гоновая 9. микробиологическая
5..Структурная 10. под напряжением
1. химическая
2. электрохимическая

ХОД ИССЛЕДОВАНИЯ :
Химическая коррозия
Коррозия является химической,если после
разрыва металлической связи атомы металла непосредственно соединяются химической связью с теми атомами или группами атомов, которые входят в состав окислителей, отнимающих валентные электроны
2 Fe +3Cl₂= 2FeCl₃

ХОД ИССЛЕДОВАНИЯ :
Электрохимическая коррозия
Коррозия является электрохимической, если при выходе из металлической решетки образующийся катион вступает в связь не с окислителем, а с другим компонентом коррозионной среды.

ХОД ИССЛЕДОВАНИЯ :
Электрохимические процессы
Анодный - переход сольватируемых катионов металла в раствор.
Катодный - связывание окислителем освобождающихся электронов.

ХОД ИССЛЕДОВАНИЯ:
Катодный процесс
1.Разряд водородных ионов
2Н+2е=Н₂(водородная деполяризация)
2.Востановление растворенного кислорода
О₂+4Н+4е=2Н₂О(кислородная деполяризация)или
О₂+2Н₂О+4е=4ОНˉ
 0,010,05 Пониженно-стойкие 0,010,05 2 0,050,1 0,10,9 малостойкие 4 0,91 3 нестойкие 910 6 5 7 15 10 9 8 10 " width="640"
0,010,05 Пониженно-стойкие 0,010,05 2 0,050,1 0,10,9 малостойкие 4 0,91 3 нестойкие 910 6 5 7 15 10 9 8 10 " width="640"
ХОД ИССЛЕДОВАНИЯ:
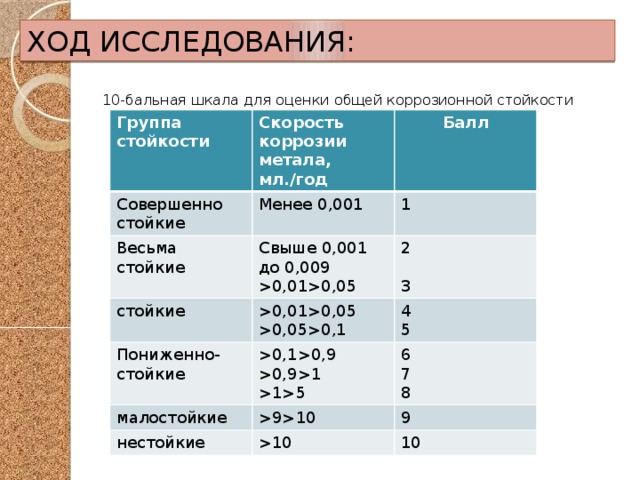
10-бальная шкала для оценки общей коррозионной стойкости металлов
Группа стойкости
Скорость коррозии метала, мл./год
Совершенно стойкие
Балл
Менее 0,001
Весьма стойкие
Свыше 0,001 до 0,009
стойкие
1
0,010,05
Пониженно-стойкие
0,010,05
2
0,050,1
0,10,9
малостойкие
4
0,91
3
нестойкие
910
6
5
7
15
10
9
8
10

ХОД ИССЛЕДОВАНИЯ :
В четыре пронумерованных стакана с
раствором хлорида натрия поместили четыре
железных гвоздя.

ХОД ИССЛЕДОВАНИЯ:
Стакан №1.
Железный
гвоздь опустили в
чистую воду:
прокорредировало
- В чистой воде коррозия идёт
медленнее
- Н₂О- слабый электролит
- Наблюдаем химическую
коррозию

Ход исследования:
Стакан № 2.
Железный гвоздь опустили в хлорид натрия:
- Скорость коррозии выросла
- Хлорид натрия увеличивает скорость коррозии
- Наблюдаем химическую коррозию

ХОД ИССЛЕДОВАНИЯ:
Стакан №3.
Железный гвоздь + медная проволока опущен в раствор хлорида натрия.
- Скорость коррозии очень велика
- Образовалось много ржавчины
- Хлорид натрия – сильнокоррозионная среда для железа
- Медь – менее активный металл

ХОД ИССЛЕДОВАНИЯ:
Стакан № 4.
Железный гвоздь опустили в хлорид натрия и добавили гидроксид натрия:
- Коррозия практически отсутствует
- Гидроксид натрия замедляет
коррозию
ингибитором

ХОД ИССЛЕДОВАНИЯ :
Опыты:
Вывод: Скорость коррозии зависит от:
- Природы металла
- Окислителя
- От концентрации
- От примисей

ХОД ИССЛЕДОВАНИЯ :
Виды защиты от коррозии
1.Поверхностные защитные покрытия металлов:
- Металлические
- Неметаллические
- Химические покрытия
2.Создание сплавов
3.Протекторная защита

Гипотеза верна , так как при погружении гвоздей в разные среды, скорость взаимодействия с железом была разной

Библиографический список:
- Габриелян О.С. Химия 11. Профильный уровень. 2016
- Акимов Г.В.Основы учения о коррозии и защите металлов М.2001
- Томашов Н.Д. Теория коррозии и окисления металлов. М.1983
- Эванс Ю.Р. Коррозия и окисление металлов/перевод с англ./М.1962
- Тодт Ф. Коррозия химической аппаратуры и коррозионностойкие металлы 3 изд.М. 1997
- Интернет ресурсы.
















 0,010,05 Пониженно-стойкие 0,010,05 2 0,050,1 0,10,9 малостойкие 4 0,91 3 нестойкие 910 6 5 7 15 10 9 8 10 " width="640"
0,010,05 Пониженно-стойкие 0,010,05 2 0,050,1 0,10,9 малостойкие 4 0,91 3 нестойкие 910 6 5 7 15 10 9 8 10 " width="640"



















