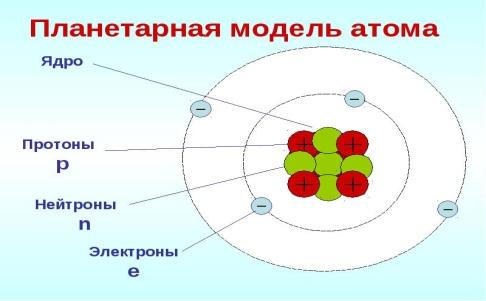
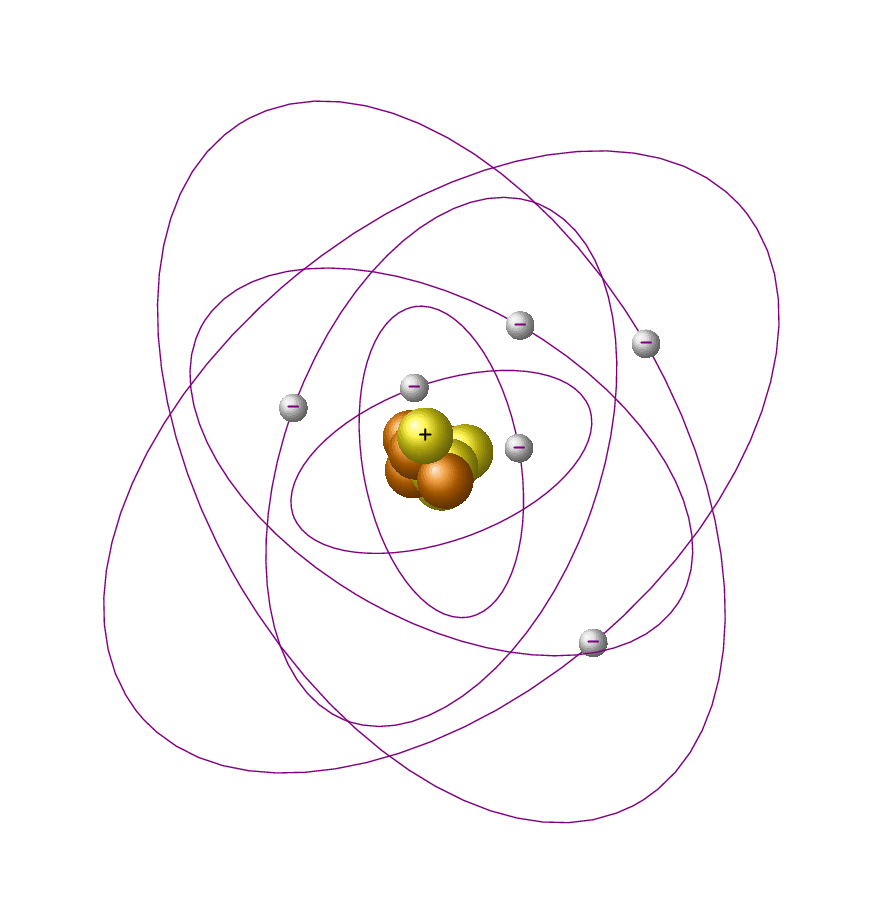
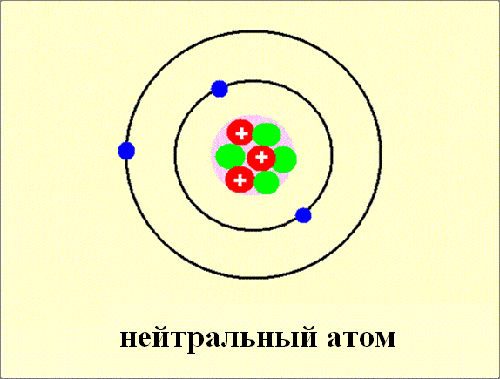
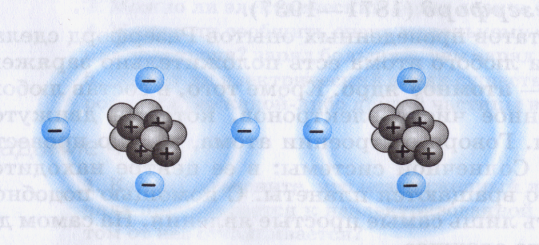
| Задание №2 «Думай – в паре-делись» Цель: структурированный способ развития идей и мыслей Проблемный вопрос: Как вы думаете, что может измениться в атоме, если он не благородный газ, а «хочет» иметь такую же оболочку? А что электроны отдаст, металл или неметалл? Почитайте §, найдите ответ. Формативное оценивание: взаимоооценивание в парах (учащиеся строят предположения, говорят, что, скорее всего, отдадут или примут ē.) Дескриптор: учащиеся объясняет, что ядра атомов прежние. Что изменяется в строении атома элемента. учащийся объясняет, что атом действительно отдают (металлы) или принимают (неметаллы) электроны. Групповая работа по составлению опорного конспекта с ключевыми понятиями. Работа с учебником и дополнительными ресурсами с целью изучения нового материала. Определения: ион, катион, анион. Рассмотреть ионный состав минеральной воды, выписать отрицательные и положительные ионы. Почему металлы стремятся отдать свои электроны? (Обосновать ответ на примере атома магния) Почему неметаллы стремятся принять электроны? (Обосновать ответ на примере атома серы) Ключевые понятия: нейтральный атом; положительно заряженный ион – катион, отрицательно заряженный – анион. Критерий оценивания: различает понятия «катион» и «анион». Дескриптор: верно определяет понятия «катион» и «анион», учащийся перечисляет в соответствии с заданиями понятия; различает понятия; «атом» и «ион», «катион» и «анион»; Взаимооценивание кластера. Расшифровать и озвучить кластер. Оценка – приём «аплодисменты». Физкультминутка. Задание № 3. Формативное оценивание: взаимоооценивание в парах. Изображены атом и ион бериллия. Проверить, нет ли ошибки в левом рисунке? Учащиеся смотрят в ПСХЭ, изучают состав ядра и эл.оболочку, говорят, что все верно. А какому благородному газу будет «подражать» бериллий, что в нем особенного? Дескриптор: учащиеся объясняет, что в изображении атома и иона бериллия нет ошибки; указывает сходство с гелием, количество электронов -2; объясняет появление заряда. Задания для групп. Карточки № 1,2,3. Оценить атом, показать, какой ион он мог бы образовать. Задание ФО. Работа в рабочих тетрадях (индивидуально) по карточкам.
№ 1. Заполните таблицу, характеризующую ионы Дескриптор: обучающийся - заполняет таблицу, характеризующую ионы; - показывает число протонов, общее количество электронов, общий заряд иона, электронное строение иона.
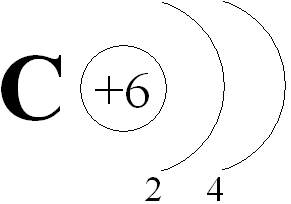
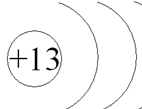
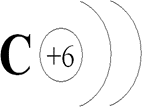
№ 2. Углерод образует ионы путём отдачи и приёма электронов. Отметьте кружком соответствующее количество электронов для атома и ионов углерода на данных схемах электронного строения.
Дескриптор: обучающийся - обозначает электроны для атома углерода; - обозначает электроны для иона углерода С+2; - обозначает электроны для иона углерода С+4; - обозначает электроны для иона углерода С-4. Загадка-вопрос в конце урока, чтобы начать с неё следующие занятия - как атомы образуют вещества с ионной связью, составление формул соединений.
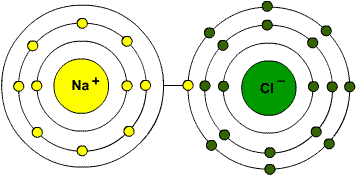
«Натрий с серой повстречался Полюбил и обвенчался. Ей отдав свой электрон, Превратился в катион. Электрон тот сера приняла, Анионом сразу стала, А супружеская связь Вдруг ионной назвалась». |