Просмотр содержимого документа
«Кремний и его соединения»


Кто хочет съесть ядро ореха, должен расколоть его скорлупу.
Цели урока:
Дать общую характеристику элементу кремний. Рассмотреть природные соединения кремния. Провести сравнительный анализ с соединениями углерода . Изучить свойства кремния.

План характеристики:
- Открытие кремния
- Получение кремния
- Строение и свойства атомов
- Физические свойства кремния
- Химические свойства кремния
- Соединения кремния
- Применение кремния

Открытие кремния
Кремний был впервые открыт в 1811 году Гей-Люссаком и Тенаром. Он является одним из наиболее распространенных в земной коре элементов. Массовая доля кремния составляет 27,6 % . В природе встречается в виде оксидов, силикатов и алюмосиликатов.

Входит также в состав растений и животных. Анализ образцов лунного грунта показал наличие SiO 2 в количестве более 40 % .


Получение кремния
SiF 4 +4K=4KF+Si
Лабораторный способ:
SiO 2 +2Mg=Si+2MgO
Промышленный способ:
SiO 2 +2 C=2CO+Si

Строение и свойства атомов

Физические свойства кремния
Кремний – кристаллическое вещество темно-серого цвета с металлическим блеском. Кристаллическая решетка кремния напоминает структуру алмаза. Полупроводник. t плав ( Si )=1415 ˚ C , t плав (алмаз)=3730 ˚ C .

Химические свойства кремния
- Si+O 2 =SiO 2 2) Si+NaOH+H 2 O=Na 2 SiO 3 +2H 2 ↑ 3) Si+C=SiC 4) Si+2Mg=Mg 2 Si 1) Mg 2 Si+H 2 O=2Mg(OH) 2 +SiH 4 2) SiH 4 +2O 2 =SiO 2 +2H 2 O

Соединение кремния
Свойства CO 2
Свойства SiO 2
Кислотный оксид
Молекулярная кристаллическая решетка
Бесцветный газ, при сжатии и охлаждении легко переходит в жидкое и твердое состояние («сухой лед»).
Химические свойства
H 2 O+CO 2 ↔H 2 CO 3
CO 2 +CaO=CaCO 3
CO 2 +Ca(OH) 2 =CaCO 3 +H 2 O
CO 2 +2Mg=2MgO+C
C+CO 2 =2CO ↑
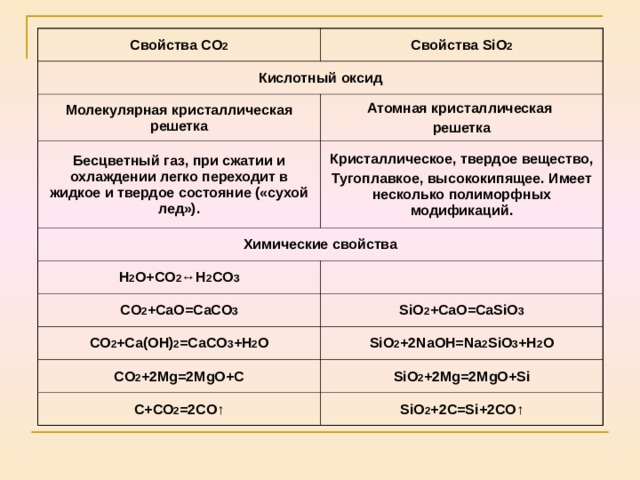
Свойства CO 2
Свойства SiO 2
Кислотный оксид
Молекулярная кристаллическая решетка
Атомная кристаллическая
решетка
Бесцветный газ, при сжатии и охлаждении легко переходит в жидкое и твердое состояние («сухой лед»).
Кристаллическое, твердое вещество,
Тугоплавкое, высококипящее. Имеет несколько полиморфных модификаций.
Химические свойства
H 2 O+CO 2 ↔H 2 CO 3
CO 2 +CaO=CaCO 3
SiO 2 +CaO=CaSiO 3
CO 2 +Ca(OH) 2 =CaCO 3 +H 2 O
SiO 2 +2NaOH=Na 2 SiO 3 +H 2 O
CO 2 +2Mg=2MgO+C
SiO 2 +2Mg=2MgO+Si
C+CO 2 =2CO ↑
SiO 2 +2C=Si+2CO ↑

Кремний
- его 26 % в природе
- по распространению в земной коре занимает 2-е место
- образует оксиды с валентностью ( IV )
- его оксиды являются основной частью песка и глины
- в виде кристаллов входит в состав горных пород
- образует бесцветные кристалла кварца и горного хрусталя
- на его основе создано промышленное производство керамики, стекла, цемента
- полупроводник

- Кремний в отличии от углерода в свободном виде в природе не встречается.
- Кремний может быть, как окислителем так и восстановителем.
- Оксид кремния в отличии от оксида углерода ( IV ) с водой не взаимодействует.
- Кремний - полупроводник, его соединение используют для получения стекла, цемента, бетона, а также для получения кирпича, фарфора, фаянса и изделия из них.
































