Просмотр содержимого документа
«Кремний и его соединения»
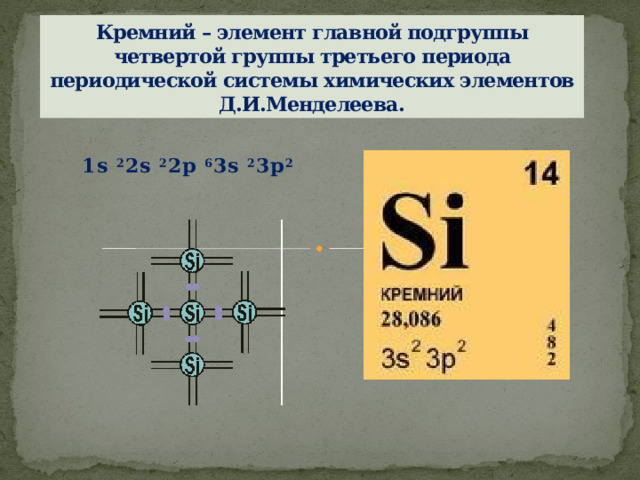
Кремний – элемент главной подгруппы четвертой группы третьего периода периодической системы химических элементов Д.И.Менделеева.
1s 2 2s 2 2p 6 3s 2 3p 2

Историческая справка
Чистый элементарный кремний был получен шведским химиком Йенсом Якобом Берцелиусом в 1825 году действием металлического калия на фтористый кремний SiF 4
Русское название «кремний» введено в 1834 году российским химиком Германом Ивановичем Гессом. В переводе с древнегреческого κρημνός — «утес, гора».

Нахождение в природе
Кремний – второй по распространенности после кислорода химический элемент. Земная кора более чем на четверть состоит из его соединений. В природе кремний встречается только в виде диоксидов (кремнезёма) и солей кремниевой кислоты (силикатов). Наиболее широко распространены алюмосиликаты.
Кварц
Слюда
Кварц
Полевой шпат
K 2 O*Al 2 O 3 *SiO 2
SiO 2
K 2 O*Al 2 O 3 *6SiO 2 *H 2 O

Физические свойства
Кристаллический кремний
Аморфный кремний
Образуется путем прокаливания с магнием мелкого белого песка.
Получается путем направленной кристаллизации расплава в тигле, а также методом зонной плавки.
- Мелкий порошок бурого цвета.
- Плотность – 2,0 г/см³
- Температура плавления – 1400ºС.
- Твердое вещество темно-серого цвета со слабым металлическим блеском.
- Полупроводник.

Химические свойства
t
Si + O 2 → SiO 2
- Горит в кислороде, образуя диоксид кремния:
- При нагревании соединяется с металлами с образованием силицидов:
- Взаимодействует со щелочами, образуя силикаты и водород:
- Силан на воздухе самовоспламеняется и сгорает с образованием диоксида кремния и воды:
- Силициды разлагаются водой или кислотами, при этом выделяется газообразное водородное соединение кремния – силан:
t
Si + 2Mg → Mg 2 Si
Si + 2 NaOH + H 2 O→
→ Na 2 SiO 3 + 2H 2 ↑
SiH 4 + 2O 2 = SiO 2 + 2H 2 O
Mg 2 Si + 2H 2 SO 4 → 2MgSO 4 + SiH 4 ↑

Получение кремния
Кремний получают, восстанавливая его из оксида кремния (IV) магнием или углеродом:
t
SiO 2 + 2Mg = 2MgO + Si,
t
SiO 2 + 2C = Si + 2CO↑.

Радуга кремнезёма
Опал
Агат
Аметист
Агат
Халцедон
Яшма
Сердолик

Радуга кремнезёма
Оксид кремния (IV), или кремнезем SiO 2 , как и CO 2 , является кислотным оксидом. Однако, он имеет не молекулярную, а кристаллическую решетку.
Физические свойства:
Твердое и тугоплавкое вещество. Не растворяется в воде и кислотах (кроме плавиковой). Взаимодействует при высоких температурах со щелочами с образованием солей кремниевой кислоты – силикатов.
t
SiO 2 + 2NaOH = Na 2 SiO 3 + H 2 O
t
SiO 2 + CaO = CaSiO 3
t
SiO 2 + CaCO 3 = CaSiO 3 + CO 2 ↑
Химические свойства:

Применение кремния
Si

Применение кремния
SiО 2

Объекты, содержащие кремний.
Диатомовые водоросли
Морские губки
Китайский погребальный сосуд
Кремниевый мушкет
Хвощ
Радиолярии

почва
песок
глина
Роль кремния в организме человека
- Кремний - основной структурный элемент, обеспечивающий четкость и слаженность управления работой всех органов со стороны нервной системы.

- В сосудистой стенке происходит замещение кремния кальцием, который делает сосуды жесткими.
- Эксперименты французских ученых М. и Ж. Лепгер доказали, что введение в организм соединений кремния приостанавливает развитие атеросклероза и помогает восстановить функцию сосудистой стенки.

Продукты, содержащие кремний



































