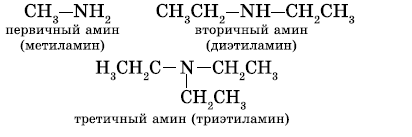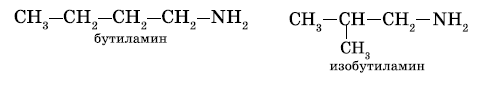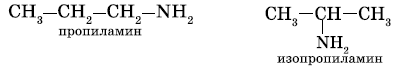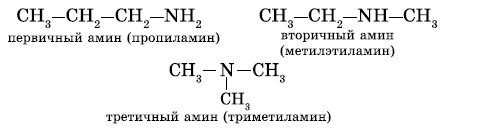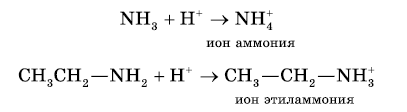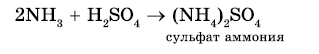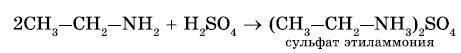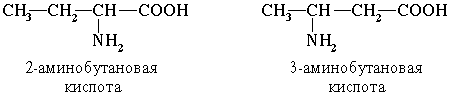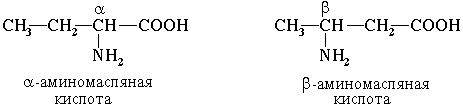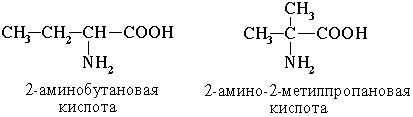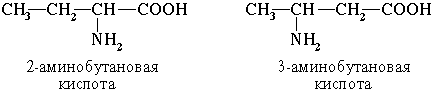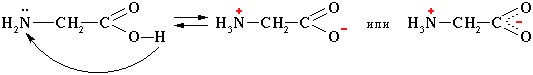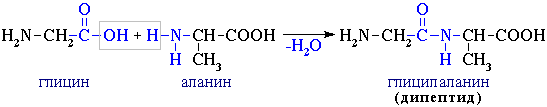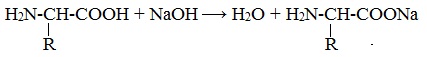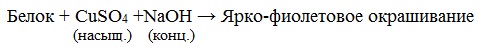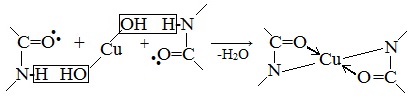Лекционный учебный материал
Учебная дисциплина ОУД .10 Химия
Преподаватель
Группы
Тема: Азотсодержащие органические соединения.
Амины. Аминокислоты. Белки.
ЦЕЛЬ: рассмотреть классификацию, изомерию, номенклатуру, свойства аминов, аминокислот, понятие о белках, уметь, познакомиться с областями применения.
Задание 1. Ознакомьтесь с теоретическим материалом занятия. Составить опорный конспект, используя различные источники литературы и интернет ресурсы по плану:
1. Определение.
2. Классификация.
3. Номенклатура и изомерия.
4. Физические свойства.
5. Химические свойства.
6. Применение.
Амины – азотсодержащие органические вещества, производные аммиака (NH3), в молекулах которых один или несколько атомов водорода замещены на углеводородный радикал (- R или – CnH2n+1)
Классификация аминов
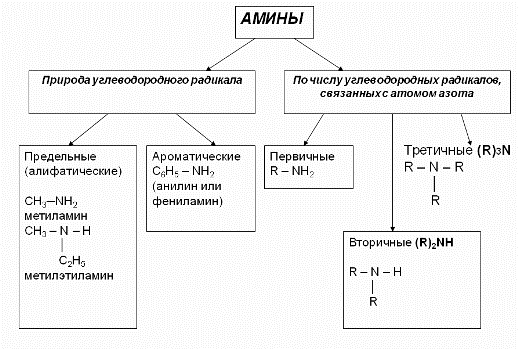
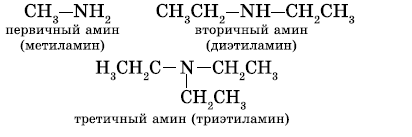
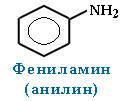
Амины, в которых аминогруппа связана непосредственно с ароматическим кольцом, называются ароматическими аминами.
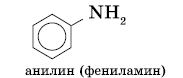
Простейшим представителем этих соединений является аминобензол, или анилин:
Функциональная группа: - NH2 аминогруппа
Изомерия аминов
1. Для аминов характерна структурная изомерия:
а) изомерия углеродного скелета начиная с С4H9NH2:
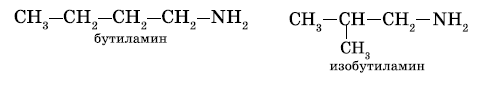
б) изомерия положения функциональной группы: начиная с С3H7NH2
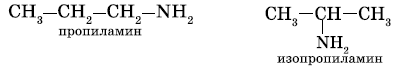
2. изомерия аминогруппы, связанная с изменением степени замещенности атомов водорода при азоте, т.е. между типами аминов.
Первичные, вторичные и третичные амины изомерны друг другу (межклассовая изомерия):
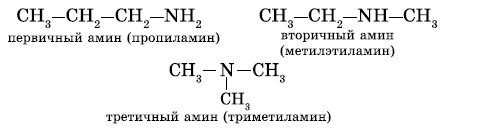
Как видно из приведенных примеров, для того чтобы назвать амин, перечисляют заместители, связанные с атомом азота (по порядку старшинства), и добавляют суффикс —амин.
Номенклатура аминов
1. В большинстве случаев названия аминов образуют из названий углеводородных радикалов и суффикса амин.
CH3-NH2 метиламин
CH3-CH2-NH2 этиламин
Различные радикалы перечисляются в алфавитном порядке.
CH3-CH2-NH-CH3 метилэтиламин
2. Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -NH2. В этом случае аминогруппа указывается в названии суффиксами амин (одна группа -NH2), диамин (две группы -NH2) и т.д. с добавлением цифр, отражающих положение этих групп в главной углеродной цепи.
Например:
CH3-CH2-CH2-NH2 пропанамин-1
H2N-CH2-CH2-CH(NH2)-CH3 бутандиамин-1,3
Нахождение аминов в природе
Амины широко распространены в природе, так как образуются при гниении живых организмов.
Получение аминов
1842 г Н. Н. Зинин получил анилин восстановлением нитробензола - в промышленности.
Восстановление нитросоединений:
R-NO2 + 6[H] t,kat-Ni → R-NH2 + 2H2O
(р. Зинина)
Другие способы:
1). Промышленный
CH3Br + 2NH3 t, ↑p → CH3-NH2 + NH4Br
Физические свойства аминов
ВИДЕО:
Изучение физических свойств анилина
Метиламин, диметиламин и триметиламин — газы, средние члены алифатического ряда - жидкости, высшие — твердые вещества.
Низшие амины имеют характерный «рыбный» запах, высшие не имеют запаха.
Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов:
Анилин представляет собой бесцветную маслянистую жидкость с характерным запахом (т. кип. 184 °С, т. пл. – 6 °С). На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит.
Химические свойства
Химические свойства аминов определяются в основном наличием у атома азота неподеленной электронной пары.
По химическим свойствам амины похожи на аммиак.
Амины как основания
ВИДЕО:
Получение гидроксида диметиламмония и изучение его свойств
ВИДЕО:
Изучение среды раствора анилина
Атом азота аминогруппы, подобно атому азота в молекуле аммиака, за счет неподеленной пары электронов может образовывать ковалентную связь по донорно-акцепторному механизму, выступая в роли донора. В связи с этим амины, как и аммиак, способны присоединять катион водорода, т. е. выступать в роли основания:
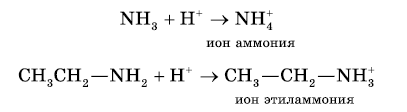
1. Реакция амионов с водой приводит к образованию гидроксид-ионов:
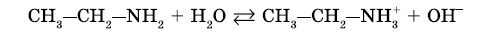
Раствор аммиака в воде обладает слабыми щелочными (основными) свойствами. Причина основных свойств аммиака — наличие у атома азота неподеленной электронной пары, которая участвует в образовании донорно-акцепторной связи с ионом водорода. По этой же причине амины также являются слабыми основаниями. Амины — органические основания.
2. Реакция с кислотами. Аммиак, реагируя с кислотами, образует соли аммония. Амины также способны вступать в реакцию с кислотами:
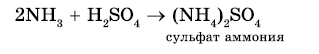
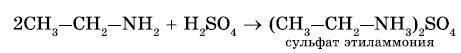
Взаимодействие с кислотами — образование солей (реакции нейтрализации). Аналогично при взаимодействии аминов с кислотами образуются соли замещенного аммония. Щелочи, как более сильные основания, вытесняют аммиак и амины из их солей.
Горение аминов
ВИДЕО:
Получение диметиламина и его горение
Амины являются горючими веществами. Продуктами горения аминов, как и других азотсодержащих органических соединений, являются углекислый газ, вода и свободный азот.
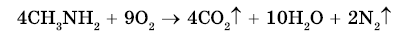
Применение
Амины используют при получении лекарственных веществ, красителей и исходных продуктов для органического синтеза. Гексаметилендиамин при поликонденсации с адипиновой кислотой дает полиамидные волокна.
Анилин находит широкое применение в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты).
Аминокислоты — органические амфотерные соединения, в состав которых входят карбоксильные группы – СООН и аминогруппы -NH2.
Аминокислоты можно рассматривать как карбоновые кислоты, в молекулах которых атом водорода в радикале замещен аминогруппой.
Классификация
Аминокислоты классифицируют по структурным признакам.
1.В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на α-, β-, γ-, δ-, ε- и т. д.
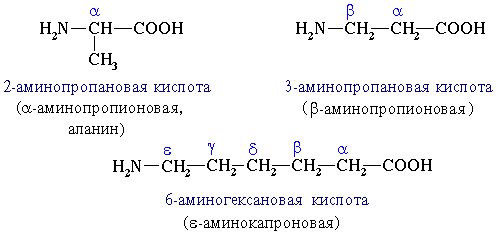
Строение аминокислот
Аминокислоты — гетерофункциональные соединения, которые обязательно содержат две функциональные группы:
аминогруппу — NH2 и карбоксильную группу —СООН, связанные с углеводородным радикалом.
Общую формулу простейших аминокислот можно записать так:
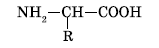
Так как аминокислоты содержат две различные функциональные группы, которые оказывают влияние друг на друга, характерные реакции отличаются от характерных реакций карбоновых кислот и аминов.
Изомерия и номенклатура аминокислот
По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе.
Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
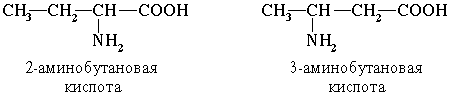
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Например:
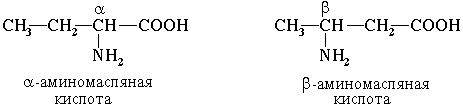
Для α-аминокислот R-CH(NH2)COOH
,которые играют исключительно важную роль в процессах жизнедеятельности животных и растений, применяются тривиальные названия.
Таблица. Некоторые важнейшие α-аминокислоты
| Аминокислота | Сокращённое обозначение | Строение радикала ( R ) |
| Глицин | Gly (Гли) | H - |
| Аланин | Ala (Ала) | CH3 - |
| Валин | Val (Вал) | (CH3)2CH - |
| Лейцин | Leu (Лей) | (CH3)2CH – CH2 - |
| Серин | Ser (Сер) | OH- CH2 - |
| Тирозин | Tyr (Тир) | HO – C6H4 – CH2 - |
| Аспарагиновая кислота | Asp (Асп) | HOOC – CH2 - |
| Глутаминовая кислота | Glu (Глу) | HOOC – CH2 – CH2 - |
| Цистеин | Cys (Цис) | HS – CH2 - |
| Аспарагин | Asn (Асн) | O = C – CH2 – │ NH2 |
| Лизин | Lys (Лиз) | NH2 – CH2- CH2 – CH2 - |
| Фенилаланин | Phen (Фен) | C6H5 – CH2 - |
Изомерия
1. Изомерия углеродного скелета
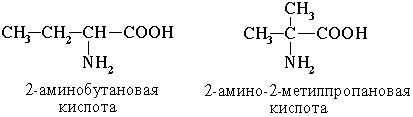
2. Изомерия положения функциональных групп
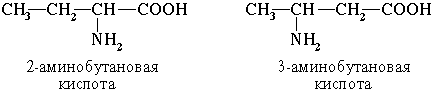
Физические свойства
Аминокислоты представляют собой кристаллические вещества с высокими (выше 250°С) температурами плавления, которые мало отличаются у индивидуальных аминокислот и поэтому нехарактерны. Плавление сопровождается разложением вещества.
Аминокислоты хорошо растворимы в воде и нерастворимы в органических растворителях, чем они похожи на неорганические соединения. Многие аминокислоты обладают сладким вкусом.
Способы получения
1.Взаимодействие α-галогенкарбоновых кислот с избытком аммиака. В ходе этих реакций происходит замещение атома галогена в галогенкарбоновых кислотах на аминогруппу. Выделяющийся при этом хлороводород связывается избытком аммиака в хлорид аммония.
2.Гидролиз белков.
При гидролизе белков обычно образуются сложные смеси аминокислот, однако с помощью специальных методов из этих смесей можно выделять отдельные чистые аминокислоты.
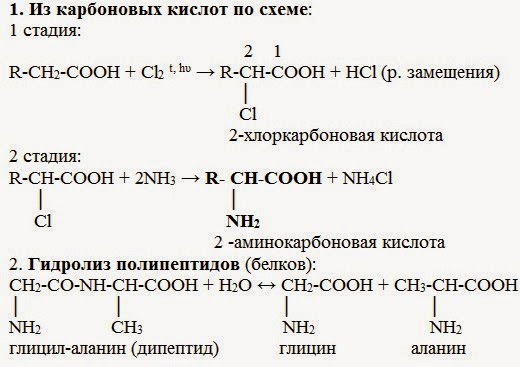
3. Микробиологический синтез. Известны микроорганизмы, которые в процессе жизнедеятельности продуцируют α - аминокислоты белков.
Химические свойства
Аминокислоты являются амфотерными соединениями, для них характерны кислотно-основные свойства. Это обусловлено наличием в их молекулах функциональных групп кислотного (-СООН) и основного (-NH2) характера.
В водных растворах и твердом состоянии аминокислоты существуют в виде внутренних солей.
Ионизация молекул аминокислот в водных растворах зависит от кислотного или щелочного характера среды.
Водные растворы аминокислот в кислой и щелочной среде проводят электрический ток.
1. С основаниями (участвует аминогруппа).→ образуются соли:
NH2-CH2-COOH + NaOH → NH2-CH2-COONa + H2O
NH2-CH2-COONa - натриевая соль 2-аминоуксусной кислоты
2. Со спиртами → образуются сложные эфиры – летучие вещества (р. этерификации): NH2-CH2-COOH + CH3OH HCl(газ)→ NH2-CH2-COOCH3 + H2O
NH2-CH2-COOCH3 - метиловый эфир 2- аминоуксусной кислоты
3С сильными кислотами (участвует карбоксильная группа).
→ соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или HOOC-CH2-NH2*HCl
4. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе:
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе:
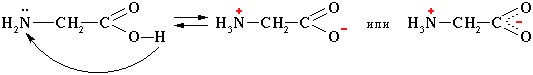
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп.
Видео-опыт «Свойства аминоуксусной кислоты»
2. Поликонденсация → образуются полипептиды (белки):
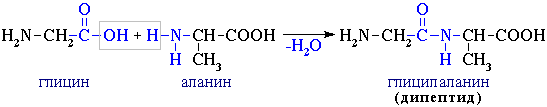
При взаимодействии двух α-аминокислот образуется дипептид.
3. Разложение → Амин + Углекислый газ:
NH2-CH2-COOH → NH2-CH3 + CO2↑
II. Свойства карбоксильной группы (кислотность)
1. С основаниями → образуются соли:
NH2-CH2-COOH + NaOH → NH2-CH2-COONa + H2O
NH2-CH2-COONa - натриевая соль 2-аминоуксусной кислоты
2. Со спиртами → образуются сложные эфиры – летучие вещества (р. этерификации): NH2-CH2-COOH + CH3OH HCl(газ)→ NH2-CH2-COOCH3 + H2O
NH2-CH2-COOCH3 - метиловый эфир 2- аминоуксусной кислоты
3. С аммиаком → образуются амиды:
NH2-CH(R)-COOH + H-NH2 → NH2-CH(R)-CONH2 + H2O
4. Практическое значение имеет внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона):
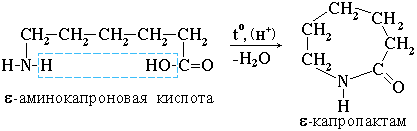
III. Свойства аминогруппы (основность)
1. С сильными кислотами → соли:
HOOC-CH2-NH2 + HCl → [HOOC-CH2-NH3]Cl
или HOOC-CH2-NH2*HCl
2. С азотистой кислотой (подобно первичным аминам):
NH2-CH(R)-COOH + HNO2 → HO-CH(R)-COOH + N2↑+ H2O
гидроксокислота
Измерение объёма выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка)
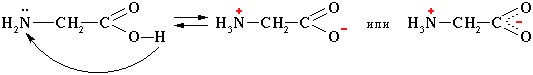
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп.
Применение
1) аминокислоты широко распространены в природе;
2) молекулы аминокислот – это те кирпичики, из которых построены все растительные и животные белки; аминокислоты, необходимые для построения белков организма, человек и животные получают в составе белков пищи;
3) аминокислоты прописываются при сильном истощении, после тяжелых операций;
4) их используют для питания больных;
5) аминокислоты необходимы в качестве лечебного средства при некоторых болезнях (например, глутаминовая кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты применяются в сельском хозяйстве для подкормки животных, что положительно влияет на их рост;
7) имеют техническое значение: аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна – капрон и энант.
Белки — это природные высокомолекулярные соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков α-аминокислот.
В основу классификации белков положены их физико-химические и химические особенности. Белки классифицируют по нескольким признакам.
Видео:Белки.
http://school-collection.edu.ru/catalog/res/d7791f38-8cff-11db-b606-0800200c9a66/view/
Видео: Свойства белков. Превращение белков в организме. Успехи в изучении и синтезе белков.
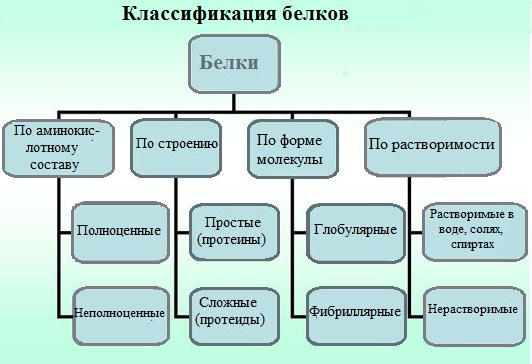
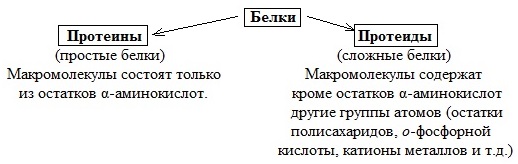
По химическому строению молекул все белки подразделяют на простые и сложные.
Простые белки (протеины) состоят только из аминокислот. К простым белкам относят альбумины, глобулины, протамины, гистоны, проламины, глютелины, протеиноиды.
Сложные белки (протеиды) состоят из глобулярных белков и небелкового компонента. Небелковая часть сложного белка называется простетической группой.
Структура белка
Белки обладают неисчерпаемым разнообразием структур.
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями.
Третичная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль.
Четвертичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной.
Физические свойства
Физические свойства белков так же разнообразны, как и функции, которые они выполняют.
Белки — кристаллические вещества белого цвета, в растворе – бесцветные вещества, если они не несут какой-нибудь хромофорной (окрашенной) группы, как, например, гемоглобин.
Кристаллические твердые белки – это запасные соединения.
По растворимости в воде белки бывают:
Глобулярные — растворяются в воде, образуют коллоидные растворы (белок молока – казеин, белок яйца – альбумин);
Фибриллярные — в воде не растворяются (кератин – волосы, ногти, перья; коллаген – мускулы, сухожилия; фиброин шелка).
Растворы фибриллярных белков обладают большой вязкостью. Примером может служить коллаген — белок соединительной ткани.
Денатурированные белки (кератин волос, миозин мускулов) являются опорными белками. Фибриллярные белки – это материал тканей сухожилий, мускульных и покровных тканей.
Белки не имеют температуры плавления и кипения, так как большинство из них при нагревании сворачиваются. При высокой температуре все белки сгорают.
Некоторые белки могут быть выделены в виде кристаллов (белок куриного яйца, гемоглобин крови).
Число аминокислотных остатков, входящих в молекулы отдельных белков, весьма различно: в инсулине их 51, в миоглобине – 153.
Поэтому и молекулярная масса белков колеблется в очень широких пределах – от 10 000 до десятков миллионов.
Например, гормон инсулин имеет молекулярную массу 5733, фермент рибонуклеаза – 13700, альбумин человека — 68500, белок крови гемоглобин – 64500, фибриноген крови – 400.000, белки вирусов – 50.000.000.
Белки входят в состав всех живых организмов и выполняют разнообразные биологические функции.
Первый белок, с которым мы знакомимся в своей жизни, это белок куриного яйца – альбумин, он хорошо растворяется в воде, при нагревании
свертывается, а при долгом хранении в тепле разрушается — яйцо протухает.
Волосы, ногти, когти, шерсть, перья, копыта, наружный слой кожи — все они почти целиком состоят из белка кератина. Кератин не растворяется в воде, не свертывается, не разрушается в земле: рога древних животных сохраняются в ней так же хорошо, как и кости.
Белок пепсин, содержащийся в желудочном соке, способен разрушать другие белки в процессе пищеварения.
Белок интерферон применяется при лечении насморка и гриппа, т.к. убивает вызывающие эти болезни вирусы.
А белок змеиного яда способен убить человека.
Химические свойства
1. Амфотерные свойства белков
Как и аминокислоты, белки являются амфотерными соединениями, так как молекула любого белка содержит на одном конце группу -NH2, а на другом конце – группу -СООН.
Так, при действии щелочей белок реагирует в форме аниона – соединяется с катионом щелочи:
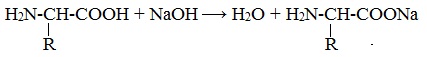
При действии же кислот он выступает в форме катиона:
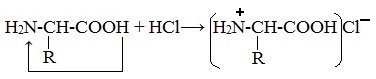
Если в молекуле белка преобладают карбоксильные группы, то он проявляет свойства кислот, если же преобладают аминогруппы, — свойства оснований.
Очень важным для жизнедеятельности живых организмов является буферное свойство белков, т.е. способность связывать как кислоты, так и основания, и поддерживать постоянное значение рН различных систем живого организма.
Белки обладают и специфическими физико-химическими свойствами.
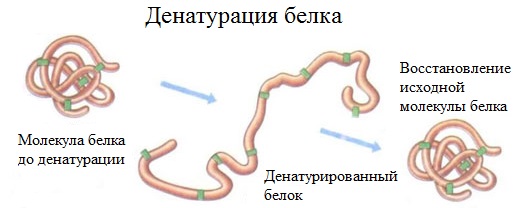
2. Денатурация белка (необратимое осаждение, свертывание)
Денатурация – это разрушение вторичной и третичной структуры белка (полное или частичное) и изменение его природных свойств с сохранением первичной структуры белка.
Сущность денатурации белка сводится к разрушению связей, обусловливающих вторичную и третичную структуры молекулы (водородных, солевых и других мостиков). А это приводит к дезориентации конфигурации белковой молекулы.
Денатурация бывает обратимой и необратимой.
Обратимая денатурация белка происходит при употреблении алкоголя, солёной пищи.
Необратимая денатурация может быть вызвана при действии таких реагентов, как концентрированные кислоты и щелочи, спирты, в результате воздействия высокой температуры, радиации, при отравлении организма солями тяжелых металлов (Hg2+, Pb2+, Си2+).
Например, яичный белок альбумин осаждается из раствора (свертывается) при варке яиц (при температуре 60-700С), теряя способность растворяться в воде.
Видеоопыт «Свертывание белков при нагревании»
Видеоопыт «Осаждение белков солями тяжелых металлов»
Видеоопыт «Осаждение белков спиртом»
3. Гидролиз белков
Гидролиз белков – это необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот.
Анализируя продукты гидролиза, можно установить количественный состав белков.
Переваривание белков в организме по своей сути представляет ферментативный гидролиз белковых молекул.
В лабораторных условиях и в промышленности проводится кислотный гидролиз.
В ходе гидролиза белков происходит разрушение пептидных связей. Гидролиз белка имеет ступенчатый характер.
4. Цветные (качественные) реакции на белки
Для белков известно несколько качественных реакций.
а) Ксантопротеиновая реакция (на остатки аминокислот, содержащих бензольные кольца)
Белки, содержащие остатки ароматических аминокислот (фенилаланина, тирозина), дают желтое окрашивание при действии концентрированной азотной кислоты.

Причина появления окраски – образование нитропроизводных ароматических аминокислот, например, фенилаланина: 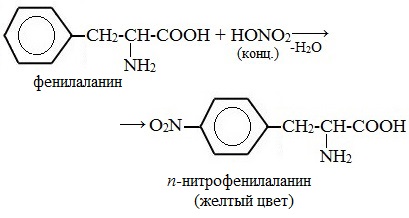
Видеоопыт «Ксантопротеиновая реакция на белки»
б) Биуретовая реакция (на пептидные связи)
Все соединения, содержащие пептидную связь, дают фиолетовое окрашивание при действии на них солей меди (II) в щелочном растворе.

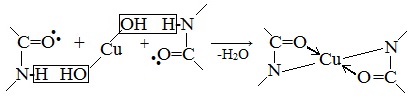
Причина появления окраски – образование комплексных соединений с координационным узлом: 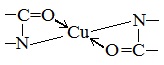
Видеоопыт «Биуретовая реакция белков»
Видеоопыт «Качественные реакции на белки: биуретовая и ксантопротеиновая»
в) Цистеиновая реакция (на остатки аминокислот, содержащих серу)

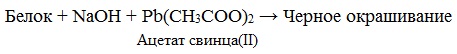
Причина появления окраски – образование черного осадка сульфида серебра (II) PbS.
Видеоопыт «Качественное определение азота в органических соединениях»
Функции белков в природе универсальны. Белки входят в состав всех живых организмов. Мышцы, кости, покровные ткани, внутренние органы, хрящи, шерсть, кровь — все это белковые вещества.
Растения синтезируют белки из углекислого газа и воды за счет фотосинтеза. Животные организмы получают, в основном, готовые аминокислоты с пищей и на их базе строят белки своего организма.
Ни один из известных нам живых организмов не обходится без белков. Белки служат питательными веществами, они регулируют обмен веществ, исполняя роль ферментов – катализаторов обмена веществ, способствуют переносу кислорода по всему организму и его поглощению, играют важную роль в функционировании нервной системы, являются механической основой мышечного сокращения, участвуют в передаче генетической информации и т.д.
Видеофильм «Функции белков»
Разнообразные функции белков определяются a-аминокислотным составом и строением их высокоорганизованных макромолекул.
1. Каталитическая (ферментативная) функция
Каталитическая функция — одна из основных функций белков. Абсолютно все биохимические процессы в организме протекают в присутствии катализаторов – ферментов. Все известные ферменты представляют собой белковые молекулы.
Белки – это очень мощные катализаторы. Они ускоряют реакции в миллионы раз, причем для каждой реакции существует свой фермент.
В настоящее время известно свыше 2000 различных ферментов, которые являются биологическими катализаторами.
Например, фермент пепсин расщепляет белки в процессе пищеварения.
Даже такая простая реакция как гидратация углекислого газа катализируется ферментом карбоангидразой.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК.
2. Транспортная функция
Некоторые белки способны присоединять и переносить (транспортировать) различные вещества по крови от одного органа к другому и в пределах клетки.
Белки транспортируют липиды (липопротеиды), углеводы (гликопротеиды), ионы металлов (глобулины), кислород и углекислый газ (гемоглобин), некоторые витамины, гормоны и др.
Например, альбумины крови транспортируют липиды и высшие жирные кислоты (ВЖК), лекарственные вещества, билирубин.
Белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
Белок миоглобин запасает кислород в мышцах.
Специфические белки-переносчики обеспечивают проникновение минеральных веществ и витаминов через мембраны клеток и субклеточных структур.
Скрыть объявление
3. Защитная функция
Защитную функцию выполняют специфические белки (антитела — иммуноглобулины), которые вырабатываются иммунной системой организма. Они обеспечивают физическую, химическую и иммунную защиту организма путем связывания и обезвреживания веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Например, белок плазмы крови фибриноген участвует в свертывании крови (образовывает сгусток). Это защищает организм от потери крови при ранениях.
Альбумины обезвреживают ядовитые вещества (ВЖК и билирубин) в крови.
Антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки. Интерфероны — универсальные противовирусные белки.
Многие живые существа для обеспечения защиты выделяют белки, называемые токсинами, которые в большинстве случаев являются сильными ядами. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
4. Сократительная (двигательная) функция
Важным признаком жизни является подвижность, в основе которой лежит данная функция белков, таких как актин и миозин – белки мышц. Кроме мышечных сокращений к этой функции относят изменение форм клеток и субклеточных частиц.
B результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
5. Структурная функция
Структурная функция — одна из важнейших функций белков. Белки играют большую роль в формировании всех клеточных структур.
Белки – это строительный материал клеток. Из них построены опорные, мышечные, покровные ткани.
Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей, эластин стенок кровеносных сосудов, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
Кератин синтезируется кожей. Волосы и ногти – это производные кожи.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
Скрыть объявление
6. Гормональная (регуляторная) функция
Регуляторная функция присуща белкам-гормонам (регуляторам). Они регулируют различные физиологические процессы.
Например, наиболее известным гормоном является инсулин, регулирующий содержание глюкозы в крови. При недостатке инсулина в организме возникает заболевание, известное как сахарный диабет.
7. Питательная (запасная) функция
Питательная функция осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
8. Рецепторная (сигнальная) функция
Некоторые белки (белки-рецепторы), встроенные в клеточную мембрану, способны изменять свою структуру под воздействием внешней среды. Так происходит прием сигналов извне и передача информации в клетку.
Например, действие света на сетчатку глаза воспринимается фоторецептором родопсином.
Рецепторы, активизируемые низкомолекулярными веществами типа ацетилхолина, передают нервные импульсы в местах соединения нервных клеток.
Скрыть объявление
9. Энергетическая функция
Белки могут выполнять энергетическую функцию, являясь одним из источников энергии в клетке (после их гидролиза). Обычно белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Но в качестве источника энергии белки используются крайне редко. Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Значение белков в организме человека
Значение белков для организма имеет огромную роль. Белки выполняют множество жизненно важных функций в человеческом организме:
— служат материалом для построения клеток, тканей и органов, образования ферментов, большинства гормонов, гемоглобина и других соединений;
— формируют соединения, обеспечивающие иммунитет к инфекциям;
— участвуют в процессе усвоения жиров, углеводов, витаминов и минеральных веществ.
Как источник энергии белки имеют второстепенное значение, поскольку могут быть заменены жирами и углеводами.
В отличие от жиров и углеводов, белки не накапливаются в резерве и не образуются из других пищевых веществ, являясь незаменимой частью пищи.
Для человека потребление животного белка биологически более ценно, чем растительного, поскольку содержащиеся в животном белке незаменимые аминокислоты легче перевариваются и растворяются человеческим организмом.
Белки поддерживают упругость кожи, отвечают за здоровье волос и ногтей. Эти соединения способствуют поддержанию тела в тонусе, так как в качестве расщепления они влияют на формирование мышц. Белки являются главным стимулятором метаболизма.
Недостаток белков ведет к нарушению ряда функций организма, в том числе функций печени, поджелудочной железы, тонкой кишки, нервной и эндокринной систем. Кроме того, наблюдаются нарушения кроветворения, обмена жиров и витаминов, развивается атрофия мышц. Ухудшается работоспособность человека, снижается его сопротивляемость к инфекциям.
Особенно неблагоприятно сказывается белковая недостаточность на растущем организме: замедляется его рост, нарушается образование костей, задерживается умственное развитие.
Избыток поступления белков оказывает также негативное воздействие на организм. При этом страдают сердечно-сосудистая система, печень и почки, усиливаются процессы гниения в кишечнике, нарушается обмен витаминов.
Потребность организма в белке зависит от ряда причин: с возрастом она снижается, но, при стрессовых ситуациях, независимо от возраста, потребность в белках значительно возрастает. Во время занятия спортом количество протеина должно быть увеличено.