
Тема урока 8 класс:
Классификация химических элементов
Составитель: учитель химии Фомина К.Н.

Предшественники Д. И. Менделеева
1. Й. Я. Берцелиус ( шведский учёный ) классифицировал все элементы на металлы и неметаллы. Он определил, что металлам чаще всего соответствуют
основные оксиды и основания , а неметаллам – кислотные оксиды и кислоты.
- Na→Na 2 O→NaOH
- S →SO 3 →H 2 SO 4
![Свойства гидроксида цинка Взаимодействие гидроксида цинка с соляной кислотой: Zn(OH) 2 + 2HCl = ZnCl 2 + 2H 2 O Вывод: гидроксид цинка – основание 2. Взаимодействие гидроксида цинка с гидроксидом натрия: Zn(OH) 2 + 2NaOH = Na 2 [Zn(OH) 4 ] Вывод: гидроксид цинка – кислота Итоговый вывод: гидроксид цинка – амфотерное соединение](https://fsd.multiurok.ru/html/2023/02/24/s_63f90e88e9342/img2.jpg)
Свойства гидроксида цинка
- Взаимодействие гидроксида цинка с соляной кислотой:
Zn(OH) 2 + 2HCl = ZnCl 2 + 2H 2 O
Вывод: гидроксид цинка – основание
2. Взаимодействие гидроксида цинка с гидроксидом натрия:
Zn(OH) 2 + 2NaOH = Na 2 [Zn(OH) 4 ]
Вывод: гидроксид цинка – кислота
Итоговый вывод: гидроксид цинка – амфотерное соединение

Предшественники Д. И. Менделеева
2. И. В. Дёберейнер ( немецкий химик) в 1829 г . предпринял первую значимую попытку систематизации элементов . Он заметил, что некоторые сходные по своим свойствам элементы можно объединить по три в группы, которые он назвал триадами. Триады Дёберейнера:
Li
Na
Ca
K
Sr
P
S
As
Ba
Cl
Se
Sb
Br
Te
I
М (Na) = ( 7 + 39 ) / 2 = 23

Предшественники Д. И. Менделеева
3. А. Бегье де Шанкуртуа (профессор Парижской высшей школы) в 1862 г . Предложил располагать элементы по спирали в порядке возрастания их атомных масс.
Спираль Шанкуртуа:

Предшественники Д. И. Менделеева
4. Д. Ньюлендс ( английский учёный)
в 1865 г . расположил элементы в порядке возрастания их атомных масс. Заметил, что сходство в свойствах проявляется между каждым восьмым элементом. Такую закономерность Ньюлендс назвал законом октав по аналогии с семью интервалами музыкальной гаммы. Октава Ньюлендса:
до
H
ре
ми
F
Li
Be
фа
Cl
Na
B
соль
Co Ni
K
Mg
C
ля
Al
Ca
Cu
Si
V
си
Ti
N
O
Zn
Cr
P
In
Mn
S
Fe
As
Se

Предшественники Д. И. Менделеева
5 . Л. Мейер (немецкий химик) в 1864 г. расположил химические элементы в порядке увеличения атомных масс и по валентности.
Таблица Мейера содержала только
28 элементов.
I ряд
Валентность IV
Валентность III
II ряд
Валентность II
III ряд
C
Валентность I
IV ряд
N
Si
V ряд
P
O
Валентность I
As
F
VI ряд
Li
Валентность II
S
Sn
Be
Sb
Se
Cl
Na
Pb
Br
Te
K
Mg
Bi
I
Ca
Rb
Sr
Cs
Ba
Tl

В основу периодического закона Д. И. Менделеев взял коренное свойство химического элемента- его атомный вес.
- С возрастанием атомного веса 1) металлические свойства постепенно ослабевают (Na Mg Al Si), а неметаллические усиливаются (Si, P, S, Cl) и обрываются у инертного газа (Ar);
- 2) валентность в высших оксидах возрастает от 1-го до 7-и;
- 3) валентность в летучих водородных соединениях уменьшается от 4-х до 1-го;
- 4)свойства химических элементов повторяются периодически (через 7 на 8-ой).
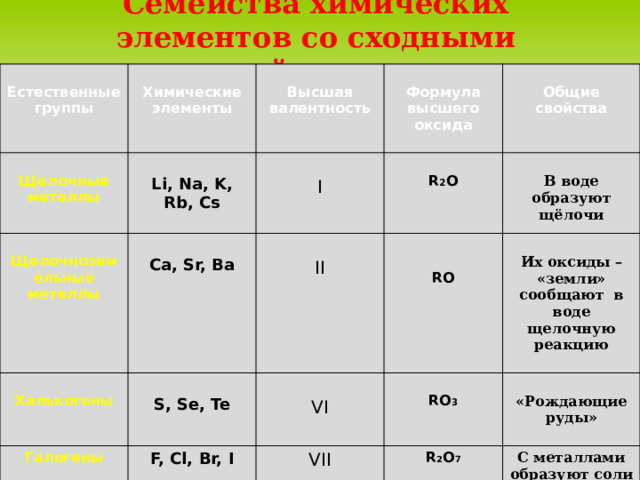
Семейства химических элементов со сходными свойствами
Естественные группы
Химические элементы
Щелочные металлы
Щелочноземельные металлы
Li, Na, K, Rb, Cs
Высшая валентность
Галогены
Халькогены
Ca, Sr, Ba
I
Формула высшего оксида
F, Cl, Br, I
Общие свойства
II
S, Se, Te
R 2 O
VII
VI
В воде образуют
RO 3
Их оксиды – «земли» сообщают в воде щелочную реакцию
RO
щёлочи
R 2 O 7
«Рождающие руды»
С металлами образуют соли

Вывод
Классификация химических элементов до
Д. И. Менделеева была не точной, не научной, не совершенной, так как за основу классификации брался не главный признак.

- Распределите по группам следующие оксиды: Na2O, CO2, P2O5, Cr2O3, ZnO, SO2, CaO, BeO, Ai2O3, CuO.
- Распределите по группам следующие оксиды: CO, Fe2O3, BaO, K2O, SiO2, Li2O, Al2O3, H2O, SO3, N2O5

Соедините прямой линией по горизонтали, вертикали или диагонали три клетки, которые содержат формулы
2 вариант
1 вариант
H 2 S
CH 4
HCl
Ca 2 SiO 3
K 2 SO 4
Na 2 SO 4
Na 2 O
H 2 O
MgF
H 2 CO 3
CH 3 OH
H 2 SO 4
Na 2 O
Na 2 SO 4
H 3 PO 4
HClO 4
H 2 SO 3
Cu(OH) 2
Соли кислородсодержащих кислот Кислородсодержащие кислоты
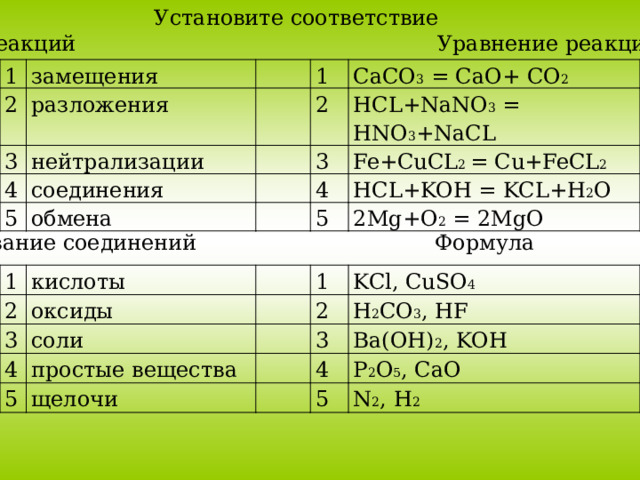
Установите соответствие
Тип реакций Уравнение реакции
1
замещения
2
3
разложения
1
4
нейтрализации
соединения
5
2
CaCO 3 = CaO+ CO 2
3
HCL+NaNO 3 = HNO 3 +NaCL
обмена
Fe+CuCL 2 = Cu+FeCL 2
4
HCL+KOH = KCL+H 2 O
5
2Mg+O 2 = 2MgO
Название соединений Формула
1
2
кислоты
3
оксиды
4
1
соли
5
простые вещества
KCl, CuSO 4
2
3
H 2 CO 3 , HF
щелочи
4
Ba(OH) 2 , KOH
P 2 O 5 , CaO
5
N 2 , H 2

Третий лишний"
Необходимо найти на каждой строке лишнюю формулу вещества и объяснить, почему именно эта формула лишняя.
1. Найти лишнюю формулу, вычеркнуть ее и назвать класс веществ:
1) Н 2 0, К 2 SO 4 , SO 2 -. . .;
2) ВаSО 4 , НС1, СuС1 2 -. . .;
3) NaОН, СuО, Сu(ОН) 2 - . . .;
4) Н 2 SО 3 , НС1, КNO 3 -. . ..
2. Найти лишнюю формулу, вычеркнуть ее и назвать класс веществ:
1) Н 2 SO 3 , LiNO 3 , Н 2 SO 4 -. . .;
2) NаОН, Ва(ОН) 2 , Н 2 S - . . . ; .
3) Nа 2 СO 3 , Р 2 O 5 , МgO -. . .;
4)А1РО 4 , СuSО 4 , Zn(ОН) 2 - . . ..

Домашнее задание
Д/з §34 упр. 1-3 ,









![Свойства гидроксида цинка Взаимодействие гидроксида цинка с соляной кислотой: Zn(OH) 2 + 2HCl = ZnCl 2 + 2H 2 O Вывод: гидроксид цинка – основание 2. Взаимодействие гидроксида цинка с гидроксидом натрия: Zn(OH) 2 + 2NaOH = Na 2 [Zn(OH) 4 ] Вывод: гидроксид цинка – кислота Итоговый вывод: гидроксид цинка – амфотерное соединение](https://fsd.multiurok.ru/html/2023/02/24/s_63f90e88e9342/img2.jpg)





























