| ЗАДАНИЕ НАПИСАТЬ КОНСПЕКТ В ТЕТРАДЬ И ВЫПОЛНИТЬ ТЕСТОВОЕ ЗАДАНИЕ Тема : Метод оксидиметрии В основе ряда методов титриметрического анализа, которые объединяются под общим названием оксидиметрия, лежат окислительно-восстановительные реакции (ОВ), т.е. реакции, протекающие с изменением степени окисления атомов химических элементов, входящих в состав реагирующих веществ. В качестве рабочих растворов (титрантов) в оксидиметрии применяют растворы окислителей и восстановителей. Классификация методов оксидиметрии. Все методы оксидиметрии классифицируют в зависимости от окислителя или восстановителя, применяемого в рабочем растворе, на следующие виды: перманганатометрия: основным титрантом служит раствор КМn04; наряду с ним обычно используются растворы сульфата железа (II) FeS04 или щавелевой кислоты Н2С2О4;  2) йодометрия: титранты - растворы йода и тиосульфата натрия Na2S203; 3) хроматометрия: основной титрант - раствор дихромата калия К2Сг207; 4) броматометрия: титрант - раствор бромата калия КВг03; 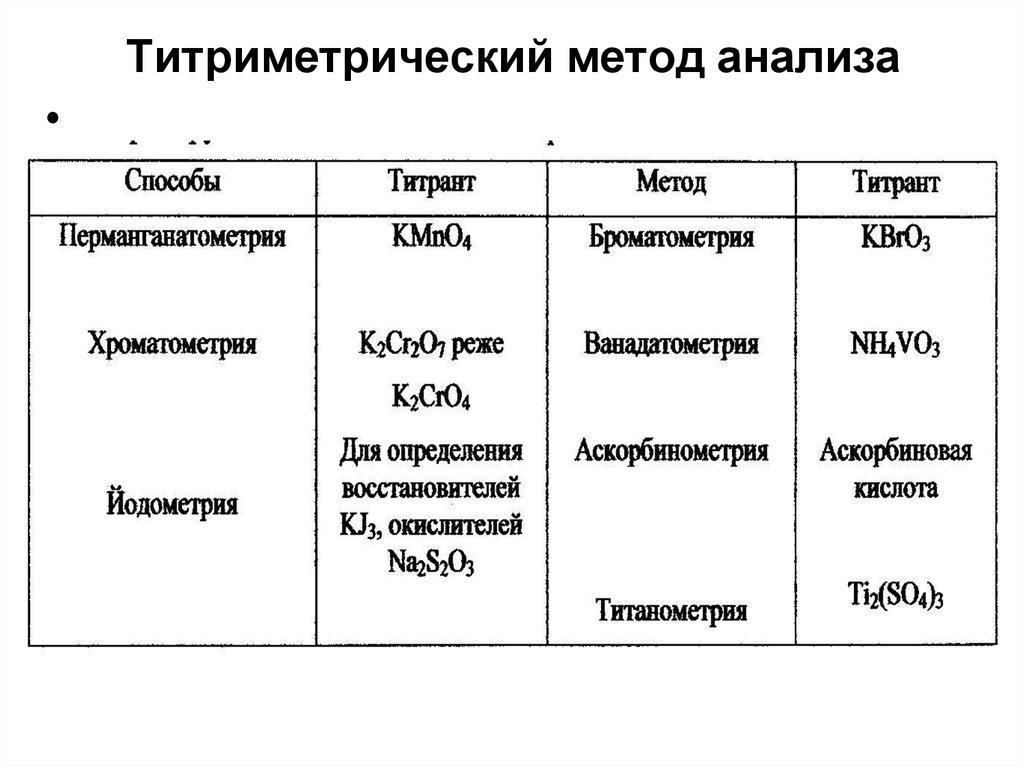 Тестовые задания по МДК 03.01.Технология выполнения химических и физико-химических методов анализа. Титриметрический анализ. Анализ веществ методом перманганатометрии. I вариант К методу оксидиметрии можно отнести: А) комплексонометрия; Б) перманганатометрия; В) броматометрия; Г) иодометрия В основе метода оксидиметрии лежат …………………………………………………(дописать ) Метод перманганатометрии основан………………………………………………………(дописать ) Индикатором в перманганатометрии служит: А) перманганат калия; Б) перманганат натрия; В) перманганат кальция; Г) марганцовка Грамм-эквивалент окислителей рассчитывают по формуле: А) Г-эквокислитель= Молекулярная масса . Количество отданых электронов
Б) Г- эквокислитель= Молекулярная масса . Количество принятых электронов В) Г- эквокислитель= Молекулярная масса . Валентность элемента Г) Г-эквокислитель= Молекулярная масса . Количество электронов Грамм-эквивалент восстановителей рассчитывают по формуле: А) Г-экввосстановитель =Молекулярная масса . Количество отданых электронов
Б) Г-экввосстановитель =Молекулярная масса . Количество принятых электронов В) Г-экввосстановитель =Молекулярная масса . Валентность элемента
Г) Г-экввосстановитель= Молекулярная масса . Количество электронов Приёмы титрования в перманганатометрии: А) прямое титрование; Б) обратное титрование; В) замещённое титрование Практически можно определить, что марганец в растворе имеет заряд (+2) если раствор окрашен: А) в красно-фиолетовый цвет; Б) в коричневый цвет; В) раствор прозрачный Практически можно определить, что марганец в растворе имеет заряд (+4) если раствор окрашен: А) в красно-фиолетовый цвет; Б) в коричневый цвет; В) раствор прозрачный Практически можно определить, что марганец в растворе имеет заряд (+7) если раствор окрашен: А) в красно-фиолетовый цвет; Б) в коричневый цвет; В) раствор прозрачный
Задание отправлять на эл.почту olga.shishkova1976@mail.ru
| 
















