Просмотр содержимого документа
«Методическая разработка. Лекционный материал по теме: "Алкены".»
Лекция. Алкены
Состав и строение молекулы:
Непредельные углеводы – это углеводороды, в молекулах которого между атомами углерода имеются кратные связи двойные или тройные.Этиленовые углеводороды (алкены) – это органические соединения, в молекулах которых между атомами углерода имеется одна двойная связь.
Общая формула:CnH2n
Гомологический ряд алкенов:
C2H4 – этен (этилен)H2C=CH2
C3H6 – пропен (пропилен)H2C=CH-CH2-CH3
C4H8 – бутен (бутилен) H2C=CH-CH2-CH3
C5H10 – пентен
C6H12 – гегсен
C7H14 – гаптен
C8H16 – октен
C9H18 – нонен
Строение молекулы алкенов:

С+62е)4е)
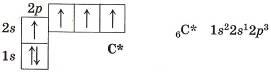
Тип гибридизации: sp2 так как каждый атом углерода связан с тремя другими атомами.
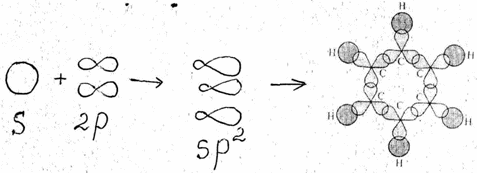
Гибридные облака перекрывают между собой и s электронными облаками атомом водорода образуя, сигма связи. p-электронные облака, не вступившие в гибридизацию перекрываются перпендикулярно сигма связи и образуют π связь.
π связь – это связь, которая образуется при перекрещивание электронных облаков перпендикулярно сигма связи.
2.Получение:
В лаборатории при нагревании этилового спирта с концентрированной H2SO4.
C2H5OH�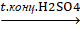 �C2H4�
�C2H4� � -HOH
� -HOH
H2SO4 – концентрированное водоотнимающие вещество.
3.Физические свойства:
Этилен – бесцветный газ, почти без запаха, немного легче воздуха, плохо растворим в воде.
От С1до С4 – газы;
От С5 до С18 – жидкости;
От С19 – твердые вещества.
4.Химические свойства:
Реакция присоединения
Качественная реакция на непредельные углеводороды
Реактив: Br2 – бромная вода.
Опыт: пропустить этилен через бромную воду.
Наблюдение: бромная вода обесцветилась, так как идет реакция присоединения.
CH2=CH2+Br2� �CH2Br-CH2Br 1,2- дибромэтан
�CH2Br-CH2Br 1,2- дибромэтан
CH2=CH2+H2� �CH3 – CH3
�CH3 – CH3
этан
C2H4+H2� �C2H6
�C2H6
правило Марковникова
Водород присоединяется к наиболее гидрогенизированному атому углерода, а атом углерода к наименее гидрогенизированному по месту двойной связи.
CH2=CH2+HBr� �CH3- CH2Br
�CH3- CH2Br
бромэтан
CH2=CH-CH3+HBr� �CH3-CHBr-CH3 2-бромпропан
�CH3-CHBr-CH3 2-бромпропан
CH2=CH-CH3+HOH� �CH3-CHOH-CH3 пропанол-2
�CH3-CHOH-CH3 пропанол-2
Реакция окисления
C2H4+3O2� �2CO2�
�2CO2� �+2H2O
�+2H2O
Качественная реакция
Реактив: раствор KMnO4
Опыт: пропустить алкен, (этилен ) через раствор KMnO4
Наблюдение:
CH2=CH2+O+HOH� �HO-CH2-CH2-OH этиленгликоль
�HO-CH2-CH2-OH этиленгликоль
III.Реакция полимеризация – это процесс соединения многих мелких молекул в одну более крупную. Полимеры - высокомолекулярные соединения.




















