Государственное бюджетное профессиональное образовательное учреждение
«Кабардино-Балкарский автомобильно-дорожный колледж»
Терский филиал
| Рассмотрен на заседании ЦМК Общеобразовательных и гуманитарных дисциплин Протокол № _02__ от _15.10__ 2025___г. Председатель _______А.С.Евазова |
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
Внеклассного мероприятия
" Все вокруг таблицы Д. И. Менделеева "
в форме круглого стола
Дата проведения
«__21__» ____ноябрь __2025г
Преподаватель Токова К.
г.п.Терек, 2025г
Круглый стол по химии: «Все вокруг таблицы Д. И. Менделеева»
Цели мероприятия:
Актуальность темы:
Периодический закон – основа современной химии. Периодическая система позволяет на основе закономерностей обобщать, делать выводы, предвидеть. Они лежат в основе решения современных задач химической науки и промышленности.
Задачи.
1.Образовательные: формировать интерес к историческому материалу великих научных открытий, показать практическое значение открытия периодического закона, расширить представления об использовании знаний одной области наук для открытия в другой области.
2.Развивающие: развивать умение работать с научно-популярной литературой, поиск материалов с использованием интернета, систематизировать и обрабатывать материал средствами ИКТ с помощью программ MICROSOFT WORD, POWERPOINT и т.д.
3.Воспитательные:
а) воспитывать коммуникативные навыки, формировать научное мировоззрение,
б) воспитывать чувство патриотизма, гордости за достижения российской науки,
в) воспитывать любовь к химии и опытам.
Форма проведения: внеклассное мероприятие по химии
Методическое оснащение внеклассного мероприятия:
1. Методическая разработка внеклассного мероприятия " Все вокруг таблицы Д. И. Менделеева "
2. Комплект вопросов для участников мероприятия, знаки химических элементов, портрет Д.И.Менделеева, кроссворд
3. Презентация по теме мероприятия.
4. Стенгазета «Д.И.Менделеев»
7. Реактивы и оборудование для проведения опытов.
Место проведения: аудитория №5
Формы работы: групповая, индивидуальная
Методы работы: Ответы на вопросы, анализ информации.
Дидактический материал: список вопросов по теме, периодическая таблица Д.И. Менделеева, стенгазета, знаки химических элементов, презентация по теме.
Лабораторное оборудование и химические реактивы.
- водные растворы веществ: гидроксида натрия, соляной, серной кислоты, этиловый спирт; нашатырный спирт;
- твёрдые вещества: активированный уголь, уголь, таблетка сухого горючего,
- химическая посуда;
-спиртовка, спички, лучинка, асбестовая сетка; пробирка, пробиркодержатель, тигельные щипцы, штатив для пробирок, коническая колба, мерный цилиндр, фарфоровая чашка, шпатель, воронка, спиртовка, асбестовая сетка, химический стакан.
Участники: студенты групп М-1/25(Т), М-2/25(Т).
Структура мероприятия:
Организационный этап: приветствие, сообщение темы, цели, установка на активную мыслительную деятельность.
1.Вступительное слово преподавателя
2.Исторические сведения об открытии периодического закон
3. Интересные факты о химических элементах (сообщения учащихся)
4. «Что в имени тебе моем» («Путешествие по таблице Менделеева»)
5. Практическая часть Подведение итогов.
Эпиграф:
«Широко распростирает химия руки свои в дела человеческие…
Куда ни посмотрим, куда не оглянемся, везде обращаются перед
нашими очами успехи её прилежания».
М.В. Ломоносов.
Ход мероприятия:
Добрый день, дорогие друзья! Я рада приветствовать вас на нашем мероприятии.
Организация деятельности студентов.
Итак, мы начинаем наше мероприятие. Для начала игры проведем разминку (предлагается ответить на вопросы):
Работаем с презентацией «Все вокруг таблицы Д.И.Менделеева».
Вступительное слово преподавателя
Мир сложен.
Он полон событий, сомнений.
И тайн бесконечных, и смелых догадок.
Как чудо Природы является гений
И в хаосе этом наводит порядок...
Весь мир большой: жара и стужа,
Планет круженье, свет зари –
Все то, что видим мы снаружи,
Законом связано внутри.
Найдется ль правило простое,
Что целый мир объединит?
Таблицу Менделеев строит,
Природы ищет алфавит!
Химия – наука удивительная. Она конкретная и касается бесчисленных полезных и вредных веществ вокруг нас и внутри нас. Поэтому химия нужна и строителю, и фермеру, и программисту, и домохозяйке. Она абстрактная и имеет дело с мельчайшими частицами, которые не разглядишь в микроскоп, со сложными формулами и на первый взгляд непонятными законами.
Периодическая система химических элементов существует в мире независимо от нас. Система химических элементов, существующая в условиях нашей планеты, возникла одновременно с образованием Земли. Она стала доступна для людей благодаря многолетним усилиям ученых многих стран — физиков и химиков. Их исследования увенчались открытием фундаментального закона природы, которому подчиняется вся система химических элементов. Это открытие произошло в 1869 г. и связано с именем нашего гениального соотечественника — Дмитрия Ивановича Менделеева.
2.Исторические сведения об открытии периодического закон (Сообщения обучающихся)
Попытки классифицировать и систематизировать известные химические элементы предпринимались задолго до Дмитрия Менделеева. Свои системы элементов предлагали такие известные ученые, как Деберейнер, Ньюлендс, Мейер и другие.
Однако из-за нехватки данных о химических элементах и их правильных атомных массах п редложенные системы были не совсем достоверными.
редложенные системы были не совсем достоверными.



По одной из легенд озарение пришло к нему за завтраком за чашкой утреннего кофе, подтверждением чему служит бумага с отпечатком кофейной кружки, написанная в день открытия периодического закона с пометками, относящимися к этой работе.
Есть еще красивая легенда о том, что свою таблицу Менделеев увидел во сне, а утром проснулся и записал ее. На самом деле, это просто миф. Сам ученый много раз говорил, что созданию и совершенствованию периодической таблицы элементов он посвятил 20 лет своей жизни: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
В каждом школьном кабинете химии вы увидите портрет Менделеева и его замечательную таблицу, сперва напоминающую обычный календарь.
Жизнь и деятельность Д.И.Менделеева
Дмитрий Иванович МЕНДЕЛЕЕВ (1834 г.р.) — гениальный русский учёный и общественный деятель. Широко известен как химик, физик, экономист, метролог, технолог, геолог, метеоролог, педагог, воздухоплаватель.
1.Сколько всего известно химических элементов?
2. Каких элементов в таблице больше, металлов или неметаллов?
3. На какие группы делятся химические элементы?
4. В каком году была открыта система химических элементов?
5. Как называются горизонтальные столбцы в таблице Менделеева?
6. Как называются вертикальные столбцы в таблице Менделеева?
7. Назовите 3 химических элемента, названные в честь планет.
8. Назовите 3 химических элемента, названные в честь стран.
9. Назовите 3 химических элемента, названные в честь учёных.
10. Назовите 2 химических элемента, названные в честь частей света.
11.Друзья Д.И.Менделеева.
12.Интересные факты из жизни Д.И.Менделеева.
13.Увлечения Д.И.Менделеева.
Какой(-ие) элемент(-ы)...:
…всегда радуются? (радий, радон)
…утверждает, что он – это не он? (неон)
…назван в честь Франции? (франций)
…назван в честь Польши? (полоний)
…назван в честь России? (рутений)
…открыт впервые на Солнце? (гелий)
…названы в честь учёных? (кюрий, менделевий, нобелий, резерфордий и т. д.)
…названы в честь планет? (уран, нептуний, плутоний)
…открыт в одном из городов Московской области и назван в честь него? (дубний)
В названии какого элемента заключено название…:
…двух животных? (мышьяк)
…волшебника? (магний)
…увеселительного заведения? (цирконий)
…настольной игры? (золото)
…напитка пиратов? (хром, бром)
…американского штата? (калифорний)
…человеческой кости? (серебро)
…цифры 3? (натрий, иттрий)
…хвойного дерева? (никель)
Назовите элемент…:
…самый распространённый на Земле (кислород)
…самый распространённый в земной атмосфере (азот)
…самый распространённый в космосе (водород)
…самый редкий из содержащихся в земной коре (астат)
…имеющий наибольшее количество аллотропных модификаций (плутоний)
…входящий в наибольшее число разнообразных соединений (углерод)
Назовите:
самый лёгкий газ (водород)
самый тяжёлый газ (радон)
самый лёгкий металл (литий)
самый тяжёлый металл (иридий, осмий)
3.Интересные факты о химических элементах
В честь учёных названы следующие химические элементы:
Гадолиний (Gd) – в честь финского химика Юхана Гадолина.
Кюрий (Cm) – в честь французского учёного, физика Пьера Кюри.
Эйнштейний (Es) – в честь немецкого физика Альберта Эйнштейна.
Фермий (Fm) – в честь физика-итальянца из Америки Энрико Ферми.
Менделевий (Md) – в честь знаменитого русского химика, автора Периодической системы химических элементов Дмитрия Ивановича Менделеева.
Нобелий (No) – в честь шведского учёного Альфреда Нобеля (название спорно, имеются и другие версии происхождения слова «нобелий»).
Лоуренсий (Lr) – в честь американского физика Эрнеста Орландо Лоуренса.
Резерфордий (Rf) – в честь британского физика новозеландского происхождения Эрнеста Резерфорда.
Сиборгий (Sg) – в честь американского физика Гленна Сиборга.
Борий (Bh) – в честь датского учёного, физика Нильса Бора.
Мейтнерий (Mt) – в честь австрийского физика Лизы Мейтнер. Точнее – Лизе Майтнер.
Рентгений (Rg) – в честь немецкого физика Вильгельма Конрада Рентгена. Правильнее – Рёнтгена.
Коперниций (Cn) – в честь польского астронома Николая Коперника.
Уран
Когда в 1896 году французский физик Анри Беккерель поместил соли урана на фотопластинку, он случайно обнаружил, что вещество радиоактивно, – и позже получил за это Нобелевскую премию. Уран – последний элемент в таблице Менделеева (номер 92), который встречается в природе. Все остальные синтезируют в лаборатории.
Золото
Специальная теория относительности Альберта Эйнштейна объясняет цвет золота. Из-за смещения уровней энергии электронов металл поглощает синий цвет, придавая отраженному свету желтый оттенок.
Ртуть
Когда путешественники Мериуэзер Льюис и Уильям Кларк в начале XIX века отправились в экспедицию к Тихому океану через всю Америку, они прихватили с собой 1300 доз ртутного слабительного (известного как «слабительное доктора Раша»). Двести лет спустя исследователи смогли точно установить, где находился лагерь путешественников в штате Монтана, благодаря следам неразлагающейся ртути.
Галлий
Менделеев оставил в первой версии Периодической таблицы пустые места, чтобы дополнить ее новыми открытиями. Первым заполненным пробелом оказался галлий (номер 31), который открыли в 1875 году. Металлический галлий (остается твердым при комнатной температуре, но плавится при температуре выше 29,7° С) стал звездой благодаря химическому трюку, в котором сделанная из него ложка тает прямо в руке или стакане чая.
Гелий
Гелий обнаружили во время исследования хромосферы Солнца в 1868 году. Это случилось за 30 лет до того, как элемент впервые нашли на Земле. А в 2018 году ученые обнаружили гелий в атмосфере экзопланеты.
Оганесон
Оганесон – последний в колонке благородных газов. Однако он не такой надменный, как соседи: в отличие от того же гелия или аргона, оганесон с готовностью отдает свои и берет чужие электроны, а его атомы могут слипаться (по крайней мере, в теории).
Интересные факты о химических элементах (сообщения учащихся)
Вот несколько интересных фактов о свойствах азота:
Жидкий азот используется в качестве средства пожаротушения. При испарении он вытесняет из очага возгорания кислород, необходимый для горения, и пожар прекращается.
Теплоёмкость азота довольно низка, поэтому невозможно моментально заморозить предмет, погрузив его в этот сжижённый газ. Любой предмет должен пробыть в ёмкости с жидким азотом какое-то время, чтобы достаточно сильно замёрзнуть.
Так как азот инертен, для его окисления требуются очень высокие температуры и, соответственно, огромная энергия. Такие условия создаются при ударах, температура которых может достигать нескольких десятков тысяч градусов.
Учёные не исключают возможности того, что где-то во Вселенной может существовать жизнь на основе азота. Подобные условия вполне могут существовать на газовых планетах, например, Нептуне, на котором азот при давлениях в миллионы атмосфер может принимать очень специфические формы.
Около 2,5% массы живых клеток растений и животных на Земле приходится на азот. По этому параметру он занимает четвёртое место, уступая лишь углероду и кислороду.
Всего существует 16 изотопов азота, но в природе встречаются лишь два из них, и оба они стабильны. В лабораторных условиях учёным удалось получить ещё 14 изотопов, причём все они радиоактивны. Скорость полураспада у них очень высока, самый стабильный из них существует всего около 10 минут.
Интересные факты о кислороде:
Кислород тяжелее воздуха. Если уравновесить на весах пустой стакан, а затем через трубку наполнить его кислородом, то равновесие нарушится.
Кислород может быть не только газообразным, но и жидким, и даже твёрдым. Жидкий кислород — подвижная, слегка голубоватая жидкость. А твёрдый кислород выглядит как кристаллы синего цвета.
Все растения планеты Земля в течение года вырабатывают около 300 миллиардов тонн кислорода.
К нехватке кислорода приводят подавленные эмоции.
Человек как биологический вид формировался, когда концентрация кислорода в атмосфере Земли достигала 38–40%.
За сутки здоровый человек в спокойном состоянии прокачивает через лёгкие 7200 л воздуха, безвозвратно забирая из атмосферы 720 л кислорода.
Содержание кислорода в современной атмосфере — 21%.
В крупных городах количество кислорода в воздухе может снижаться до 17–18%, а при неблагоприятных метеорологических условиях до 12–15%. Недостаток кислорода человек начинает ощущать уже при его снижении в атмосфере до 18%. А критическими для жизни являются 7%.
Интересные факты о свойствах водорода:
Во Вселенной водорода 88,6%. Большей частью он содержится в звёздах и межзвёздном газе.
Из-за своей лёгкости молекулы водорода двигаются с огромными скоростями, сопоставимыми со второй космической скоростью. Благодаря этому его теплопроводность превышает теплопроводность воздуха в 7,3 раза.
При давлении около 1,5–2,0 млн атм водород приобретает способность к поглощению инфракрасного излучения. Явление подтвердило способность электронных оболочек молекул вещества поляризоваться.
Предполагается, что твёрдый водород при гигантских давлениях в сотни тысяч атмосфер приобретёт металлические свойства.
Из верхних частей атмосферы молекулы водорода легко улетают в космос. Таким образом наша планета теряет 3 кг водорода каждую секунду.
Водород — важный биогенный элемент. Образует воду, содержится во всех живых тканях, в амино- и нуклеиновых кислотах, белках, липидах, жирах, углеводах.
Интересные факты об алюминии:
Чистый алюминий (без примесей) в микроскопических количествах можно найти только в жерлах вулканов.
От воздействия кислорода воздуха металл почти мгновенно покрывается прочной оксидной плёнкой, которая защищает его от коррозии.
Чистый полированный алюминий отражает до 92% видимого света и инфракрасных лучей. Благодаря отличной отражающей способности неокрашенного отполированного Al, используется для изготовления зеркал.
Изотоп под названием алюминий 26 излучает гамма радиацию и считается единственным из радиоактивных изотопов химического элемента Al.
Алюминий можно перерабатывать практически бесконечно, и при этом его свойства почти не теряются. Производство вторичного алюминия требует в 20 раз меньше энергии, чем получение металла из руды.
В организме взрослого человека содержится примерно 140 мг алюминия. В растительных продуктах этого химического элемента в 50-100 раз больше, чем в продукции животного происхождения. Так, к примеру, в яблоках его до 150 мг/кг. Источником поступления этого металл в наш организм также служит вода. В питьевой воде Al – 2-4 мг./литр.
Алюминий часто называют «крылатым металлом», так как это идеальный материал для создания летательных аппаратов. Ещё в начале ХХ века немецких химик Альфред Вильм получил лёгкий сверхпрочный сплав «дюраль», который стали применять в авиастроении.
Из высокопрочных алюминиевых сплавов изготовлены корпуса современных самолётов и многие элементы МКС.
Мелкодисперсный алюминиевый порошок применяется в качестве присадки к ракетному топливу. Ракета «Сатурн» за время полёта сжигает 36 тонн алюминиевого порошка.
Кузовы современных автомобилей часто изготавливаются из алюминиевых сплавов. Каждый килограмм Al в корпусе экономит расход топлива и позволяет увеличить скорость автомобиля. 1 кг даёт экономию больше 10 л на 2 тыс. км. Audi TT, Audi Q7, Range Rover Evoque - автомобили почти с полностью алюминиевыми кузовами.
Около 30% всех напитков в мире разливаются в алюминиевые банки. Следует знать, что обычная алюминиевая банка из-под напитка имеет один, но очень весомый недостаток – разлагается в почве примерно 80-100 лет.
Несколько интересных фактов о меди:
Латинское название меди («cuprum») происходит от названия острова Кипр, одного из первых мест, где началась выплавка этого металла.
Большая часть электрических кабелей во всём мире изготавливается именно из меди.
Медные самородки встречаются намного чаще, чем железные, несмотря на то, что железо — один из самых распространённых металлов.
Медь препятствует распространению бактерий по своей поверхности. Поэтому часто дверные ручки и тому подобные скобяные изделия делают из бронзы — она прочнее и при этом обладает схожими свойствами, так как меди в её составе много.
Медные инструменты при ударе друг о друга не могут вызвать искру, в отличие от железных.
Нередко медь добавляется в ювелирные сплавы, чтобы повысить их прочность.
Средняя норма потребления меди для взрослого человека составляет порядка 0,9 миллиграмма.
По производству и потреблению медь занимает третье место в мире, уступая лишь железу и алюминию.
В Непале медь считается чем-то вроде священного металла. Местные жители верят, что она помогает бороться с болезнями, и часто пьют воду, в которую кидают медные монеты.
Благодаря высокой коррозионной стойкости меди из неё стали изготавливать капсулы для захоронения токсичных и радиоактивных отходов.
Медь — один из металлов, который активно перерабатывается и используется повторно. В среднем в мире перерабатывается около 80% всего объёма меди.
Несколько интересных фактов о железе:
На протяжении нескольких веков больше всего железа в России добывалось в Екатеринбурге. Именно из местной железной руды изготовлена кровля Британского парламента.
Железо испаряется, если нагреть его до температуры в 2862 градуса. При этом оно становится жидким при нагреве до 1538 градусов.
Когда люди только научились добывать железо и обрабатывать его, оно стоило дороже золота.
Ещё до развития металлургии древние люди иногда находили железные самородки, зачастую метеоритного происхождения, и изготавливали из них орудия труда и оружие.
Наша кровь имеет красный цвет именно благодаря железу, которое входит в состав красных кровяных телец, переносящих кислород. У некоторых моллюсков аналогичные процессы основаны не на железе, а на меди, поэтому кровь у них голубого цвета.
На железо приходится около 4,65% всей массы земной коры.
В организме среднестатистического взрослого человека содержится около 5 грамм железа.
Из распространённых продуктов больше всего железа содержится в гранатах, яблоках, шоколаде, некоторых бобовых, а также в свиной и говяжьей печени.
Самый большой кусок чистого железа, когда-либо обнаруженный, весит 66 тонн. Это всё, что осталось от метеорита, некогда упавшего на африканскую страну Намибия.
Серная и азотная кислоты способны полностью растворить железо.
Именно из железа изготавливают магниты, как обычные, так и электрические.
Несколько интересных фактов о золоте:
Первая добыча золота велась в Болгарии ещё в каменном веке. Археологи нашли доказательства, что именно золото стало первым металлом, добытым человеком в 4000 г. до н. э..
На океанском дне покоится более десяти миллиардов тонн золота. Это как чистые залежи металла, так и утопленные вместе с кораблями хранилища.
Учёные выяснили, что в космосе есть несколько околоземных астероидов, которые содержат платину и золото. Их запасы могут быть значительно выше, чем объём всего добытого золота на земном шаре (за всю историю человечества).
Золото настолько пластично, что из него можно выковать полупрозрачные листы толщиной всего в 100 нанометров, или нити для шитья.
Металл демонстрирует светоотражательную способность. Он может отражать даже инфракрасное излучение.
Золото используют при изготовлении микросхем. У него высокий показатель теплопроводности и низкий показатель сопротивления.
В ядре Земли тоже есть огромные запасы золота. Ими можно покрыть всю поверхность планеты.
Золото невозможно растворить. Оно отличается стойкостью к химическому воздействию. Единственное, на что металл может отреагировать, — это на смесь из соляной и азотной кислот.
Знаете ли Вы, что?
Всего же за последние 50 лет Периодическая таблица Д.И.Менделеева пополнилась 17-ю новыми элементами (с 102-го по 118-й), 9 из которых были синтезированы в Объединенном институте ядерных исследований в подмосковном Дубне. 2 декабря 2016 года было добавлено сразу четыре новых элемента: нихоний (элемент №113), московий (элемент №115), тенессин (элемент №117) и оганесон (элемент №118).
Три элемента получили свои названия в честь городов или государств, в которых их удалось получить, а оганесон был назван в честь российского физика-ядерщика Юрия Оганесяна за его вклад в получение этого элемента.
Почти все названия элементов имеют какой-то смысл. Как правило, названия элементов относятся к одной из пяти основных категорий. Первая – это имена известных учёных, классический вариант – эйнштейний. Кроме того, элементы могут получить свои имена в зависимости от тех мест, где они были впервые зарегистрированы, например, германий, америций, галлий и т. д. Используются и названия планет. Элемент уран был впервые обнаружен вскоре после того, как была открыта планета Уран. Элементы могут носить имена, связанные с мифологией, например, существует титан, названный так в честь древнегреческих титанов, и торий, названный по имени скандинавского бога-громовержца. И, наконец, есть названия, описывающие свойства элементов. Аргон происходит от греческого слова «аргос», что означает «ленивый» или «медленный». Из названия следует предположение, что этот газ не отличается активностью. Бром – это ещё один элемент, название которого происходит от греческого слова. «Бромос» означает «зловоние», и это довольно точно описывает запах брома.
Мы классифицировали аргон как самый «ленивый» и «медленный» элемент в истории нашей вселенной. Похоже, что Менделеевым овладели такие же чувства. Когда в 1894 году впервые удалось получить чистый аргон, он не вписывался ни в один из столбцов таблицы, поэтому, вместо того чтобы заняться поисками решения, учёный решил просто отрицать его существование.
Ещё более поразительно, что аргон был не единственным элементом, который изначально постигла эта судьба. Помимо аргона, без классификации остались ещё пять других элементов. Это коснулось радона, неона, криптона, гелия и ксенона – и все отрицали их существование просто потому, что Менделеев не смог найти для них места в таблице. После нескольких лет перегруппировки и переклассификации этим элементам (названных инертными газами) всё-таки посчастливилось присоединиться к достойному клубу признанных реально существующими.
Элемент 115 живет меньше секунды. Большинство изотопов сверхтяжелых элементов (элементов с порядковым номером 100) являются нестабильными и подвергаются распадам в течение очень короткого промежутка времени. Так, недавно открытый унунпентий, также известный как элемент 115 и эка-висмут, имеет период полураспада всего около 220-ти миллисекунд.
Менделеев предсказал существование элементов, которые еще предстояло открыть. Одной из важных особенностей, которая делает периодическую таблицу выдающимся открытием, является ее предсказательная сила. В таблице на момент ее появления оставались пустые ячейки для элементов, которые, согласно предположениям Менделеева, должны существовать, но еще не были открыты. К примеру, свойства галлия, скандия и магния Менделеев описал еще до их открытия.
Как вы, возможно, уже знаете, на сегодняшний день в периодической таблице присутствует 118 элементов. Можете ли вы догадаться, сколько элементов из этих 118 были получены лабораторным путём? Из всего общего списка в природных условиях можно найти лишь 90 элементов , а 28 - искусственно созданы. Их синтезируют, начиная с 1937 года, и учёные продолжают это делать и сейчас. Все эти элементы вы можете найти в таблице. Посмотрите на элементы с 95 по 118, все эти элементы отсутствуют на нашей планете и были синтезированы в лабораториях. То же касается и элементов под номерами 43, 61, 85 и 87.
3 .«Что в имени тебе моем» ( «Путешествие по таблице Менделеева»)
Другого ничего в природе нет
Ни здесь, ни там, в космических глубинах,
Все: от песчинок малых до планет –
Из элементов состоит единых.
1. В названия каких химических элементов входят названия животных?
(Мышьяк – мышь, як.)
2. Отбросив в названии элемента восьмой группы первую и последнюю буквы, получите название скошенной и высушенной травы.
(Ксенон – сено.)
3. Добавьте одну букву в название элемента шестой группы и получите название парнокопытного животного.
(Сера – серна)
4. Заменив одну букву в названии химического элемента семейства актиноидов на другую, получите название летучей мыши с большими ушами.
(Уран – ушан)
5. Название какого химического элемента не соответствует его роли в живой природе?
(Азот – «безжизненный»)
6. В названии какого химического элемента входит название дерева?
(Никель – ель)
7. Назовите химический элемент, название которого совпадает с названием соснового леса? (Бор)
8. Переставьте буквы в названии элемента восьмой группы таким образом, чтобы получилось название леса из молодых ёлочек.
(Никель – ельник)
8. В название какого важнейшего для жизни растений соединения, обусловливающего их окраску в зелёный цвет, входит название химического элемента?
(Хлор – хлорофилл)
9. Измените лишь букву в названии элемента четвертой группы и получите название представителя важнейшего класса органических соединений, широко распространённых в природе и являющихся главным источником энергии в организмах.
(Углерод – углевод)
10. В названия каких структурных элементов ядра клетки, содержащих ДНК, входит название химического элемента?
(Хром – хромосомы)
11. Отбросьте две первые буквы в названии химического элемента первой группы и получите название дугообразно загнутой кости, входящей в состав грудной клетки.
(Серебро – ребро)
12. Заменив последнюю букву в названии химического элемента четвёртого периода на другую, получите название органов человека и животных, вырабатывающих специфические вещества участвующие в различных биохимических процессах.
(Железо – железа)
13. Изменив лишь одну букву в названии элемента семейства галогенов, получите фамилию известного немецкого зоолога и путешественника, автора многотомного труда «Жизнь животных».
(Бром – Брем)
14. Отбросив первые три буквы в названии химического элемента семейства лантаноидов, получите название сильного наркотика, используемого в медицине как болеутоляющее средство.
(Европий – опий)
15. Название какой аквариумной рыбки идентично названию химического элемента.
(Неон)
16. Какой химический элемент был открыт в продуктах выщелачивания пепла морских водорослей?
(Иод)
17. Какой металл может «болеть чумой»?
(Олово)
18. Недостаток какого элемента в организме человека приводит к кариесу зубов?
(Фтор)
19.В честь какого химического элемента названа Аргентина?
(Серебро. От латинского наименования элемента Argentum.)
20.С названием какого химического элемента созвучно название земной коры?
(Литий – литосфера, от греч. lithos – камень)
21.Какой химический элемент объединяет Норвегию, Швецию и Финляндию?
(Скандий – Скандинавский полуостров, на котором находятся эти страны.)
22.Название какого химического элемента из группы актиноидов происходит от названия части света?
(Америций – Америка)
23.Как называется химический элемент, одноименный с городом Мурманской области?
(Никель)
24.В названии столицы Эстонии измените две последние буквы на одну, и вы получите название химического элемента девятого ряда периодической системы Д.И.Менделеева.
(г.Таллинн – таллий)
25.Отгадайте химический элемент из группы актиноидов, название которого совпадает с названием планеты.
(Уран.)
26.Невнимательный химик хотел написать название химического элемента пятой группы, а получилось название портового города Ростовской области.
(Азот – г.Азов)
27.между Черным и Мраморным морями, а получилось название химического элемента третьего периода.
(Босфор — Фосфор)
28.Шутливый вопрос. Каким химическим элементом можно чистить обувь?
(Кремний – крем)
29.Какой химический элемент находится в градуснике?
(Ртуть)
30.Из какого «химического элемента» можно сшить сапоги?
(Из хрома)
«Химический кроссворд»
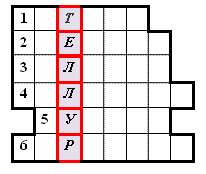
1. Элемент, входящий в состав поваренной соли (Натрий).
2. Основной элемент земной мантии (Кремний).
3. Химический элемент, образующий известковые породы (Кальций).
4. Металл, извлекаемый из руд с помощью бактерий (Молибден).
5. Металл, также извлекаемый из руд с помощью бактерий (Сурьма).
6. Элемент, входящий в состав океанических базальтов (Марганец).
Практическая часть
1.Химические свойства цинка (взаимодействие с соляной кислотой и гидроксидом натрия),
2.химические свойства углерода (взаимодействие активированного угля с чернилами и горение)
Заключительное слово преподавателя.
Пусть зимний день с метелями.
Не навевает грусть –
Таблицу Менделеева
Я знаю наизусть.
Зачем ее я выучил?
Могу сказать зачем.
В ней стройность и величие
Любимейших поэм.
Без многословья книжного.
В ней смысла торжество.
И элемента лишнего.
В ней нет ни одного.
В ней пробужденье дерева.
И вешних льдинок хруст.
Таблицу Менделеева
Я знаю наизусть. (А. Чивилихин)
Без химии жизни, поверьте, нет,
Без химии стал бы тусклым весь свет.
С химией ездим, живем и летаем,
В разных точках Земли обитаем,
Чистим, стираем, пятна выводим,
Едим, спим, и с прическами ходим.
Химией лечимся, клеим и шьем
С химией мы бок обок живем!
Так что вы без нее пропадете,
Если значение ее не поймете!
А чтобы больше и лучше все знать,
Надо химию понять.
Значение периодического закона заключено в словах А.Е. Ферсмана:
«Будут появляться, и умирать новые теории, блестящие сообщения будут сменять наши понятия, величайшие открытия будут сводить на нет прошлые и открывать невиданные по новизне и широте горизонты - все это будет приходить, и уходить, Периодический закон Д.И. Менделеева будет всегда жить, развиваться и совершенствоваться».
Используемая литература и информационные ресурсы:
Макареня А.А., Рысев Ю.В. Д.И.Менделеев: Кн. для учащихся. – 2-е изд., перераб. – М., Просвещение, 2023.
Соловьев Ю.И. и др. История химии. Развитие основных направлений современной химии. Пособие для учителей. М., Просвещение,2024.
Трифонов Д.Н., Трифонов В.Д. Как были открыты химические элементы: Пособие для учащихся – М., Просвещение,2023.
Материал в ресурсах ИНТЕРНЕТ
http://slovo.mosmetod.ru/2019/03/01/triumf-russkoj-himicheskoj-nauki/







 редложенные системы были не совсем достоверными.
редложенные системы были не совсем достоверными.














