

F
Фтор
Cl
Хлор
Br
Бром
I
Иод
At
Астат
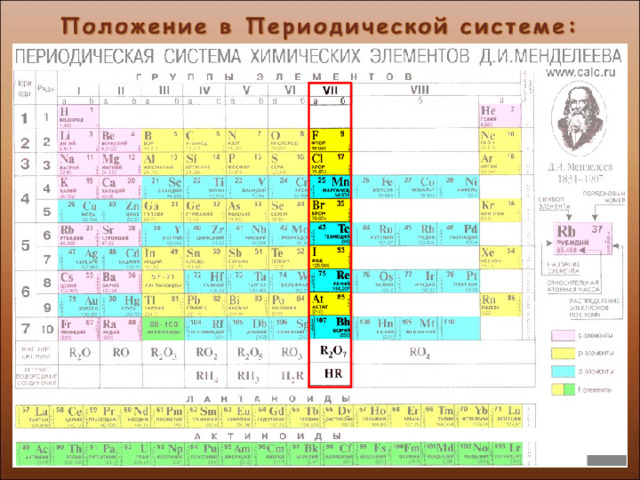
ГАЛОГЕНЫ
(от греческого
halos - соль
genes-рождающий, рождённый)
VII группа,
Главная подгруппа
![Число валентных электронов 2s 2 2p 5 3s 2 3p 5 4s 2 4p 5 5s 2 5p 5 6s 2 6p 5 Элемент F Ar Cl 19 Число электронных слоев Br 35,5 ) ) R атома I 80 ) ) ) Число валентных электронов 127 At ) ) ) ) НеМеталсвойства [210] ) ) ) ) ) Окисл. свойства ) ) ) ) ) ) Элемент F Ar 19 Число электронных слоев Cl R атома 35,5 Br 80 I Число валентных электронов At 127 НеМетал свойства [210] Окисл. свойства Элемент Ar F Число электронных слоев Cl Br R атома Число валентных электронов I At НеМеталсвойства Окисл. свойства](https://static.multiurok.ru/multiurok/html/2021/03/10/s_6048ad8c8f4d1/img3.jpg)
Число валентных электронов
2s 2 2p 5
3s 2 3p 5
4s 2 4p 5
5s 2 5p 5
6s 2 6p 5
Элемент
F
Ar
Cl
19
Число электронных слоев
Br
35,5
) )
R атома
I
80
) ) )
Число валентных электронов
127
At
) ) ) )
НеМеталсвойства
[210]
) ) ) ) )
Окисл.
свойства
) ) ) ) ) )
Элемент
F
Ar
19
Число электронных слоев
Cl
R атома
35,5
Br
80
I
Число валентных электронов
At
127
НеМетал свойства
[210]
Окисл.
свойства
Элемент
Ar
F
Число электронных слоев
Cl
Br
R атома
Число валентных электронов
I
At
НеМеталсвойства
Окисл.
свойства
Cl
+
Cl
Cl
Cl
Cl
Cl
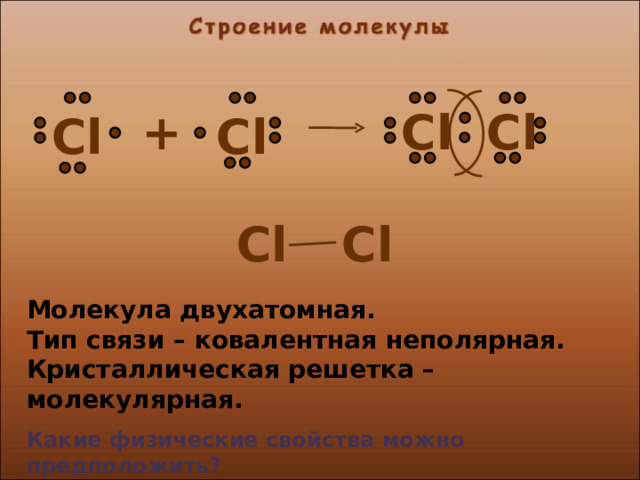
Молекула двухатомная.
Тип связи – ковалентная неполярная.
Кристаллическая решетка – молекулярная.
Какие физические свойства можно предположить?
5

5

5

5

5

5
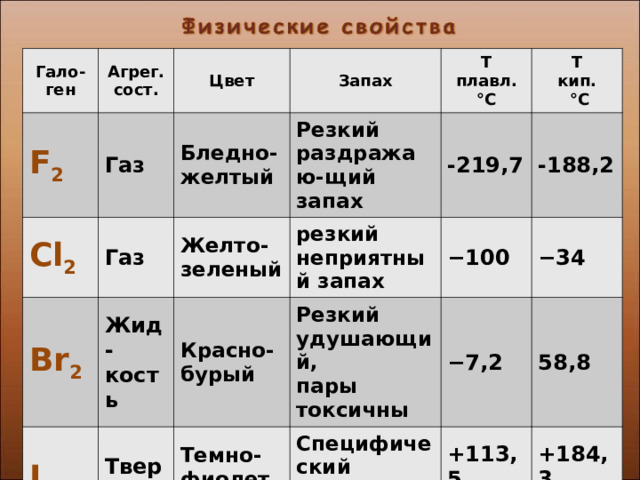
Гало-ген
Агрег. сост.
F 2
Газ
Цвет
Cl 2
Газ
Бледно-желтый
Br 2
Запах
Резкий раздражаю-щий запах
I 2
T
плавл.
°C
Желто-зеленый
Жид-кость
Красно-бурый
Твер-дое
резкий неприятный запах
-219,7
T
кип.
°C
− 100
Резкий удушающий,
пары токсичны
Темно-фиолето-вый
-188,2
− 7,2
Специфический резкий запах
− 34
+113,5
58,8
+184,3

At 2
12

F 2
13

Cl 2
14

Cl 2
15

Br 2
I 2
Бром и иод добывают из природных вод.
Источник иода – морские
водоросли –
ламинарии.
16

1. Взаимодействие с металлами.
2. Взаимодействие с водородом.
3. Взаимодействие с водой.
4. Взаимодействие со сложными веществами.
17

1. Взаимодействие с металлами.
При взаимодействии галогенов с металлами образуются соли – галогениды.
Zn + F 2 = ZnF 2 фторид цинка
2 Fe + 3 Cl 2 − 2 FeCl 3
Fe + Cl 2 − FeCl 3 хлорид железа
2 Al + 3 Br 2 − 2 AlBr 3
Al + Br 2 − AlBr 3 бромид алюминия
2 Al + 3 I 2 − 2 AlI 3
Al + I 2 − AlI 3 иодид алюминия
18

2. Взаимодействие с водородом.
При взаимодействии галогенов с водородом образуются галогеноводороды (при растворении в воде галогеноводороды образуют кислоты)
H 2 + F 2 − 2 HF
H 2 + Cl 2 − 2 HCl
фтороводород (со взрывом)
хлороводород (со взрывом при
ярком солнечном освещении)
H 2 + Br 2 − 2 HBr
бромоводород (при нагревании)
H 2 + I 2 − 2 HI
иодоводород (при нагревании,
медленно)
H 2 + F 2 − HF
H 2 + Cl 2 − HCl
фтороводород (со взрывом)
хлороводород (со взрывом при
ярком солнечном освещении)
H 2 + Br 2 − HBr
H 2 + I 2 − HI
бромоводород (при нагревании)
иодоводород (при нагревании,
медленно)

F 2 особо !
3. Взаимодействие с водой.
Cl 2 , Br 2 , I 2 взаимодействуют по схеме:
Г al 2 + H 2 O = H Г al О + НГ al
Cl 2 + H 2 O = HClO + HCl ( хлороводородная кислота)
(хлорноватистая кислота)
Вода горит во фторе:
F 2 + H 2 O − HF + O 2
2 F 2 + 2 H 2 O = 4 HF + O 2
20
 Cl 2 Br 2 I 2 активность уменьшается К Br + Cl 2 − KCl + Br 2 2 К Br + Cl 2 − 2 KCl + Br 2 21 " width="640"
Cl 2 Br 2 I 2 активность уменьшается К Br + Cl 2 − KCl + Br 2 2 К Br + Cl 2 − 2 KCl + Br 2 21 " width="640"
4. Взаимодействие со сложными веществами.
Более активный галоген вытесняет менее активный из
растворов солей.
F 2 Cl 2 Br 2 I 2 активность уменьшается
К Br + Cl 2 − KCl + Br 2
2 К Br + Cl 2 − 2 KCl + Br 2
21
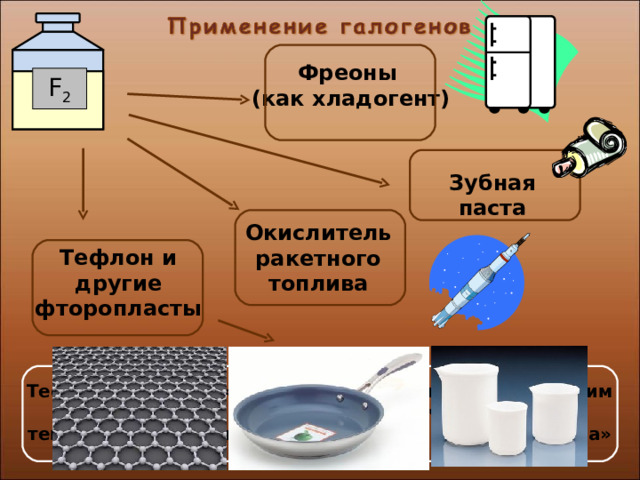
Фреоны
(как хладогент)
F 2
Зубная паста
Окислитель ракетного топлива
Тефлон и другие фторопласты
Тефлон называют «органической платиной». Перед ним бессильны расплавленные щелочи, высокие температуры, сильные кислоты, даже «Царская водка»
22
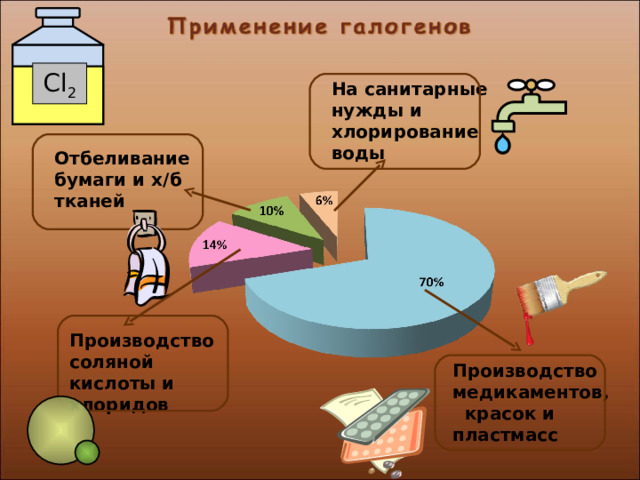
Cl 2
На санитарные нужды и хлорирование воды
Отбеливание бумаги и х/б тканей
Производство соляной кислоты и хлоридов
Производство медикаментов, красок и пластмасс
23
Br 2
Лекарственные вещества
В фотографии
Ингибиторы воспламенения
24
I 2
Лекарственные препараты
Цветная фотография
Глубокая очистка металлов
Галогеновые лампы
25

Фтор находится в организме во всех органах и тканях.
F 2
Но наибольшее его количество содержится в зубах, костях, волосах и ногтях.
Кости – своеобразное «депо» фтора.
Недостаток фтора – один из факторов, вызывающих болезнь зубов – кариес.
26
В организме человека присутствует около 95 г хлора.
Cl 2
Хлор поддерживает давление плазмы крови, лимфы, сохраняя баланс воды в организме.
Он участвует в образовании соляной кислоты, обмене веществ.
27

Содержание брома в организме человека (масса тела 70 кг) составляет 260 мг.
Br 2
Бром находится в крови, мозге, печени, почках. Больше всего его в мозге человека.
Препараты брома применяют при заболеваниях нервной системы: истерии, неврастении и других неврозах.
28
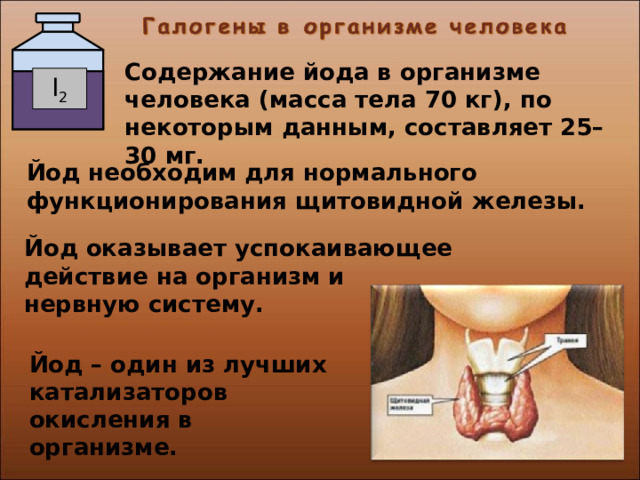
Содержание йода в организме человека (масса тела 70 кг), по некоторым данным, составляет 25–30 мг.
I 2
Йод необходим для нормального функционирования щитовидной железы.
Йод оказывает успокаивающее действие на организм и нервную систему.
Йод – один из лучших катализаторов окисления в организме.
29










![Число валентных электронов 2s 2 2p 5 3s 2 3p 5 4s 2 4p 5 5s 2 5p 5 6s 2 6p 5 Элемент F Ar Cl 19 Число электронных слоев Br 35,5 ) ) R атома I 80 ) ) ) Число валентных электронов 127 At ) ) ) ) НеМеталсвойства [210] ) ) ) ) ) Окисл. свойства ) ) ) ) ) ) Элемент F Ar 19 Число электронных слоев Cl R атома 35,5 Br 80 I Число валентных электронов At 127 НеМетал свойства [210] Окисл. свойства Элемент Ar F Число электронных слоев Cl Br R атома Число валентных электронов I At НеМеталсвойства Окисл. свойства](https://static.multiurok.ru/multiurok/html/2021/03/10/s_6048ad8c8f4d1/img3.jpg)
















 Cl 2 Br 2 I 2 активность уменьшается К Br + Cl 2 − KCl + Br 2 2 К Br + Cl 2 − 2 KCl + Br 2 21 " width="640"
Cl 2 Br 2 I 2 активность уменьшается К Br + Cl 2 − KCl + Br 2 2 К Br + Cl 2 − 2 KCl + Br 2 21 " width="640"


















