Просмотр содержимого документа
«Общая характеристика галогенов»


Открытие галогенов
- Фтор в свободном виде получил впервые в 1866 г. французский химик Анри Муассан, лауреат Нобелевской премии. Свое название элемент получил от греч. фторос – разрушающий.
- Хлор открыт шведским химиком К. Шееле в 1774 г. Элемент получил название за свой цвет ( от греч. хлорос – желто - зеленый).
- Бром открыт в 1826 г. французским химиком А. Баларом. Элемент назван так за свой запах (греч. бромос – зловонный).
- Йод получен в 1811 г. французским ученым Б. Куртуа, а название получил за цвет своих паров (греч. иодэс – фиолетовый).

Нахождение в природе
Из-за высокой химической активности галогены в природе в свободном виде не встречаются .
Соединения галогенов
CaF 2 плавиковый шпат
NaCI•KCI сильвинит
NaCI каменная соль
KIO 3 , KIO 4 в залежах селитры, в морских растениях

ОБЩАЯ ХАРАКТЕРИСТИКА ГАЛОГЕНОВ
Галогены – это естественная группа элементов , расположенных в главной подгруппе VII группы .
- Ф тор ( F), хлор(Cl), бром (Br), йод (I), астат (At)
- Галогены имеют степень окисления + 1 ,+3,+5,+7, - 1
- У фтора только -1
- В природе наиболее распространён - хлор. Астат получен искусственным путём.
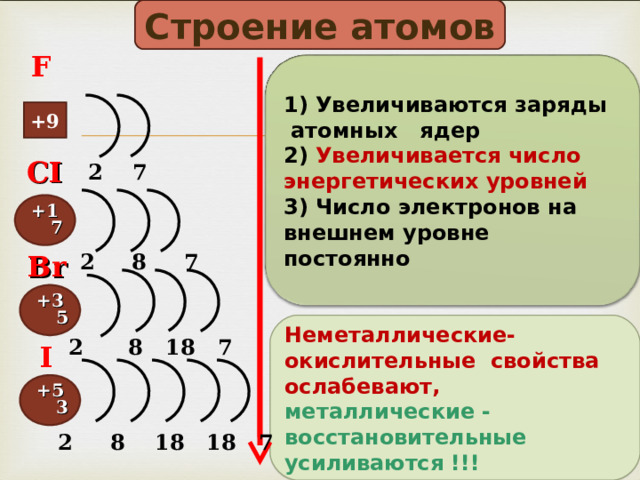
Строение атомов
F
1) Увеличиваются заряды атомных ядер
2) Увеличивается число энергетических уровней
3) Число электронов на внешнем уровне постоянно
+9
CI
2 7
+17
Br
2 8 7
+35
Неметаллические-окислительные свойства ослабевают,
металлические -восстановительные усиливаются !!!
2 8 18 7
I
+53
2 8 18 18 7
5

Электронные формулы
F
1S 2 2S 2 2P 5
2
5
S P
CI
1S 2 2S 2 2P 6 3S 2 3P 5
Br
Вывод :
галогены - р - элементы
На внешнем энергетическом
уровне 7 электронов, один из них неспаренный .
… 4S 2 4P 5
I
… 5S 2 5P 5

CI 2
Br 2
Простые
вещества
F 2
I 2

?
Химическая связь
..
..
..
..
.
.
:Г + Г: → :Г(:) Г:
..
..
..
..
Ковалентная неполярная
Кристаллическая решетка
молекулярная
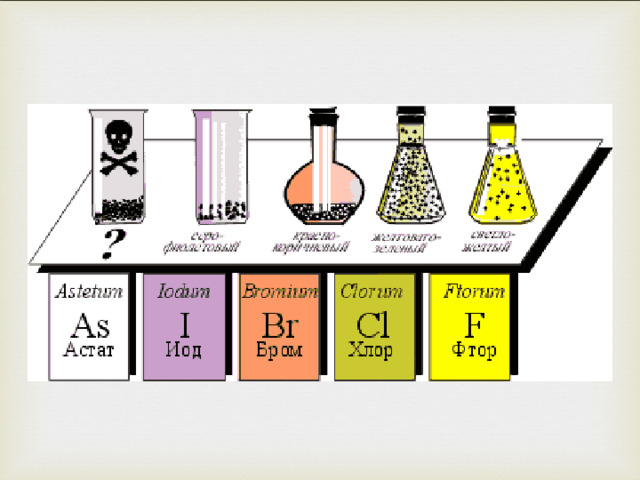
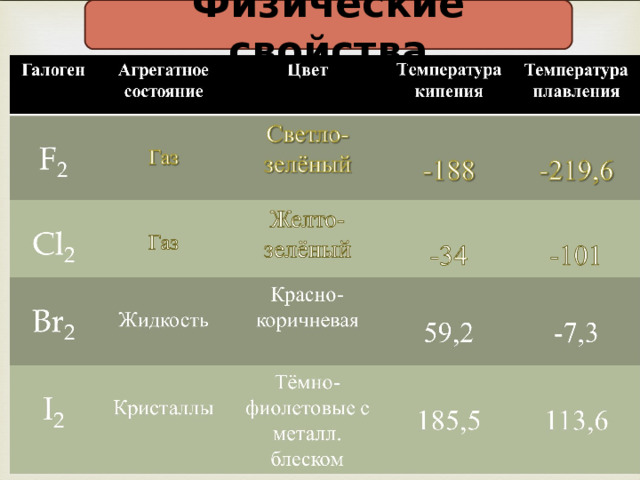
Физические свойства

- Переход из твердого состояния в газообразное, минуя жидкое состояние

Химические свойства
1.Взаимодействие с металлами
+ -
2 Na 0 + CI 2 0 = 2 NaCI
CI 2 0 окислитель
Получаются соли: фториды, хлориды, бромиды, йодиды .

Что является окислителем?

2 . Взаимодействие с водородом
Н 2 0 + Г 2 0 = 2Н + Г -
Н 2 0 + F 2 0 = 2Н F
Н 2 0 + CI 2 0 = 2Н CI
Н 2 0 + Br 2 0 = 2Н Br
Н 2 0 + I 2 0 = 2Н I

3 . Взаимодействие с водой
CI 2 + H 2 O = HCI + HCIO
Хлорноватистая кислота
Соляная кислота
2 F 2 + 2Н 2 О = 4 Н F + О 2
Плавиковая кислота

4 . Взаимодействие с растворами солей
галогенов:
CI 2
F 2
Br 2
I 2
CI 2 + 2Na Br = 2 NaCl + Br 2
CI 2 + 2Na I = 2 NaCl + I 2
Br 2 + 2Na I = 2 NaBr + I 2

Применение галогенов
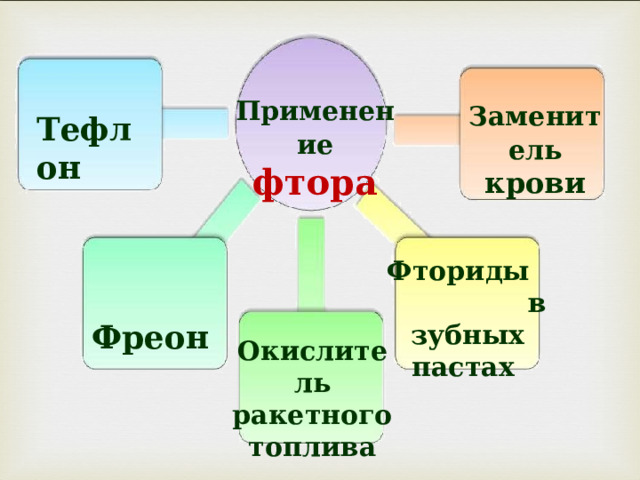
Применение фтора
Заменитель крови
Тефлон
Фториды в зубных пастах
Фреон
Окислитель ракетного топлива
14
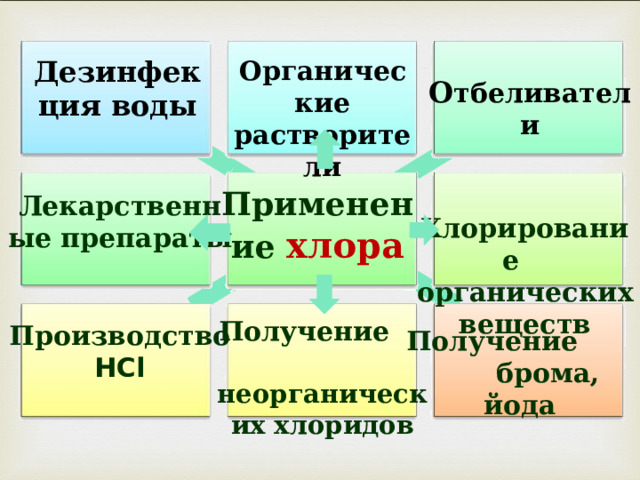
Органические растворители
Дезинфекция воды
О тбеливатели
Хлорирование органических веществ
Применение хлора
Лекарственные препараты
Получение неорганических хлоридов
Производство
HCl
Получение брома, йода
14

Лекарственные препараты
Дезинфекция одежды
Применение йода
Красители
Фотография
Электролампы
14

Домашнее задание
§19 ,
РТ: стр. 116-117
Часть II зад. 1-8






































