

- Век медный, бронзовый, железный
- Нахождение металлов в природе
- Положение металлов в ПСХЭ Д.И. Менделеева
- Физические свойства
- Получение металлов
- Сплавы
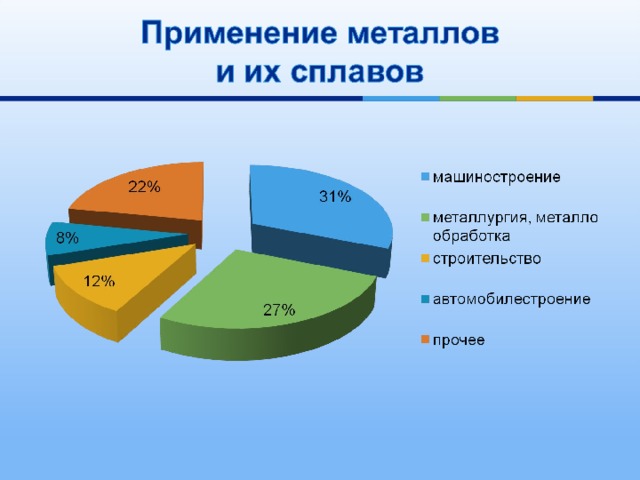
- Применение


(от лат. metallum — шахта, рудник) вещества, обладающие высокой электропроводностью и теплопроводностью,
ковкостью, пластичностью
и металлическим блеском.

Металл -
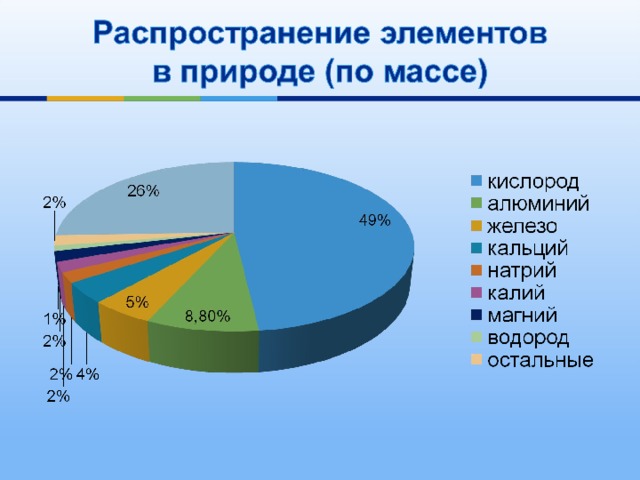
один из самых распространённых материалов,
используемых цивилизацией на протяжении практически всей её истории.

Египетские
пирамиды
Колосс
Родосский
Висячие сады
Семирамиды
Мавзолей в
Галикарнасе
Статуя
Зевса Олимпийского
Александрийский
маяк.
Храм
Артемиды Эфесской
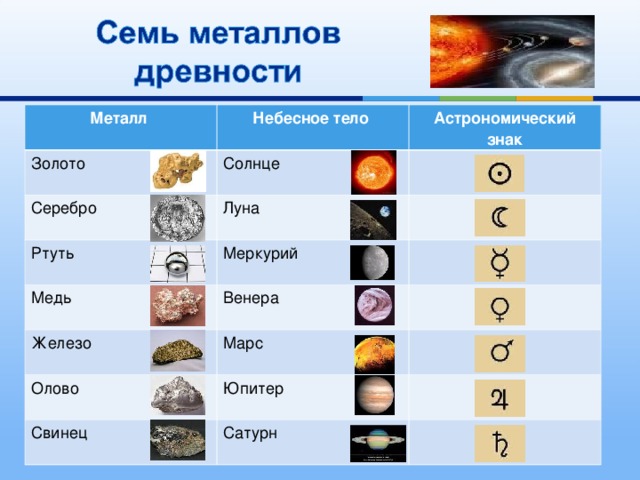
Металл
Небесное тело
Золото
Солнце
Серебро
Астрономический знак
Луна
Ртуть
Меркурий
Медь
Венера
Железо
Олово
Марс
Юпитер
Свинец
Сатурн
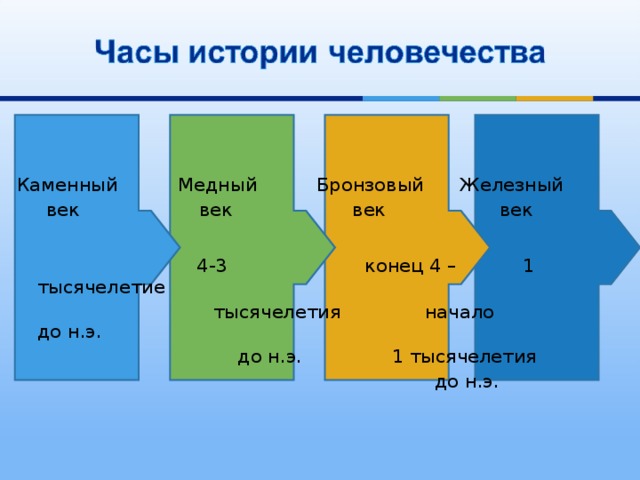
Каменный Медный Бронзовый Железный
век век век век
4-3 конец 4 – 1 тысячелетие
тысячелетия начало до н.э.
до н.э. 1 тысячелетия
до н.э.

Украшения
из меди
Предметы
домашней
утвари
Древние монеты

Предметы
домашней утвари
Оружие

Бронзовые творения
Колосс Родосский
(32 метра) Древний порт Родос)
Царь-колокол
(Московский Кремль)
Царь-пушка
(Московский Кремль)

Орудия труда
Железная посуда
Украшения

«Рабочий и колхозница» (нержавеющая сталь)
Решетка ограды
Летнего сада

Паллада
Церера

- «стальной характер»
- «железные нервы»
- «золотое сердце»
- «металлический голос»
- «свинцовый кулак»
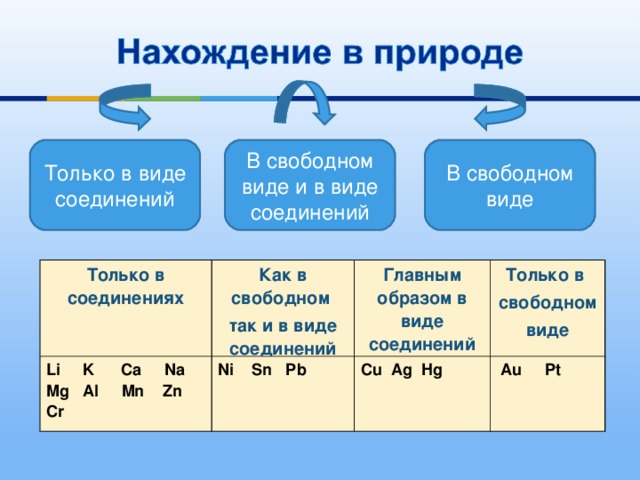
Только в виде соединений
В свободном виде и в виде соединений
В свободном виде
Только в соединениях
Как в свободном
так и в виде соединений
Li K Ca Na Mg Al Mn Zn Cr
Главным образом в виде соединений
Ni Sn Pb
Только в
свободном
виде
Cu Ag Hg
Au Pt

Хлориды
Ортофосфаты
Нитраты
Поваре нн ая соль
(хлорид натрия)
Апатит
(фосфат кальция)
Нитрат калия

Сульфаты
Глауберова соль
(кристаллогидрат
сульфата натрия)
Гипс
(кристаллогидрат
сульфата кальция)
Барит
(сульфат бария)

Карбонаты
Силикаты
Серафинит
(алюмосиликат магния)
Поташ
(карбонат
калия)
Мрамор (карбонат кальция)
Лазурит
(алюмосиликат натрия)

Оксиды
Хромит
(сложный оксид
хрома и железа)
Магнетит и гематит
(оксид железа)

Сульфиды
Гринокит
(сульфид кадмия)
Пирит
(серный колчедан
сульфид железа)
Сфалерит
(цинковая обманка
сульфид цинка)

Самородок
золота
Самородок
платины
Самородок серебра
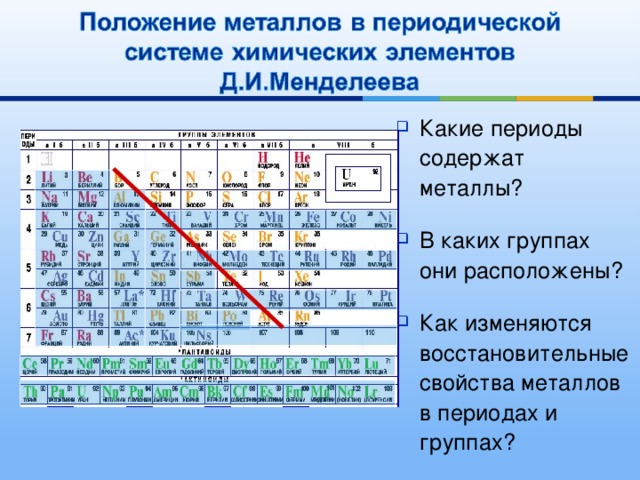
- Какие периоды содержат металлы?
- В каких группах они расположены?
- Как изменяются восстановительные свойства металлов в периодах и группах?
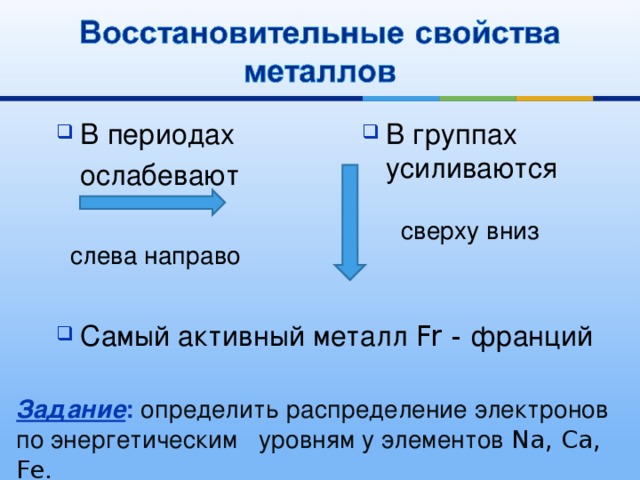
ослабевают
сверху вниз
слева направо
- Самый активный металл Fr - франций
Задание : определить распределение электронов по энергетическим уровням у элементов Na, Ca, Fe.
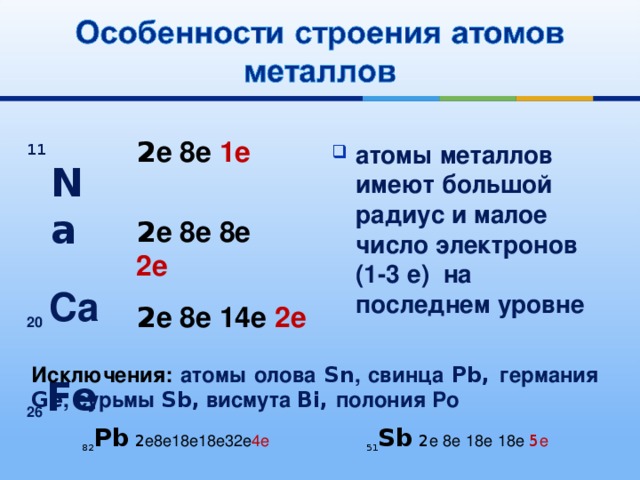
11 Na
20 Са
26 Fe
2 е 8е 1е
- атомы металлов имеют большой радиус и малое число электронов (1-3 е) на последнем уровне
2 е 8е 8е 2е
2 е 8е 14е 2е
Исключения: атомы олова Sn , свинца Pb, германия Ge , сурьмы Sb, висмута Bi, полония Ро
82 Pb 2 е8е18е18е32е 4е 51 Sb 2 е 8е 18е 18е 5 е


3 Li 2 е 1е
19 K 2 е 8e 8e 1е
12 Mg 2 е 8e 2 е
13 Al 2 е 8e 3 е
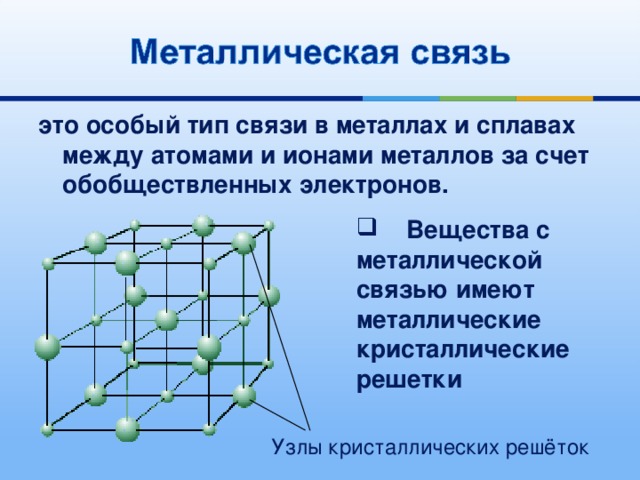
это особый тип связи в металлах и сплавах между атомами и ионами металлов за счет обобществленных электронов.
- Вещества с металлической связью имеют металлические кристаллические решетки
Узлы кристаллических решёток
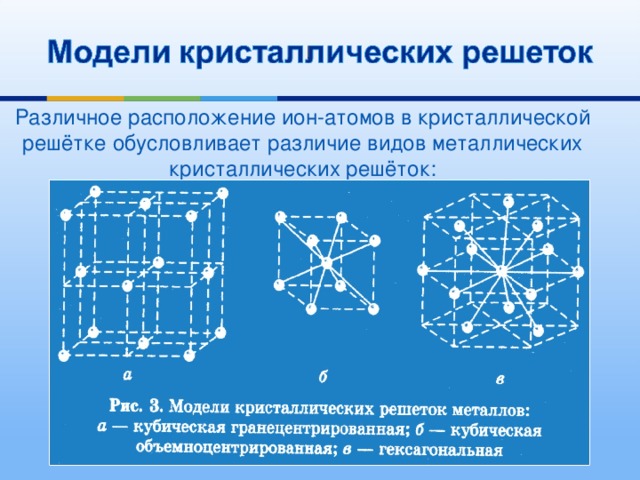
Различное расположение ион-атомов в кристаллической решётке обусловливает различие видов металлических кристаллических решёток:

Какие физические свойства металлов вам известны?

- Металлический блеск
- Пластичность
- Электропроводность
- Теплопроводность
- Твердость металлов
- Температура плавления
- Плотность металлов

- Металлический блеск – результат отражения световых лучей

- Пластичность и ковкость металлов связана со смещением слоев кристаллической решетки относительно друг друга
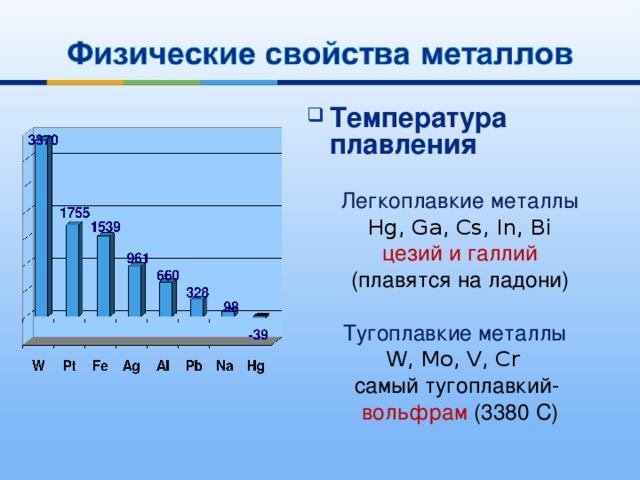
Легкоплавкие металлы
Hg, Ga, Cs, In, Bi
цезий и галлий
(плавятся на ладони)
Тугоплавкие металлы
W, Mo, V, Cr
самый тугоплавкий-
вольфрам ( 3380 С )
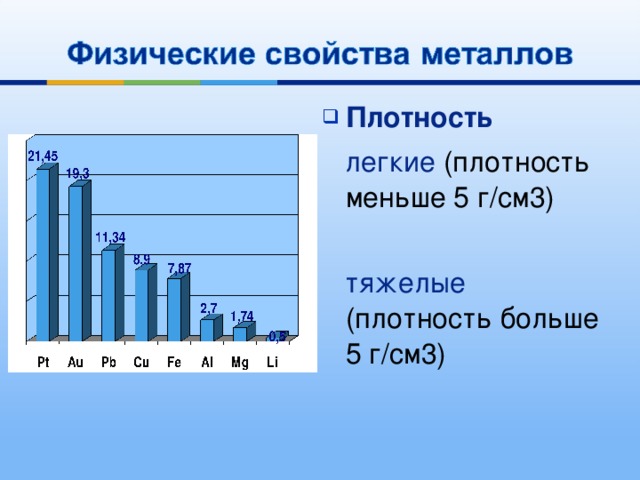
легкие (плотность меньше 5 г/см3)
тяжелые (плотность больше 5 г/см3)
- Схема 1. Классификация металлов по ________
металлы
легкие тяжелые
______________ _____________
______________ _____________
- Схема 2. Классификация металлов по ________
металлы
легкоплавкие тугоплавкие
______________ _____________
______________ _____________

самый мягкий металл – калий,
самый твердый металл – хром
Ртуть – единственный
жидкий металл
→
→
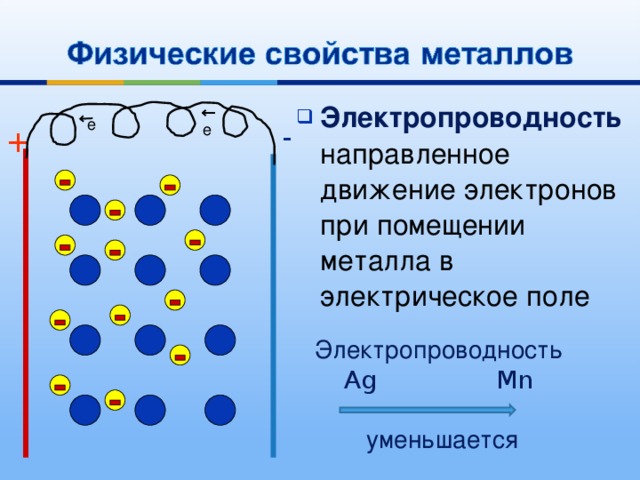
- Электропроводность направленное движение электронов при помещении металла в электрическое поле
е
-
е
+
Электропроводность
Ag Mn
уменьшается

- Теплопроводность движение свободных электронов быстро выравнивает температуру в массе металла
Теплопроводность
Hg, Cu, Ag, Al, Fe
уменьшается

1. Самый легкий металл:
А) цезий; Б) вольфрам; В) литий
2. Самый тяжелый металл:
А) вольфрам; Б) осмий; В) железо
3. Самый мягкий металл:
А) кальций; Б) натрий; В) алюминий
4. Самый твердый металл:
А) железо; Б) хром; В) вольфрам
5. Лучшим проводником является:
А) свинец; Б) медь; В) марганец

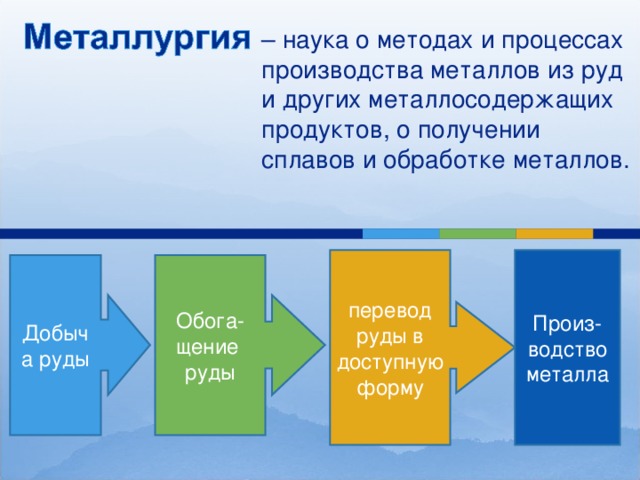
– наука о методах и процессах производства металлов из руд и других металлосодержащих продуктов, о получении сплавов и обработке металлов.
перевод руды в доступную форму
Произ-водство металла
Добыча руды
Обога-щение руды
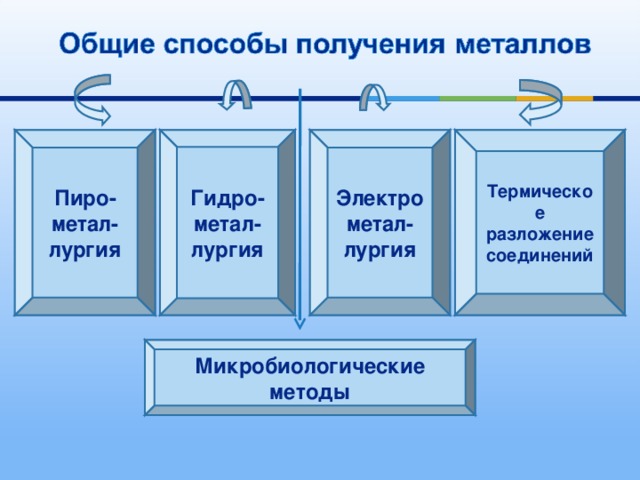
Пиро-
метал-лургия
Гидро-
метал-лургия
Электрометал-лургия
Термическое разложение соединений
Микробиологические методы

восстановление безводных соединений при высоких температурах
- карботермия - ( С или СО )
PbO +C = Pb + CO;
Fe 2 O 3 +3CO =2Fe +3CO 2
сульфиды предварительно обжигают
2ZnS+3O 2 =2ZnO+2SO 2 ; ZnO +C =Zn +2CO
- металлотермия - ( Al; Mg и др.) Cr 2 O 3 +2AL=2Cr +Al 2 O 3 ; TiCl 4 +2Mg=Ti +2MgCl 2
- водородотермия - ( Н 2 )
MoO 3 +3H 2 =Mo+3H 2 O
( MgO, CaO, Al 2 O 3 и др.)

восстановление из растворов солей другими более активными металлами.
- Гидрометаллургические процессы включают стадию перевода нерастворимых соединений металлов из руд в растворы:
CuO + H 2 SO 4 = CuSO 4 + H 2 O
CuSO 4 +Fe = FeSO 4 + Cu
получаемые металлы:
Cd, Ag, Au, Cu

восстановление металлов электрическим током
2 KCl (расплав) 2 K + Cl 2
получаемые металлы :
ЩМ, ЩЗМ, AL .
эл.ток
![Получают металлы в особо чистой форме: [Fe(CO) 5 ] = Fe + 5CO [Ni(CO) 4 ] = Ni + 4CO Fe и Ni получают из карбонилов, Ti, Zr, Th – из галогенидов , V, Ta, Nb – из оксидов. 160-200 C 200 C](https://static.multiurok.ru/multiurok/html/2017/02/24/s_58b093f76a949/img48.jpg)
- Получают металлы в особо чистой форме:
[Fe(CO) 5 ] = Fe + 5CO
[Ni(CO) 4 ] = Ni + 4CO
Fe и Ni получают из карбонилов,
Ti, Zr, Th – из галогенидов ,
V, Ta, Nb – из оксидов.
160-200 C
200 C

- Использование жизнедеятельности некоторых видов бактерий для перевода нерастворимых солей металлов в растворимые.
Тионовые бактерии:
Нерастворимые Растворимые
сульфиды сульфаты

Металл
Способ получения
А. Алюминий
1. Электролиз расплава соли
Б. Медь
2. Электролиз раствора соли
В. Натрий
3. Электролиз расплава оксида в криолите
Г. Железо
4. Пирометаллургия
А
Б
?
В
?
Г
?
?

А
Б
3
2
В
Г
1
4

- Сплавы – это материалы с характерными свойствами, состоящие из двух и более компонентов, из которых по крайней мере один – металл
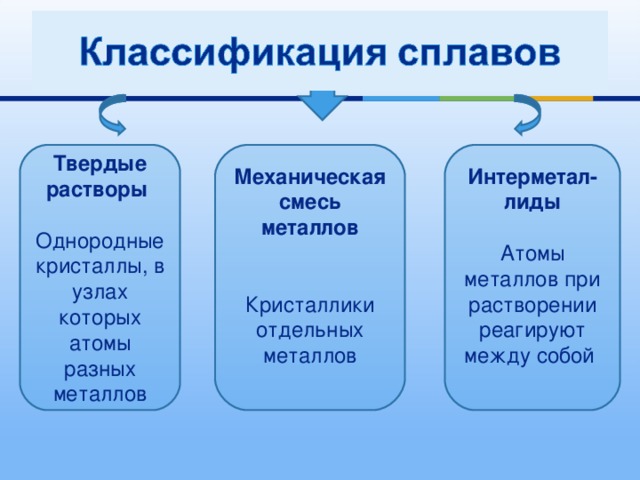
Интерметал-лиды
Атомы металлов при растворении реагируют между собой
Механическая смесь металлов
Кристаллики отдельных металлов
Твердые растворы
Однородные кристаллы, в узлах которых атомы разных металлов

Задание: заполнить таблицу «Сплавы»
(работа с учебником)
Название сплава
Примерный состав
Свойства
Применение


“ Человек не может обойтись без металлов...
Если бы не было металлов, люди
Влачили бы самую омерзительную и
Жалкую жизнь среди диких зверей...”
Георг Агрикола, 1556 г.

Создание презентации
«Металлов огненный поток»
Хайрутдинова Альфия Измаиловна
учитель химии
МОУ СОШ р.п. Старотимошкино
МО «Барышский район» Ульяновской области






















































![Получают металлы в особо чистой форме: [Fe(CO) 5 ] = Fe + 5CO [Ni(CO) 4 ] = Ni + 4CO Fe и Ni получают из карбонилов, Ti, Zr, Th – из галогенидов , V, Ta, Nb – из оксидов. 160-200 C 200 C](https://static.multiurok.ru/multiurok/html/2017/02/24/s_58b093f76a949/img48.jpg)





















