

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока

Была в сети 26.05.2020 16:11

Գափոյան Մարինե Թաթուլի
Քիմիայի ուսուցիչ
45 лет
Местоположение
Հայաստանի հանրապետություն, Երևան




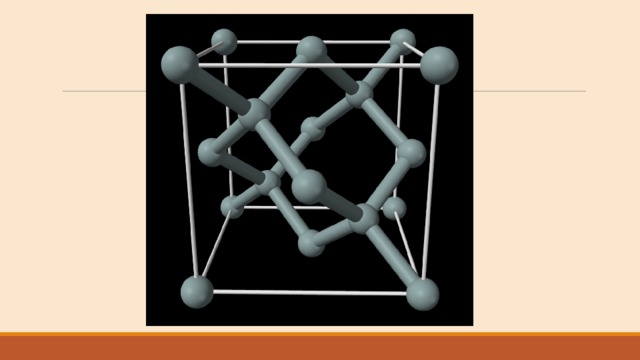

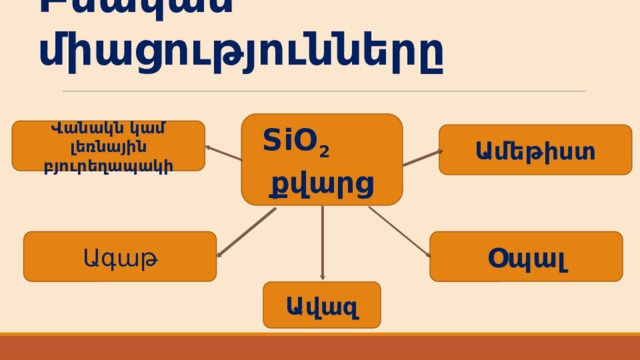





 2 , որտեղ X —հիմնականում K, նաև Na, NH 4 , Y — սովորաբար Mg, Fe, Al, երբեմն Ba, Mn, Ca, Ti, Zn, B, V, UO 2 . Ասբեստ 3MgO•2SiO 2 •2H 2 O](https://static.multiurok.ru/multiurok/html/2020/05/11/s_5eb988010b8b9/img10.jpg)




























