
- Подготовила
- Учитель химии
- МОУ СОШ№2 с.п.Атажукино
- Архестова Л.З.
- Проблемная тема:
- « Кто-то теряет, а кто-то находит.»
 Ca 2+ 2 8 8 2 2 8 8 атом ион S 0 +16 ) ) ) S 2- +16 ) ) ) S 0 + 2 e = S 2- 2 8 6 2 8 8 атом ион Ca 0 + S 0 = Ca +2 S -2 " width="640"
Ca 2+ 2 8 8 2 2 8 8 атом ион S 0 +16 ) ) ) S 2- +16 ) ) ) S 0 + 2 e = S 2- 2 8 6 2 8 8 атом ион Ca 0 + S 0 = Ca +2 S -2 " width="640"
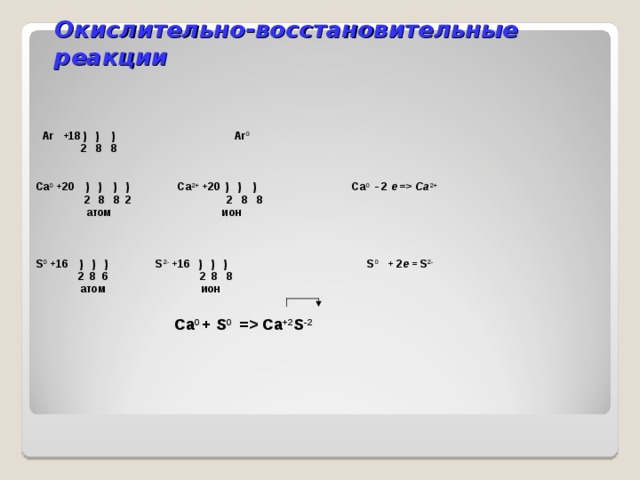
Окислительно-восстановительные реакции
Ar +18 ) ) ) Ar 0
2 8 8
Ca 0 +20 ) ) ) ) Ca 2+ +20 ) ) ) Ca 0 - 2 e = Ca 2+
2 8 8 2 2 8 8
атом ион
S 0 +16 ) ) ) S 2- +16 ) ) ) S 0 + 2 e = S 2-
2 8 6 2 8 8
атом ион
Ca 0 + S 0 = Ca +2 S -2

Расставьте степени окисления элементов в реакциях.
Сравните, как ведут себя степени окисления в процессе реакции.
+ 1 - 1 + 1 - 2 + 1 + 1 - 1 + 1 - 2
HCl + NaOH = NaCl + H 2 O
2 HCl + Zn = ZnCl 2 + H 2
+ 1 - 1 0 + 2 - 1 0
Окислительно-восстановительная реакция
Реакции, в которых происходит изменение степеней окисления, называются
окислительно-восстановительными

2 H +1 Cl -1 + Zn 0 = Zn +2 Cl 2 -1 + H 2 0
Zn 0
2 H +
Zn +2
H 2 0
- 2 е -
окисление
+ 2 е -
восстановление
H +
- окислитель
Zn 0
- восстановитель

Окисление – процесс отдачи электронов.
Восстановление – процесс присоединения электронов.
Окислитель – элемент, принимающий электроны.
Восстановитель – элемент, отдающий электроны.
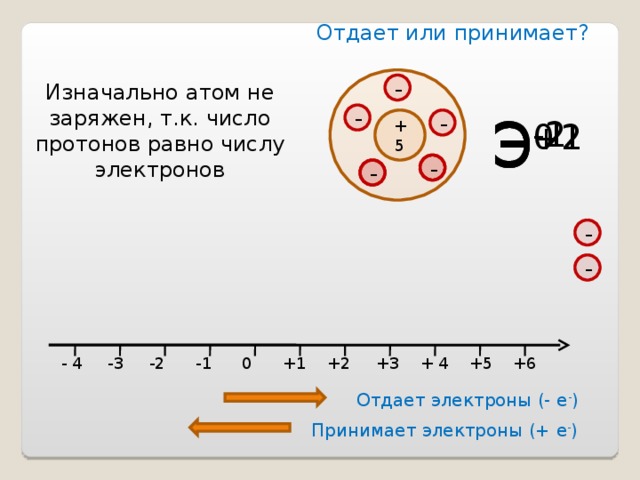
Отдает или принимает?
Изначально атом не заряжен, т.к. число протонов равно числу электронов
-
Э -1
Э -2
Э +1
Э +2
Э 0
-
-
+5
-
-
-
-
-
-
- 4 -3 -2 -1 0 +1 +2 +3 + 4 +5 +6
Отдает электроны (- е - )
Принимает электроны (+ е - )
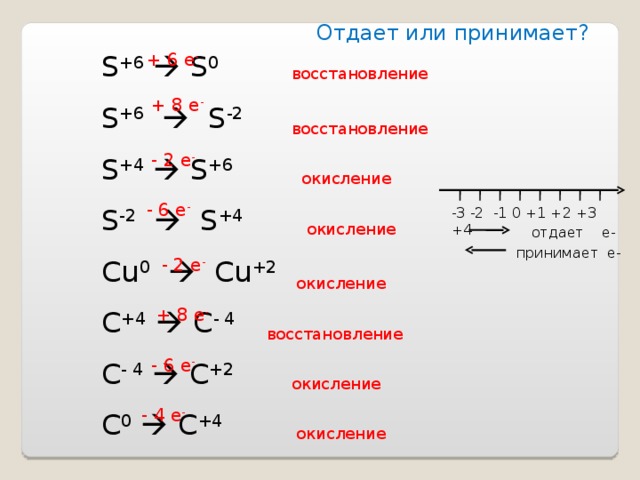
Отдает или принимает?
S +6 S 0
S +6 S -2
S +4 S +6
S -2 S +4
Cu 0 Cu +2
C +4 C - 4
C - 4 C +2
C 0 C +4
+ 6 e -
восстановление
+ 8 e -
восстановление
- 2 e -
окисление
- 6 e -
-3 -2 -1 0 +1 +2 +3 +4
окисление
отдает е-
принимает е-
- 2 e -
окисление
+ 8 e -
восстановление
- 6 e -
окисление
- 4 e -
окисление

Какая польза от теории ОВР?
Например, расстановка коэффициентов в сложных уравнениях – метод электронного баланса
+1 -1 +1 +7 -2 +2 -1 +1 -1 0 +1 -2
2
HCl + KMnO 4 = MnCl 2 + KCl + Cl 2 + H 2 O
8
16
2
2
5
Mn +7 +5 e- Mn +2
Восст-ие
2
10
2Cl -1 - 2 e- Cl 2 0
5
окисление
Mn +7 – окислитель
С l -1 – восстановитель

Расставьте коэффициенты методом электронного баланса .
Al + MnO 2 = Al 2 O 3 + Mn
Fe 2 O 3 + Zn = ZnO + Fe
Mg + H 2 SO 4 = MgSO 4 + H 2 S + H 2 O
Cu + HNO 3 = Cu(NO 3 ) 2 + NO + H 2 O
KI + FeCl 3 = l 2 + KCl + FeCl 2
Cr 2 O 3 + K 2 CO 3 + O 2 = K 2 CrO 4 + CO 2


Выяснить , как окислительно-восстановительные реакции применяются в быту .

Вы пролили йод на белую салфетку. Хлорная известь и персоль не обесцветят пятно йода. Вывести пятно помогут восстановители, например водный раствор сульфита натрия
I 2 +Na 2 SO 3 +2NaOH = 2NaI+Na 2 SO 4 +H 2 O .
Однако знайте, что через несколько дней пятно исчезнет благодаря постепенной сублимации йода.

При обработке персолью отбеливание происходит за счет окисления загрязнений
2H 2 O 2 = 2H 2 O+O 2 .
Для того чтобы образующийся
кислород не улетучивался
из емкости, лучше
держать ее
закрытой.

С помощью пероксида водорода реставрируют старинные картины. Промывая пероксидом водорода старые картины, сульфид переводят в белый сульфат:
PbS+4H 2 O 2 =PbSO 4 +4H 2 O .
Картины обновляются –
становятся вновь
яркими.

Мы часто сталкиваемся с окислительно-восстановительными реакциями в быту:
- при избавлении от пятен йода на ткани ;
- при стирке изделий из натуральной шерсти ;
- при удалении пятен от кофе, чая, фруктов ;
- при очищении ткани от загрязнений ;
- при полоскании горла и промывания ран .
 Li 2 O C 0 + O 2 0 = CO 2 H 0 2 + O 2 0 = H 2 O " width="640"
Li 2 O C 0 + O 2 0 = CO 2 H 0 2 + O 2 0 = H 2 O " width="640"
Покажите электронные переходы в следующих схемах ОВР Назовите окислитель и восстановитель
- Li 0 + O 2 0 = Li 2 O
- C 0 + O 2 0 = CO 2
- H 0 2 + O 2 0 = H 2 O
 СаО + СО 2 KMnO 4 = K 2 Mn О 4 + Mn О 2 + О 2 CuS + О 2 = С u О + S О 2 " width="640"
СаО + СО 2 KMnO 4 = K 2 Mn О 4 + Mn О 2 + О 2 CuS + О 2 = С u О + S О 2 " width="640"
Из приведенных схем уравнений реакций выпишите те, которые можно отнести к ОВР
- СаСО 3 = СаО + СО 2
- KMnO 4 = K 2 Mn О 4 + Mn О 2 + О 2
- CuS + О 2 = С u О + S О 2
 C +4 О 2 -2 + 2 H 2 +1 О- 2 -8e С -4 C +4 - восстановитель - ( окисляется ) 4|1 +4e О 2 0 2 О- 2 - окислитель - ( восстанавливается ) 8 |2 " width="640"
C +4 О 2 -2 + 2 H 2 +1 О- 2 -8e С -4 C +4 - восстановитель - ( окисляется ) 4|1 +4e О 2 0 2 О- 2 - окислитель - ( восстанавливается ) 8 |2 " width="640"
Расставьте коэффициенты методом электронного баланса в следующих схемах ОВР Определите окислитель, восстановитель
- 1)С -4 Н 4 +1 + 2 О 2 0 = C +4 О 2 -2 + 2 H 2 +1 О- 2
-8e
- С -4 C +4 - восстановитель - ( окисляется ) 4|1
+4e
- О 2 0 2 О- 2 - окислитель - ( восстанавливается ) 8 |2

Домашнее задание:
- Параграф 43, вопросы письменно 1,3,7
- Предложите на звание «чуда» примеры из цикла наук предметов естественнонаучного цикла.

Рефлексия
- Я сегодня узнал…
- Я удивился…
- Теперь я умею…
- Я хотел бы…
- Я смог…
- Я научился…
- Урок мне дал дляжизни …







 Ca 2+ 2 8 8 2 2 8 8 атом ион S 0 +16 ) ) ) S 2- +16 ) ) ) S 0 + 2 e = S 2- 2 8 6 2 8 8 атом ион Ca 0 + S 0 = Ca +2 S -2 " width="640"
Ca 2+ 2 8 8 2 2 8 8 атом ион S 0 +16 ) ) ) S 2- +16 ) ) ) S 0 + 2 e = S 2- 2 8 6 2 8 8 атом ион Ca 0 + S 0 = Ca +2 S -2 " width="640"













 Li 2 O C 0 + O 2 0 = CO 2 H 0 2 + O 2 0 = H 2 O " width="640"
Li 2 O C 0 + O 2 0 = CO 2 H 0 2 + O 2 0 = H 2 O " width="640"
 СаО + СО 2 KMnO 4 = K 2 Mn О 4 + Mn О 2 + О 2 CuS + О 2 = С u О + S О 2 " width="640"
СаО + СО 2 KMnO 4 = K 2 Mn О 4 + Mn О 2 + О 2 CuS + О 2 = С u О + S О 2 " width="640"
 C +4 О 2 -2 + 2 H 2 +1 О- 2 -8e С -4 C +4 - восстановитель - ( окисляется ) 4|1 +4e О 2 0 2 О- 2 - окислитель - ( восстанавливается ) 8 |2 " width="640"
C +4 О 2 -2 + 2 H 2 +1 О- 2 -8e С -4 C +4 - восстановитель - ( окисляется ) 4|1 +4e О 2 0 2 О- 2 - окислитель - ( восстанавливается ) 8 |2 " width="640"












