
ОПОРНЫЕ КОНСПЕКТЫ: «ЩЕЛОЧНЫЕ МЕТАЛЛЫ. IА» «ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ. IIA» «АЛЮМИНИЙ. IIIА» «ЖЕЛЕЗО – ЭЛЕМЕНТ ПОБОЧНОЙ ПОДГРУППЫ»
Составила: Учитель химии Харина Елена Юрьевна
МБОУ «СОШ №10 с углубленным

ЩЕЛОЧНЫЕ МЕТАЛЛЫ.
I группа. Главная подгруппа.
Li, Na, K, Rb, Cs, Fr
ns 1 - общая электронная плотность
p
- ē
s
+1
увеличивается радиус атома
Li, Na, K, Rb, Cs, Fr
увеличиваются восстановительные свойства
Очень мягкие металлы с малой плотностью, малой электроотрицательностью,
малым потенциалом ионизации, низкими температурами кипения и плавления;
чрезвычайно реакционноспособны, растворимы в жидком аммиаке, аминах, эфирах.
Оксиды и гидроксиды – сильные основания.
ПОЛУЧЕНИЕ
ЭЛЕКТРОЛИЗ РАСПЛАВОВ
ХЛОРИДОВ И ГИДРОКСИДОВ
ЭТИХ МЕТАЛЛОВ
NaCl
NaOH
KCl
KOH
Электролиз – это окислительно-восстановительный процесс,
проходящий на электродах под действием электрического тока
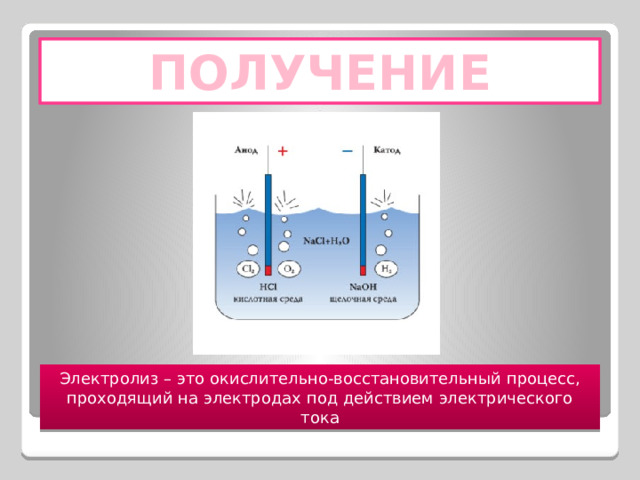
ПОЛУЧЕНИЕ
Электролиз – это окислительно-восстановительный процесс,
проходящий на электродах под действием электрического тока

ХИМИЧЕСКИЕ СВОЙСТВА
1. С КИСЛОРОДОМ
2Na+O 2 =Na 2 O 2 (в обычных условиях)
4Li+O 2 =2Li 2 O (только оксид лития)
2. С ГАЛОГЕНАМИ
2Na+Cl 2 =2NaCl (галогенид)
3. С СЕРОЙ ПРИ НАГРЕВАНИИ
2Na+S=Na 2 S (сульфид)
4. С АЗОТОМ
6Na+N 2 =2Na 3 N (нитрид)
5. С ВОДОРОДОМ ПРИ НАГРЕВАНИИ
2Na+H 2 =2NaH (гидрид)
6. С ВОДОЙ
2Na+2H 2 O=2NaOH+H 2

ОКРАШИВАНИЕ ПЛАМЕНИ
качественные реакции
Li +
Na +
ЖЁЛТОЕ
КРАСНОЕ
ПЛАМЯ
ПЛАМЯ
K +
Cs +
ФИОЛЕТОВОЕ
РОЗОВОЕ
ПЛАМЯ
ПЛАМЯ

СОЕДИНЕНИЯ
ЩЕЛОЧНЫХ МЕТАЛЛОВ
ЩЕЛОЧИ Me(OH)
ТВЁРДЫЕ КРИСТАЛЛИЧЕСКИЕ
ВЕЩЕСТВА, ТИПИЧНО ИОННЫЕ
СОЕДИНЕНИЯ, СИЛЬНЫЕ ОСНОВАНИЯ
1) NaOH+HCl=NaCl+H 2 O
2) NaOH+CuCl 2 =Cu(OH) 2 +NaCl
3) 2NaOH+CO 2 =Na 2 CO3+H 2 O (при недостатке CO 2 )
NaOH+CO 2 =NaHCO 3 (при избытке CO 2 )
4) NaOH+Al(OH) 3 =NaAlO 2 +2H 2 O
Применение (примеры):
NaOH – для титрирования кислот, гидролиза органических соединений;
для производства мыла.
KOH – для получения жидкого мыла, электролит в аккумуляторах.

KOH
NaOH
Используется для изготовления
Гидролиз белка
жидкого мыла
(при изготовлении
детского питания и
питания для спортсменов)
Применение (примеры):
NaOH – для титрирования кислот, гидролиза органических соединений;
для производства мыла.
KOH – для получения жидкого мыла, электролит в аккумуляторах.

СОЕДИНЕНИЯ
ЩЕЛОЧНЫХ МЕТАЛЛОВ
ИОННЫЕ СОЕДИНЕНИЯ, ХОРОШО
СОЛИ ЩЕЛОЧНЫХ
МЕТАЛЛОВ
РАСТВОРИМЫ В ВОДЕ,
РАСТВОРИМОСТЬ РАСТЁТ ОТ Li к Cs
Важнейшие:
ХЛОРИД НАТРИЯ NaCl – используется в пище, для консервирования;
сырьё для получения гидроксида Na, хлора, соляной кислоты, соды…
СУЛЬФАТ НАТРИЯ Na 2 SO 4 – используется в производстве соды и стекла.
КАЛИЙНЫЕ СОЛИ – используются в качестве удобрений
(калийные удобрения KCl, KCl*MgCl 2 , K 2 CO 3 )

NaCl
Калийные соли
Na 2 SO 4
Важнейшие:
ХЛОРИД НАТРИЯ NaCl – используется в пище, для консервирования;
сырьё для получения гидроксида Na, хлора, соляной кислоты, соды…
СУЛЬФАТ НАТРИЯ Na 2 SO 4 – используется в производстве соды и стекла.
КАЛИЙНЫЕ СОЛИ – используются в качестве удобрений
(калийные удобрения KCl, KCl*MgCl 2 , K 2 CO 3 )
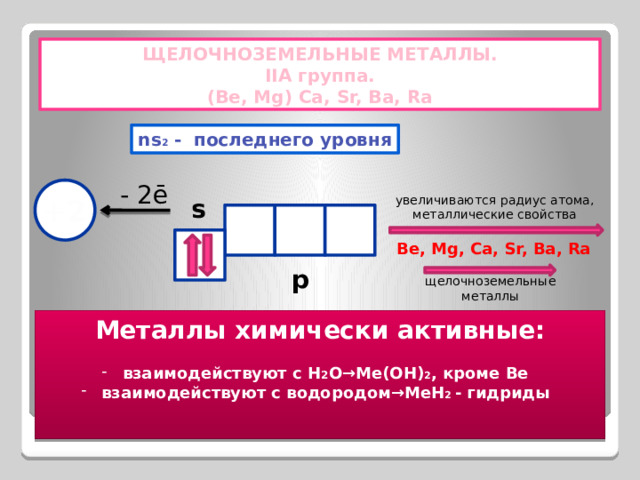
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ.
IIA группа.
(Be, Mg) Ca, Sr, Ba, Ra
ns 2 - последнего уровня
- 2ē
увеличиваются радиус атома,
металлические свойства
s
+2
Be, Mg, Ca, Sr, Ba, Ra
p
щелочноземельные
металлы
Металлы химически активные:
- взаимодействуют с H 2 O →Me(OH) 2 , кроме Be
- взаимодействуют с водородом→MeH 2 - гидриды

ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ.
IIA группа.
(Be, Mg) Ca, Sr, Ba, Ra
Be Mg Ca Sr Ba

КАЛЬЦИЙ Ca
Физические свойства Ca:
лёгкий, беловато-серый, пластичный
В природе:
CaSO4*2H2O – гипс; C3(PO4)2 - фосфорит
ПОЛУЧЕНИЕ Са:
- электролиз расплавов солей CaCl 2 =Ca+Cl 2 ;
- из оксидов 2CaO+2Al=2Ca+Al 2 O 3
ХИМИЧЕСКИЕ СВОЙСТВА Са
С ПРОСТЫМИ ВЕЩЕСТВАМИ
СО СЛОЖНЫМИ ВЕЩЕСТВАМИ
- Ca+H 2 =CaH 2
- 3Ca+Cl 2 =CaCl 2 (галогениды)
- 2Ca+O 2 =2CaO (кирпич – красное пламя), Ca+O 2 =CaO 2 (пероксиды)
- 3Ca+Na 2 =Ca 3 N 2 (при нагревании (не вступает в эту реакцию))
- Ca+2C=CaC 2 (карбид) при нагревании
- Ca+2NH 3 =Ca(NH 2 ) 2 ↓+H 2 ↑ Be и Mg с NH3 (жидк.) не образуют амиды
- Ca+2H 2 O=Ca(OH) 2 +H 2 ↑ (в холодной воде кроме Mg и Be)
- Ca+2HCl=CaCl 2 +H 2 ↑ любая кислота кроме HNO3

СОЕДИНЕНИЯ Са
Оксид кальция CaO – «негашеная известь»
Получение: CaCO 3 =CaO+CO 2 ↑ (обжиг)
Химические свойства: CaO – основной оксид
- CaO+SiO 2 =CaSiO 3
- CaO+CO 2 =CaCO 3
- CaO+2HCl=CaCl 2 +H 2 O
- CaO+3C=CaC 2 +CO ↑ (нагревание)
Гидроксид кальция Ca(OH)2 – «гашеная известь»
Получение: CaO+H 2 O=Ca(OH) 2
Физические свойства: твёрдое вещество белого цвета,
малорастворимое в воде.
Качественная реакция на Ca 2+
Ca(OH) 2 +CO 2 =CaCO 3 ↑ +H 2 O – раствор мутнеет, при дальнейшем пропускании СО 2 раствор становится прозрачным:
CaCO 3 +CO 2 +H 2 O=Ca(HCO 3 ) 2
ПРИМЕНЕНИЕ:
CaC l2 – водопоглощающее средство, CaS – для выделки кожи;
Ca(OH) 2 – в сельском хозяйстве, строительстве

СОЕДИНЕНИЯ Са
СТРОИТЕЛЬСТВО
ВОДОПОГЛАЩАЮЩЕЕ
СРЕДСТВО
(побелка потолка)
ВЫДЕЛКА КОЖИ
ПРИМЕНЕНИЕ:
CaCl 2 – водопоглощающее средство, CaS – для выделки кожи;
Ca(OH) 2 – в сельском хозяйстве, строительстве
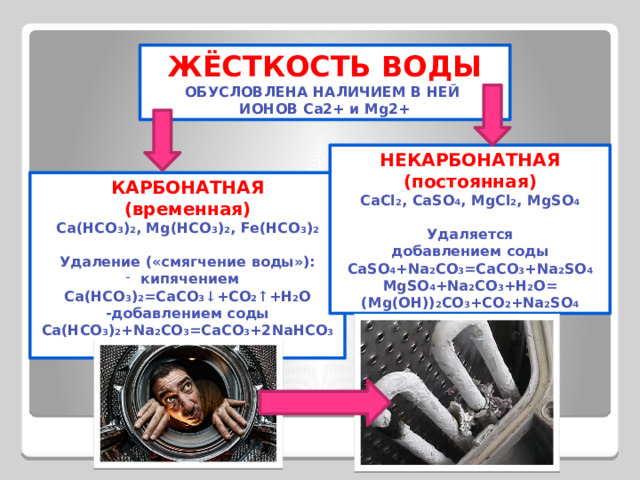
ЖЁСТКОСТЬ ВОДЫ
ОБУСЛОВЛЕНА НАЛИЧИЕМ В НЕЙ
ИОНОВ Ca2+ и Mg2+
НЕКАРБОНАТНАЯ
(постоянная)
CaCl 2 , CaSO 4 , MgCl 2 , MgSO 4
Удаляется
добавлением соды
CaSO 4 +Na 2 CO 3 =CaCO 3 +Na 2 SO 4
MgSO 4 +Na 2 CO 3 +H 2 O=
(Mg(OH)) 2 CO 3 +CO 2 +Na 2 SO 4
КАРБОНАТНАЯ
(временная)
Ca(HCO 3 ) 2 , Mg(HCO 3 ) 2 , Fe(HCO 3 ) 2
Удаление («смягчение воды»):
Ca(HCO 3 ) 2 =CaCO 3 ↓ +CO 2 ↑ +H 2 O
-добавлением соды
Ca(HCO 3 ) 2 +Na 2 CO 3 =CaCO 3 +2NaHCO 3
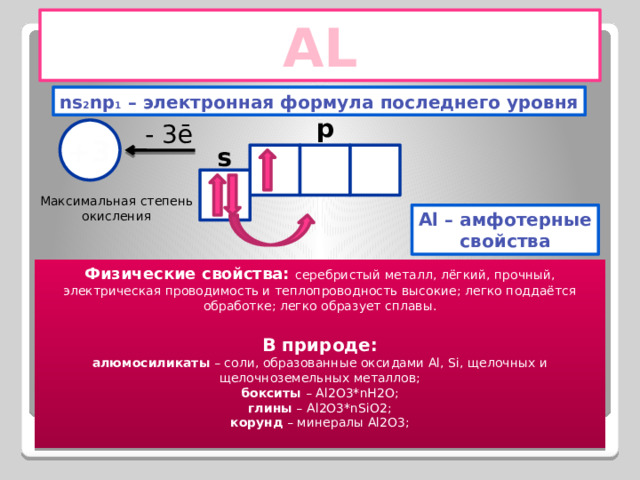
AL
ns 2 np 1 – электронная формула последнего уровня
p
- 3ē
+3
s
Максимальная степень
окисления
Al – амфотерные
свойства
Физические свойства: серебристый металл, лёгкий, прочный, электрическая проводимость и теплопроводность высокие; легко поддаётся обработке; легко образует сплавы.
В природе:
алюмосиликаты – соли, образованные оксидами Al, Si, щелочных и щелочноземельных металлов;
бокситы – Al2O3*nH2O;
глины – Al2O3*nSiO2;
корунд – минералы Al2O3;
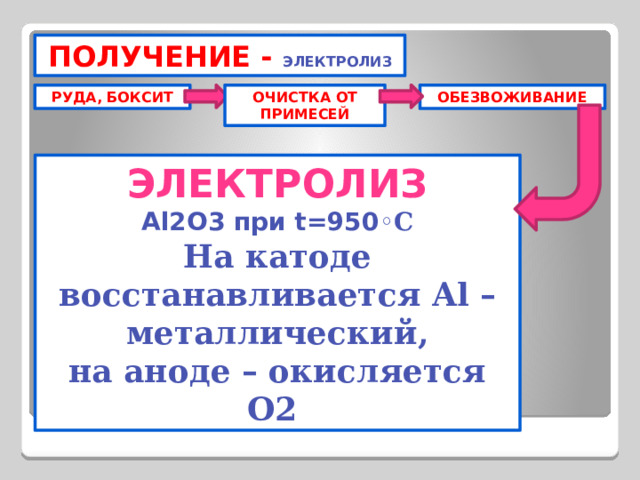
ПОЛУЧЕНИЕ - ЭЛЕКТРОЛИЗ
РУДА, БОКСИТ
ОЧИСТКА ОТ
ОБЕЗВОЖИВАНИЕ
ПРИМЕСЕЙ
ЭЛЕКТРОЛИЗ
Al2O3 при t=950 ◦C
На катоде восстанавливается Al – металлический,
на аноде – окисляется O2

ПОЛУЧЕНИЕ - ЭЛЕКТРОЛИЗ
На одну тонну алюминия при электролизе необходимо
приблизительно две тонны глинозема,
0,6 тонн угольных электродов (используются в качестве анодов),
100 килограмм криолита и
от 17 до 18 тысяч киловатт в час электроэнергии.

ХИМИЧЕСКИЕ СВОЙСТВА Al
1. ПОКРЫВАЕТСЯ ПРОЧНОЙ ПЛЁНКОЙ ОКСИДА
4Al+3O 2 =2AlO 3
2. НА ХОЛОДЕ
2Al+3Cl 2 =2AlCl 3 (Br 2 , J 2 )
3. ПРИ НАГРЕВАНИИ
2Al+3S=Al 2 S 3 (N, C)
4. ПРИ ПРЕДВАРИТЕЛЬНОЙ ОБРАБОТКЕ Al
СОЛЯМИ РТУТИ. РЕАКЦИЯ С ВОДОЙ ПРОТЕКАЕТ
С ОБРАЗОВАНИЕМ ГИДРОКСИДА РТУТИ
2Al+6H 2 O=2Al(OH) 3 +3H 2

ХИМИЧЕСКИЕ СВОЙСТВА Al
5. ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ
РАЗНОЙ АКТИВНОСТИ И КОНЦЕНТРАЦИИ
2Al+6HCl=2AlCl 3 +3H 2
2Al+6H 2 SO 4 (конц.) =Al 2 (SO 4 ) 3 +3SO 2 +6H 2 O
Al+6HNO 3(конц.)= Al(NO 3 ) 3 +3NO 2 +3H 2 O
АЛЮМОТЕРМИЯ
получение металлов (Fe, Cr, Mn, Ti, W) из их оксидов:
8Al+3Fe3O4=4Al2O3+9Fe (термит)

ПРОЦЕСС АЛЮМОТЕРМИТНОЙ
СВАРКИ РЕЛЬСОВ
АЛЮМОТЕРМИЯ
получение металлов (Fe, Cr, Mn, Ti, W) из их оксидов:
8Al+3Fe3O4=4Al2O3+9Fe (термит)

ИСПОЛЬЗОВАНИЕ
Al
Al – конструкционный материал, входит в состав сплавов, например: дюралюмин (с 5%Cu и 2%Mg) и др.; устойчив к коррозии; алюминиевые бронзы (Cu+5%Al) – для чеканки монет; пигмент краски «серебрянки»; в металлургии – для получения металлов; для сварки стали.

Al – материал для чеканки монет
Al – конструкционный
материал
каркас из алюминия
Al – пигмент
Al – сварка стали

СОЕДИНЕНИЯ Al +3
ОКСИД Al 2 O 3 (корунд)
ГИДРОКСИД Al(OH) 3
Белые, твёрдые вещества, не растворяются в воде.
ПОЛУЧЕНИЕ
- Очистка природных соединений
- В лаборатории:
4Al+3O 2 =2Al 2 O 3 (сжигание в O 2 )
AlCl 3 +3NaOH=Al(OH) 3 +3NaCl
2Al(OH) 3 =Al2O 3 +3H 2 O (прокаливание)
АМФОТЕРНЫЕ СВОЙСТВА
- Al 2 O 3 +6HCl=2AlCl 3 +3H 2 O
- Al 2 O 3 +2NaOH=2NaAlO 2 +H 2 O
- Al(OH) 3 +3HCl=3H 2 O+AlCl 3
- Al(OH) 3 +NaOH=NaAlO 2 +2H 2 O
(сплавление)
(сплавление)

ЖЕЛЕЗО
(n-1)d (6-8) ns 2 - общая электронная плотность
s
s
s
d
- 3ē
d
d
- 2ē
+2
+3
0
степень окисления
степень окисления

ПОЛУЧЕНИЕ ЖЕЛЕЗА
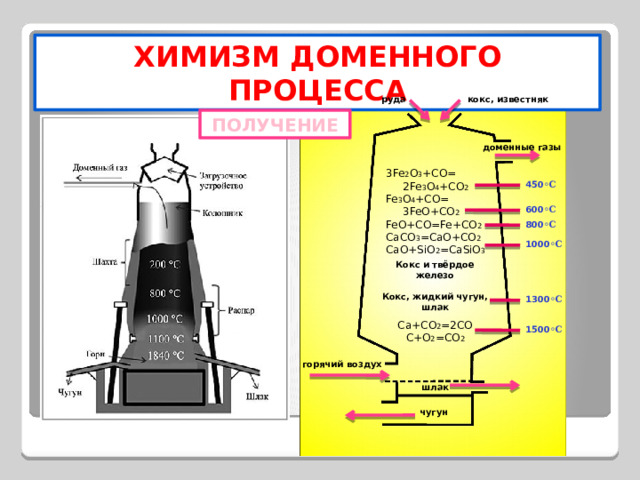
ХИМИЗМ ДОМЕННОГО ПРОЦЕССА
кокс, известняк
руда
ПОЛУЧЕНИЕ
доменные газы
3Fe 2 O 3 +CO=
2Fe 3 O 4 +CO 2
Fe 3 O 4 +CO=
3FeO+CO 2
FeO+CO=Fe+CO 2
CaCO 3 =CaO+CO 2
CaO+SiO 2 =CaSiO 3
450 ◦С
600 ◦С
800 ◦С
1000 ◦С
Кокс и твёрдое
железо
Кокс, жидкий чугун,
шлак
1300 ◦С
Ca+CO 2 =2CO
C+O 2 =CO 2
1500 ◦С
горячий воздух
шлак
чугун

Fe
В природе:
Fe 3 O 4 (FeO*Fe 2 O 3 ) – магнитный железняк; Fe 2 O 3 – гематит (красный железняк; Fe 2 O 3 *H 2 O – лимонит (бурый железняк); FeS 2 – пирит; FeCO 3 – шпатовый железняк.
Физические свойства:
железо – блестящий серебристо-белый металл, обладает хорошей пластичностью, Тпл. = 1539 ◦С. Легко намагничивается и размагничивается.
Химические свойства:
металл средней активности, восстановитель, в сухом воздухе – защитная плёнка оксида, во влажном – ржавеет.
(до Fe 3+ ): 3О 2 +Fe=2Fe 2 O 3
3Cl 2 +2Fe=2FeCl 3
2) Со слабыми окислителями
(до Fe 2+ ): S+Fe=FeS
CuSO 4 +Fe=FeSO 4 +Cu
3Fe+4H 2 O=Fe 3 O 4 +4H 2
3) 4HNO 3 +Fe=Fe(NO 3 ) 3 +NO+2H 2 O
6H 2 SO 4 +2Fe 2 (SO 4 ) 3 +3SO 2 +6H 2 O
На холоде не реагирует – пассивируется!

Повторите пройденное. Параграфы 11-14 СПАСИБО ЗА ВНИМАНИЕ.















































