План-конспект урока по физике в 9 классе
«Опыт Резерфорда»
Подготовила:
Цели:
Образовательная: ознакомить учащихся с историей формирования представлений о строении вещества, возникновением понятия «атом», познакомиться с планетарной (ядерной) моделью атома по Э. Резерфорду, её недостатками, узнать современные взгляды на строение атома (постулаты Н. Бора).
Развивающая: способствовать развитию познавательной активности, образного мышления; развивать умение учащихся применять полученные знания при решении задач.
Воспитательная: воспитывать чувство ответственности и готовности к сотрудничеству; приобретение навыков общения и самоорганизации; способствовать формированию научного мировоззрения.
Тип урока: комбинированный.
Методы: лекция, поисковая беседа, работа с визуальным опорным конспектом, решение качественных задач.
Оборудование: персональный компьютер, мультимедийный проектор, плакат: таблица «Периодическая система химических элементов Д.И. Менделеева».
экран, презентация к уроку.
План урока
| Этапы урока | Время, мин | Приёмы и методы |
| І. Организационный момент, сообщение плана работы на уроке. | 1-2 мин | Информация учителя |
| ІІ. Активизация знаний. | 3-5 мин | Беседа |
| ІІІ. Изучение нового материала. | 20-25 мин | Беседа, рассказ, сопровождающийся презентаци ,фильм «Опыт Резерфорда» |
| ІV. Закрепление изученного материала. | 8-10 мин | Решение качественных задач. |
| V. Домашнее задание | 1-2 мин | Сообщение учителя |
ХОД УРОКА:
I. Объявить тему, цель и задачи урока.
IІ. Актуализация знаний учащихся. Фронтальный опрос:
1. Как называется мельчайшая частица вещества? (Молекула)
2. Из чего состоят молекулы? (Из атомов)
3. Из чего состоят атомы? (Электроны, протоны, нейтроны)
4. Чему равен электрический заряд атома? (Атом электрически нейтрален)
5. Как называется «частица» электромагнитной волны? (Квант, фотон)
III. Изучение нового материала. Работа с опорным конспектом + презентация.
Атомистические взгляды античных философов.
Модель атома Томсона.
Опыты Резерфорда.
Ядерная (планетарная) модель атома Резерфорда.
Квантовые постулаты Н. Бора.
1. Атомистические взгляды античных философов. Гипотеза о том, что все вещества состоят из большого числа атомов, зародилась свыше двух тысячелетий тому назад. Сторонники атомистической теории рассматривали атом как мельчайшую неделимую частицу и считали, что всё многообразие мира есть не что иное, как сочетание неизменных частиц-атомов.
Позиция Демокрита: «Существует предел деления атома».
Позиция Аристотеля: «Делимость вещества бесконечна».
2. Модель атома Томсона. К 1902 г. было проведено достаточно экспериментов, убедительно доказавших, что одной из основных составных частей любого вещества является электрон. На этом основании Дж. Томсон в 1903 г. предложил модель, согласно которой атомы представляют собой однородные шары из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду «шара». Поэтому атом в целом электрически нейтрален. 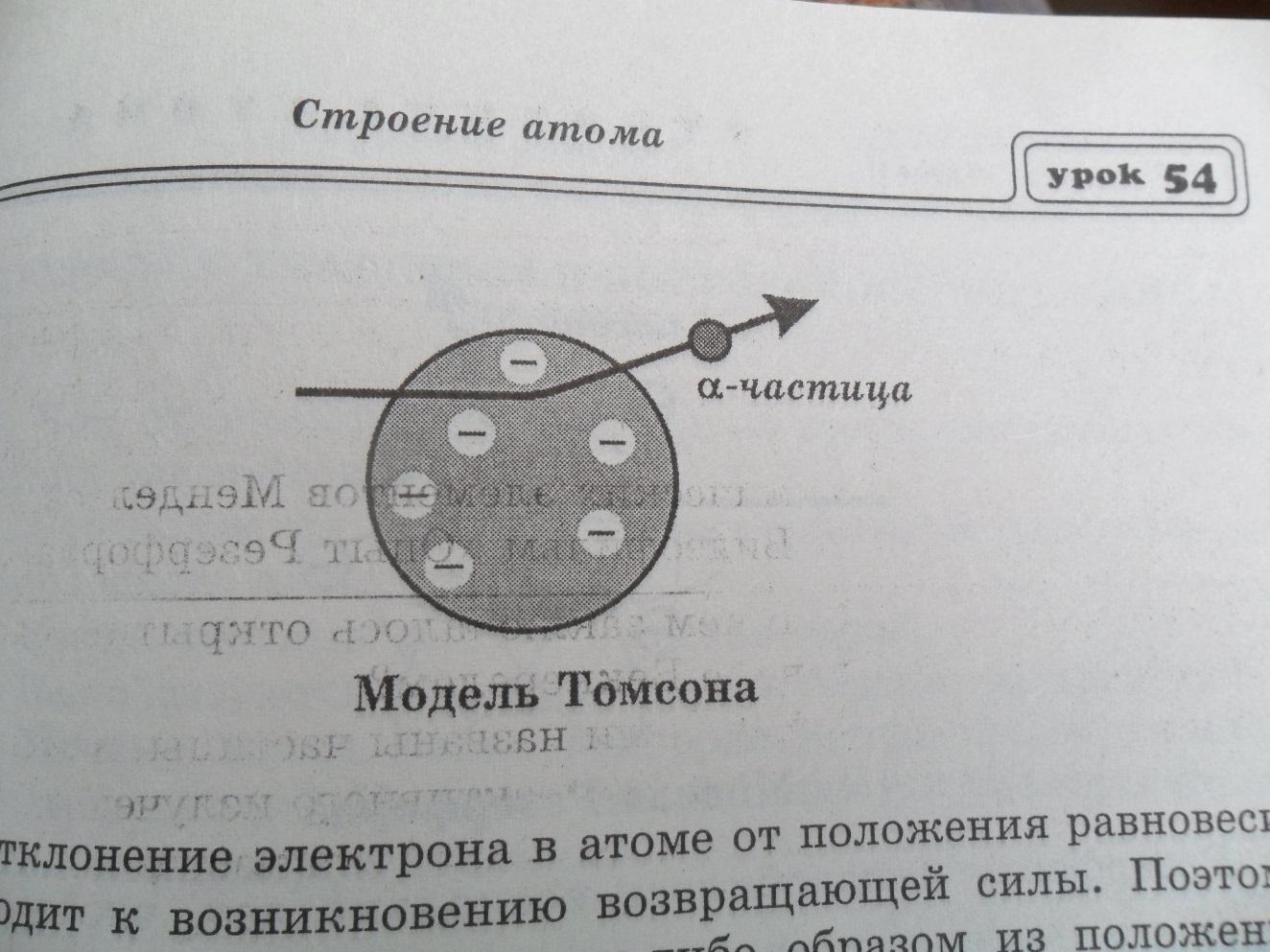
Эта модель получила название «пудинг», «кисель», «кекс», так как электроны были вкраплены в положительно заряженную среду, подобно изюму в пудинге.
3. Опыты Э. Резерфорда. Экспериментальная проверка модели Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом. Пропуская пучок α-частиц (заряд qα = +2e, масса mα = 8000me, скорость υα = 15000м/с) через тонкую золотую фольгу, Э. Резерфорд обнаружил, что некоторая часть частиц отклоняется на значительный угол от своего первоначального направления, а 1/20 000 часть частиц отражается от фольги толщиной всего лишь 4 10-5см.
Резерфорду понадобилось несколько лет, чтобы понять рассеяние α-частиц на большие углы. Он пришёл к выводу, что положительный заряд атома сосредоточен в очень малом объёме в центре атома, а не распределён по всему объёму, как в модели Томсона. 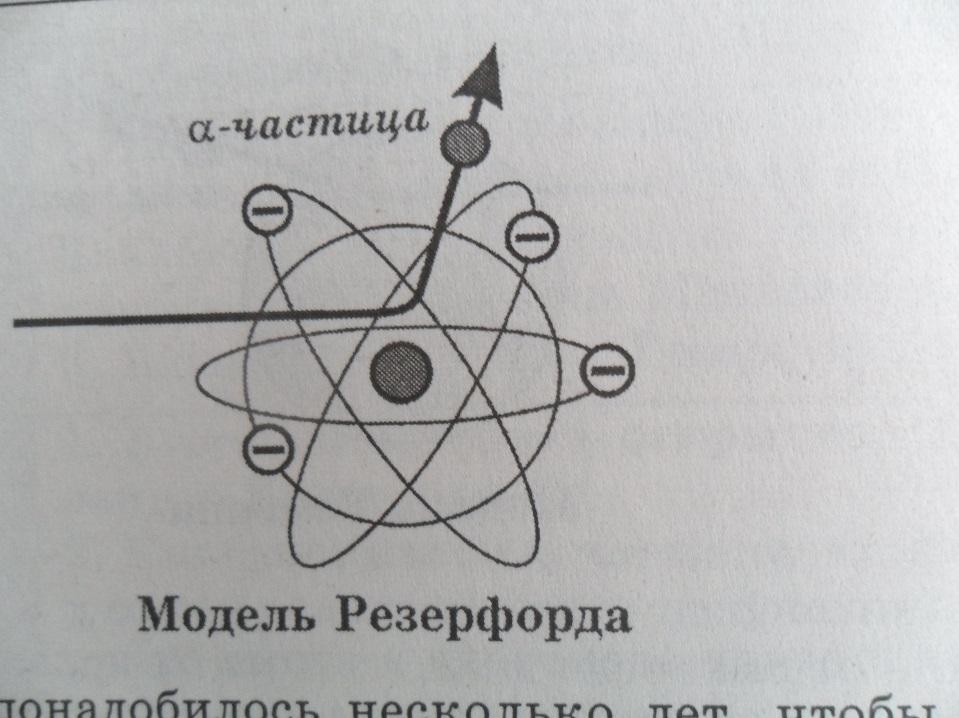
4. Ядерная (планетарная) модель атома Резерфорда. Резерфорд предложил ядерную (планетарную) модель атома:
- атомы любого элемента состоят из положительно заряженной части – ядра; (dя = 10-15 – 10-14 м, mя = mат, qя = +Z qe );
- вокруг ядра вращаются электроны;
- dат = 10-10 – 10-9м, dя = 10-15 – 10-14 м, mя = mат, qя = +Z qe (Z – порядковый номер элемента в таблице Менделеева);
Атом, потерявший (или приобретший) один или несколько электронов, становится положительным (или отрицательным) ионом.
Но: предложенная Э. Резерфордом планетарная модель атома не объясняла наличие линейчатых спектров излучения (вращаясь вокруг ядра, электрон должен непрерывно излучать электромагнитные волны). Выходом из этих противоречий стали сформулированные в 1913 г. постулаты Н. Бора:
Атом может находиться только в особых, стационарных состояниях. Находясь в стационарном состоянии, атом не излучает и не поглощает.
Излучение света происходит при переходе атома из стационарного состояния с большей энергией Еk в стационарное состояние с меньшей энергией Еn.
Атом может излучать (и поглощать) свет только с определёнными частотами:
ν = (Еk – Еn) / h, h – постоянная Планка.
IV. Закрепление изученного материала. Для закрепления изученного материала предлагается обсудить фильм «Опыт Резерфорда»
из серии« Учебное видео .Вопросы § 21
Учитель: Теперь откройте таблицу Менделеева и внимательно посмотрите на нее. Рассмотрим строение атома химических элементов водорода, гелия, лития, бериллия (H, He,Li,Be). Пример: Атом водорода занимает первую клеточку в таблице Менделеева. Электрический заряд ядра атома водорода положителен и равен произведению элементарного электрического заряда e на порядковый номер Z химического элемента в таблице Менделеева. q=Ze .Значит, заряд ядра равен 1. Мы можем определить и количество электронов в атоме водорода. Так как атом нейтрален, то количество электронов в атоме водорода будет равно 1.Электрон имеет отрицательный заряд.
Вопросы:
Каков заряд ядра атома He,Li,Be?
Сколько электронов в атоме He,Li,Be?
Чем отличаются друг от друга атомы различных химических элементов?
Что является главной характеристикой определенного химического элемента?
В чем сущность планетарной модели строения атома?
V. Изложение материала развивающего характера.
Сообщения учащихся: «Страницы биографии Эрнеста Резерфорда».
V1. Подведение итогов. Ученикам, отвечавшим на вопросы и самостоятельно размышлявшим в ходе урока, выставляются оценки. При ответах оценивается не только правильность ответа, но и ход рассуждений, количество и качество ошибок.
Домашнее задание § 21, 22.. Нарисовать схему модели атома лития, азота, кислорода, фтора. Определить заряд ядра каждого атома.
Литература
Физика –9 кл. О. Ф.Кабардин , Москва:,Просвещение,2014г.
Теория и методика обучения физике в школе. Частные вопросы. Под редакций С.Е.Каменецкого Москва:,Akademia,2000 г.
Физика –11 кл. С.В.Громов Москва:,Просвещение,1999 г.
С. Кудрявцев Курс истории физики.Москва:,Просвещение,1974 г.
Интернет – ресурсы:


















