
Государственное бюджетное профессиональное
образовательное учреждение
«Починковский сельскохозяйственный техникум»
Открытый урок по химии
Выполнила:
Преподаватель ООД
Могина Татьяна Альбертовна
с. Починки
2022 г.
1
2
6
5
3
4
1. Процесс выравнивания S и P
электронных облаков
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
6
2
3
5
4
2. Гомолог метана, формула которого C 4 H 10.
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
6
5
3
Б
У
Т
А
Н
4
3. Основной компонент болотного газа
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
6
5
М
Е
Т
А
Н
4
Б
У
Т
А
Н
4. Вещества относящиеся к одному классу, но отличающиеся друг от друга на одну или несколько групп -CH 2 -
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
6
Г
О
М
О
Л
О
Г
И
5
М
Е
Т
А
Н
Б
У
Т
А
Н
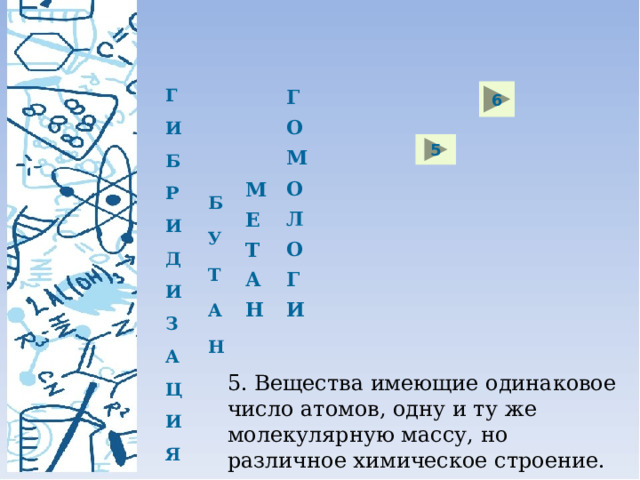
5. Вещества имеющие одинаковое число атомов, одну и ту же молекулярную массу, но различное химическое строение.

Г
О
М
О
Л
О
Г
И
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
6
И
З
О
М
Е
Р
Ы
М
Е
Т
А
Н
Б
У
Т
А
Н
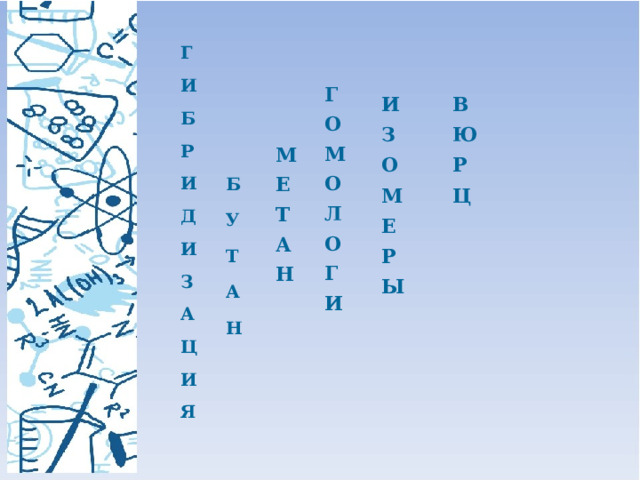
6. Ученый, который получил этан из галогеннопроизводных предельных углеводородов с металлическим натрием.
Г
И
Б
Р
И
Д
И
З
А
Ц
И
Я
Г
О
М
О
Л
О
Г
И
В
И
З
Ю
О
Р
М
Ц
Е
Р
Ы
М
Е
Т
А
Н
Б
У
Т
А
Н
Этапы маршрута
5. Порт
1. Фарватер основных понятий
4. Залив знаний
2. Море классов
органических соединений
3. Рифы химических формул
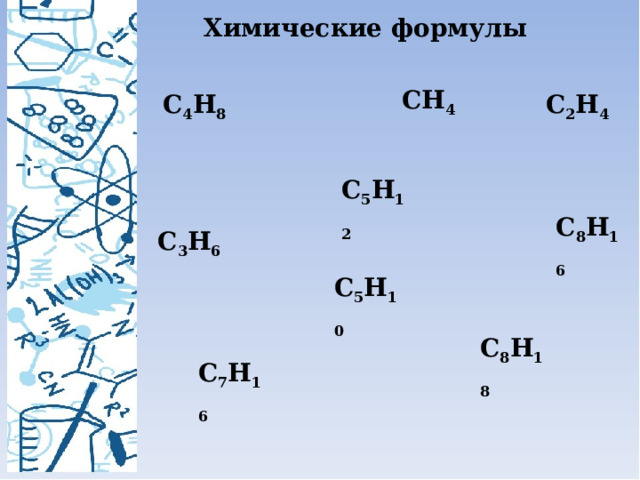
Химические формулы
CH 4
C 4 H 8
C 2 H 4
C 5 H 12
C 8 H 16
C 3 H 6
C 5 H 10
C 8 H 18
C 7 H 16
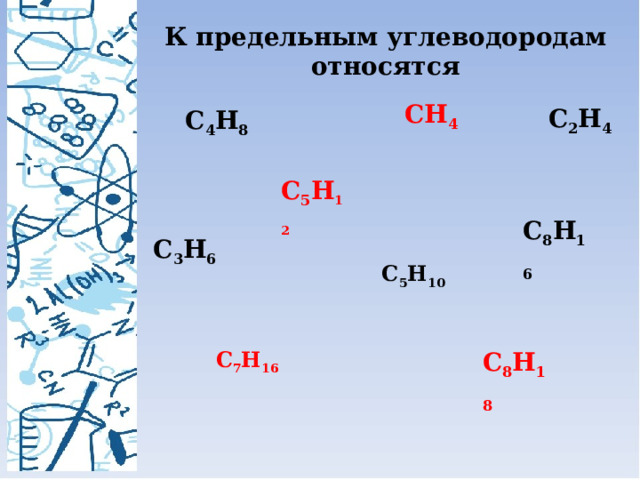
К предельным углеводородам относятся
CH 4
C 2 H 4
C 4 H 8
C 5 H 12
C 8 H 16
C 3 H 6
C 5 H 10
C 8 H 18
C 7 H 16
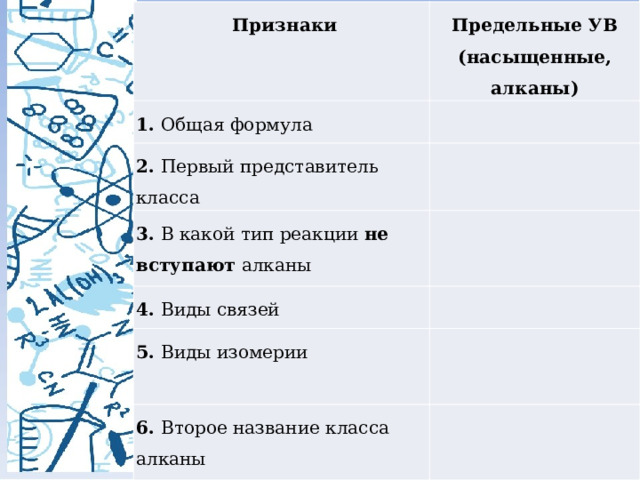
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
2. Первый представитель класса
3. В какой тип реакции не вступают алканы
4. Виды связей
5. Виды изомерии
6. Второе название класса алканы
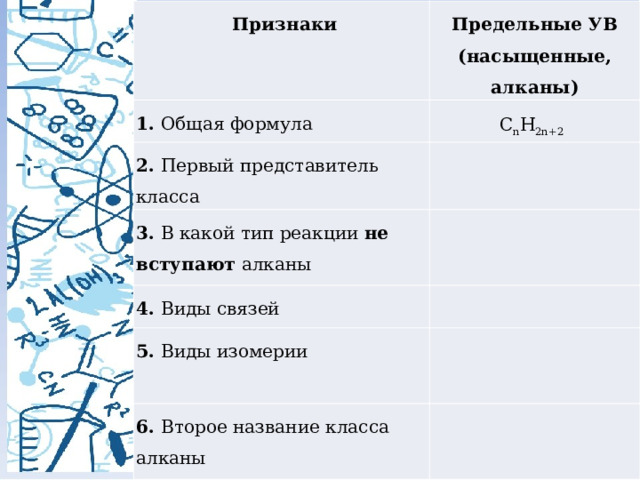
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
3. В какой тип реакции не вступают алканы
4. Виды связей
5. Виды изомерии
6. Второе название класса алканы
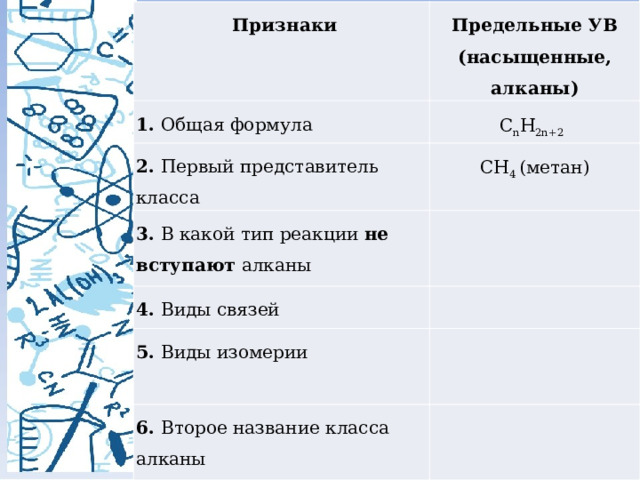
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
CH 4 (метан)
3. В какой тип реакции не вступают алканы
4. Виды связей
5. Виды изомерии
6. Второе название класса алканы
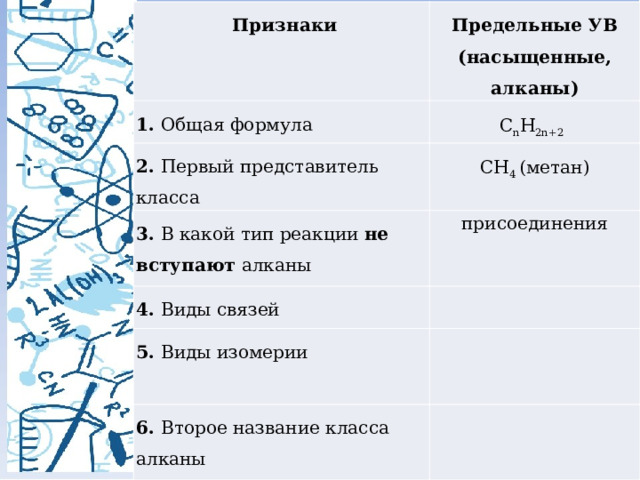
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
CH 4 (метан)
3. В какой тип реакции не вступают алканы
присоединения
4. Виды связей
5. Виды изомерии
6. Второе название класса алканы
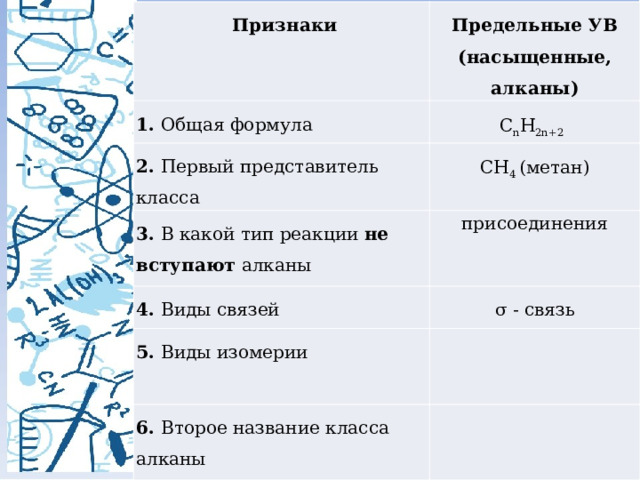
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
CH 4 (метан)
3. В какой тип реакции не вступают алканы
присоединения
4. Виды связей
σ - связь
5. Виды изомерии
6. Второе название класса алканы
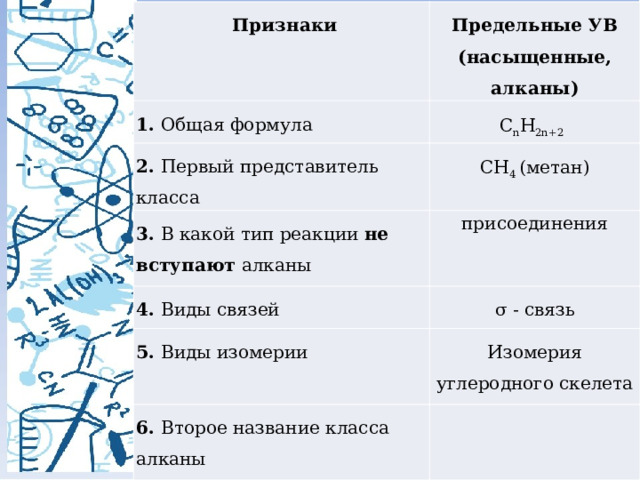
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
CH 4 (метан)
3. В какой тип реакции не вступают алканы
присоединения
4. Виды связей
σ - связь
5. Виды изомерии
Изомерия углеродного скелета
6. Второе название класса алканы
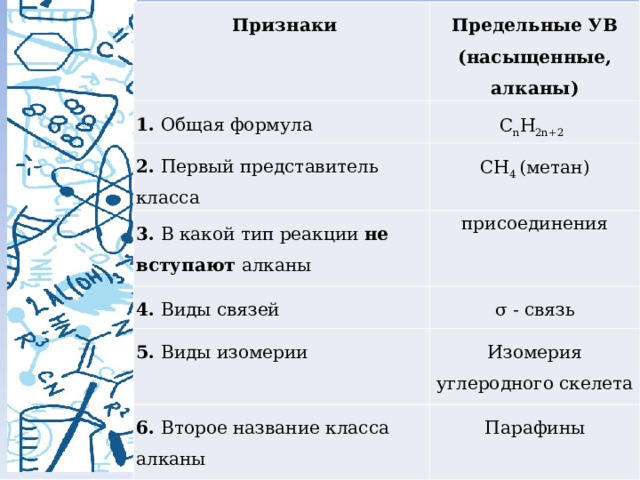
Признаки
Предельные УВ
1. Общая формула
(насыщенные, алканы)
C n H 2n+2
2. Первый представитель класса
CH 4 (метан)
3. В какой тип реакции не вступают алканы
присоединения
4. Виды связей
σ - связь
5. Виды изомерии
Изомерия углеродного скелета
6. Второе название класса алканы
Парафины
Этапы маршрута
5. Порт
1. Фарватер основных понятий
4. Залив знаний
2. Море классов
органических соединений
3. Рифы химических формул

Реакция дегидрирования алканов
Тема: Алкены. Общая характеристика.
Получение алкенов и их свойства.
Цель : Изучить класс непредельных углеводородов. Дать краткую характеристику.

Немного из истории…
Иоганн Иоахим Бехер (1635 – 1682)
Немецкий химик и врач
C 2 H 5 OH → C 2 H 4 + H 2 O
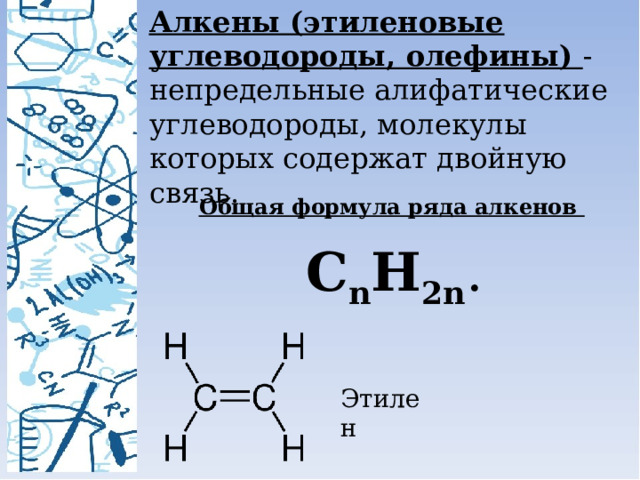
Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь.
Общая формула ряда алкенов
C n H 2n .
Этилен
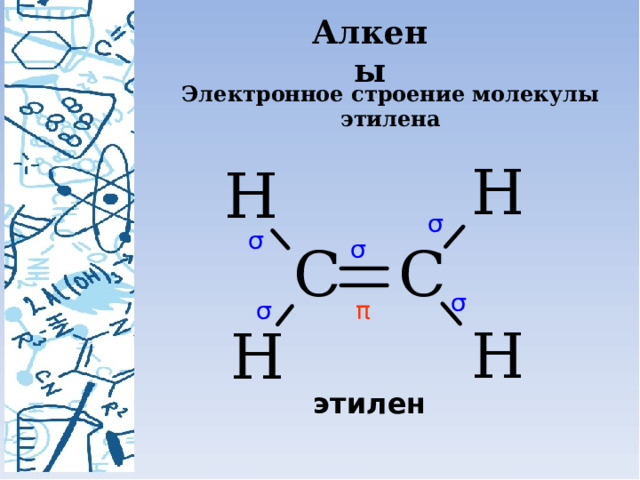
Алкены
Электронное строение молекулы этилена
σ
σ
σ
σ
σ
π
этилен
Этапы маршрута
5. Порт
1. Фарватер основных понятий
4. Залив знаний
2. Море классов
органических соединений
3. Рифы химических формул
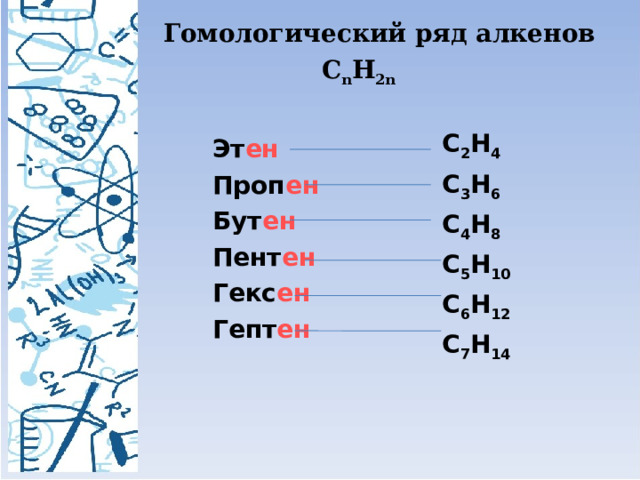
Гомологический ряд алкенов
С n Н 2n
C 2 H 4
C 3 H 6
C 4 H 8
C 5 H 10
C 6 H 12
C 7 H 14
Эт ен
Проп ен
Бут ен
Пент ен
Гекс ен
Гепт ен
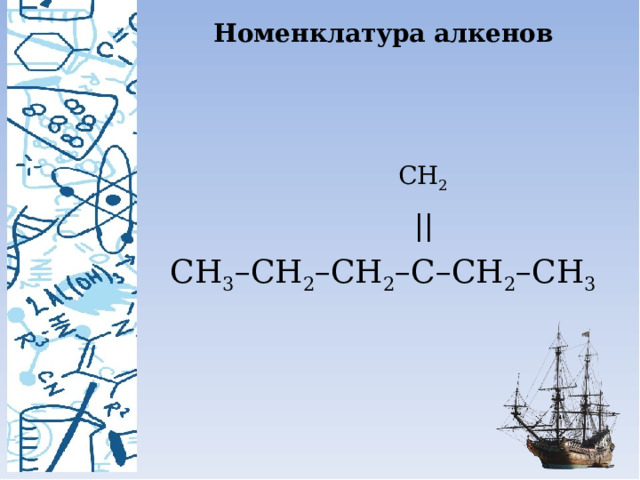
Номенклатура алкенов
СН 2
||
СН 3 –СН 2 –СН 2 –С–СН 2 –СН 3
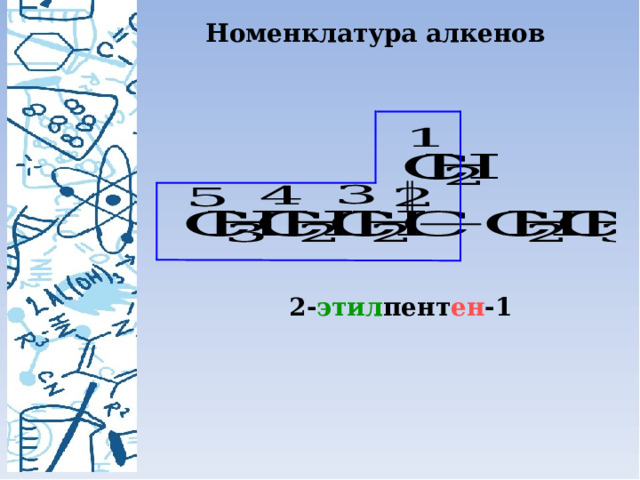
Номенклатура алкенов
2- этил пент ен -1
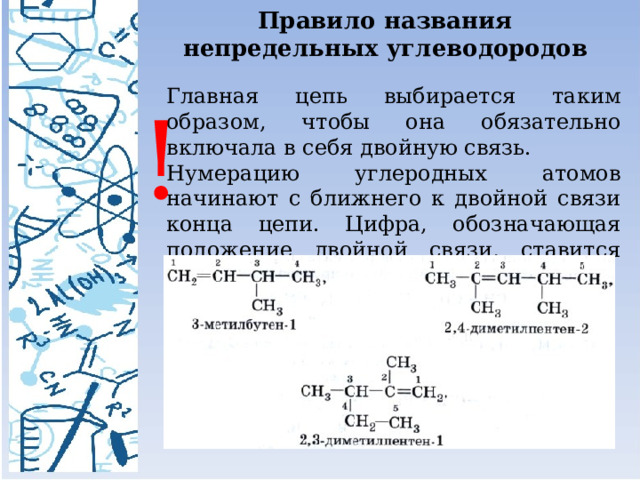
Правило названия
непредельных углеводородов
Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь.
Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится после суффикса – ен .
!

Радикалы алкенов
– СН=СН 2 –СН 2 -СН=СН 2
винил аллил
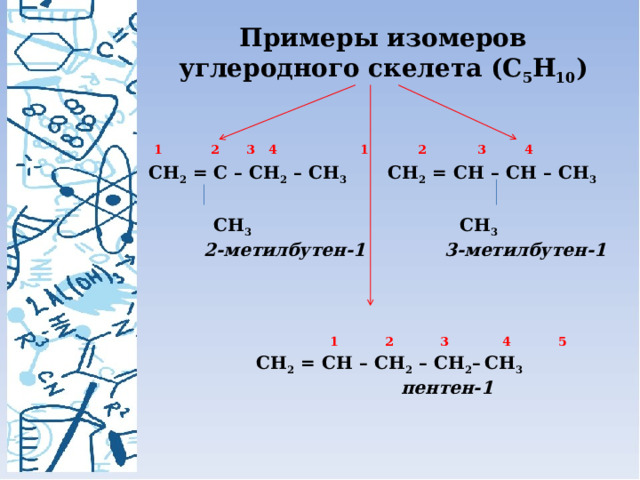
Примеры изомеров углеродного скелета (С 5 Н 10 )
1 2 3 4 1 2 3 4
СН 2 = С – СН 2 – СН 3 СН 2 = СН – СН – СН 3
СН 3 СН 3
2-метилбутен-1 3-метилбутен-1
1 2 3 4 5
СН 2 = СH – СН 2 – СН 2 – СН 3
пентен-1
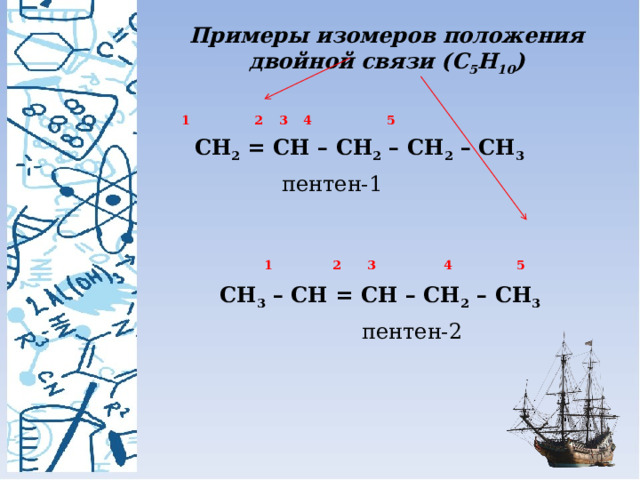
Примеры изомеров положения двойной связи (С 5 Н 10 )
1 2 3 4 5
СН 2 = СН – СН 2 – СН 2 – СН 3
пентен-1
1 2 3 4 5
СН 3 – СН = СН – СН 2 – СН 3
пентен-2
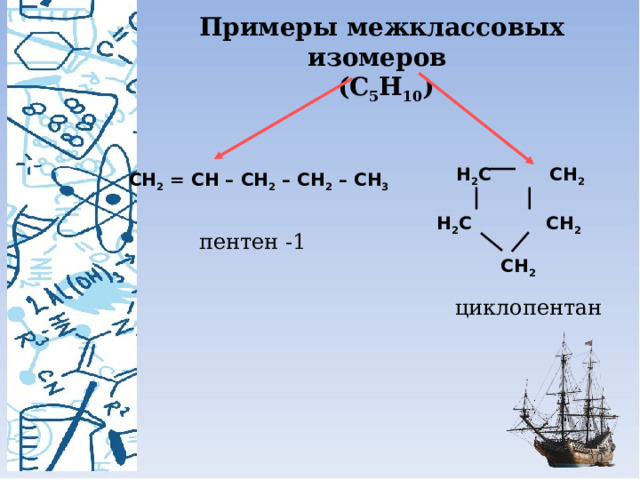
Примеры межклассовых изомеров
(С 5 Н 10 )
Н 2 С СН 2
СН 2 = СН – СН 2 – СН 2 – СН 3
Н 2 С СН 2
пентен -1
СН 2
циклопентан

Физические свойства алкенов
Алкены плохо растворимы в воде, но хорошо растворяются в органических растворителях.
С 2 – С 4 - газы
С 5 – С 17 - жидкости
С 18 … - твёрдые вещества
С увеличением молекулярной массы алкенов, в гомологическом ряду, повышаются температуры кипения и плавления, увеличивается плотность веществ.

Распространение в природе
В отличие от предельных УВ алкены в природе, как правило, не встречаются, что объясняется их высокой химической активностью. Этилен может входить в состав природного и попутного газов, правда содержание его невелико (0,5- 4%). Газообразные алкены выделяют из газов нефтепереработки, а также из газов коксообразования угля.
Этапы маршрута
5. Порт
1. Фарватер основных понятий
4. Залив знаний
2. Море классов
органических соединений
3. Рифы химических формул
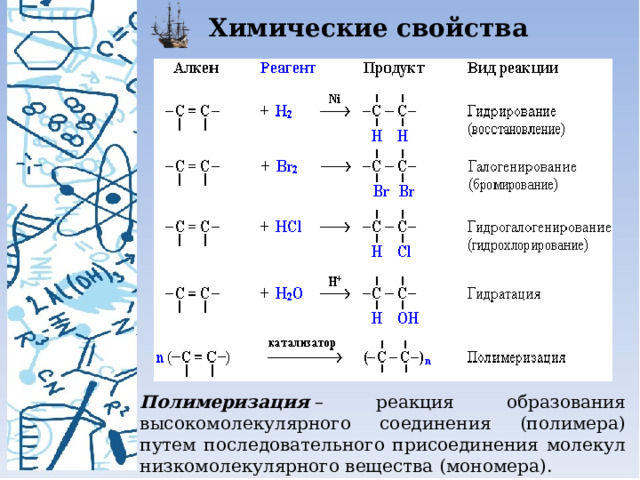
Химические свойства
Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера).

Получение алкенов
1. Дегидрогалогенирование моногалогеналканов при действии спиртового раствора щелочи
2. Дегидратация спиртов при температуре менее 150°C в присутствии водоотнимающих реагентов
Реакции элиминирования идут в соответствии с правилом Зайцева :
Отщепление атома водорода в реакциях дегалогенирования и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода.
Этапы маршрута
5. Порт
1. Фарватер основных понятий
4. Залив знаний
2. Море классов
органических соединений
3. Рифы химических формул

Домашнее задание
Электронная библиотечная система
ПРОФСПО.
1. Хамитова, А. И. Органическая химия для студентов СПО 2016. — 172 c.
Стр. 12-15
2. Стр.15 Задания для самостоятельной работы № 1,2,3.

Спасибо за внимание!
До скорой встречи!


























































